Что такое эхинококкоз?
Для того чтобы начинать говорить о симптомах заболевания и тем более о профилактике и предотвращении заражения паразитами, необходимо четко понимать с чем мы имеем дело.
И так, эхинококкоз – это заболевание вызванное паразитами из группы ленточных червей. Заболевание поражает паразитными кистами, образованными в тканях внутренних органов, чаще всего в печени и легких.
Как экхинококкозный паразит попадает в организм?
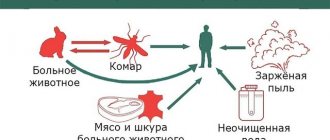
Эхинококкоз – это болезнь зооноз, так как передается от животного к человеку, но какой путь паразит проходит, прежде чем попадает в организм человека?
Промежуточными переносчиками паразита являются травоядные и всеядные животные, употребившие зараженные яйцами пищу и воду. Далее в организме животного паразит проходит свою личиночную стадию, которая проходит во внутренних органах.
Окончательным носителем является плотоядное животное. Паразит проживает в кишечнике, а окончательный носитель заражается, поедая зараженные кистами органы промежуточных животных.
Человек выступает как случайный промежуточный носитель. Все дело в том, что лди могут заразиться эхинококкозом та же, как и промежуточные носители — животные, но не могут передать заражение окончательному носителю.
Симптомы эхинококкоза.
При заражении в человеческом организме развивается от одной до нескольких гидатид. Они чаще всего локализируются в печени или легких, в редких случаях инфекция затрагивает иные органы и ткани.
Человек может быть заражен эхинококкозом, но не подозревать об этом на протяжении многих лет. Все это может продолжаться до момента проявления клинических признаков. При этом более половины зараженных пациентов, получают курс лечения после прохода большого количества времени от начала заражения инфекцией.
Основными симптомами заболевания может быть боль в животе и его области, тошнота и рвота, эти признаки характерны для эхинококкоза печени. В случаях заражения легочной ткани замечаются боли в груди, нехватка воздуха при вдохе или хронический кашель.
Почему мы рассматриваем эхинококкоз легких и печени?
Все дело в том, что на локализацию в печени и легких приходится наибольший процент случаев заражения инфекцией. Ниже мы рассмотрим эхинококкоз печени и легких отдельно и подробнее.
Роль паразитов в структуре заболеваемости населения Российской Федерации в последние годы неуклонно возрастает. Все чаще эхинококкоз встречается в неэндемичных очагах, где врачи не знакомы или мало знакомы с основными принципами его диагностики и лечения, что нередко приводит к позднему выявлению заболевания и к досадным ошибкам в лечении. Эти факты заставляют уделять более пристальное внимание проблеме эхинококковой инвазии. Ведь помимо того, что страдают, как правило, молодые трудоспособные люди, а также дети, более чем 2/3 пациентов требуется хирургическое лечение. К сожалению, остается высокой частота рецидивов заболевания, что вызывает вполне понятную неудовлетворенность хирургов результатами лечения этой категории больных [2, 4, 8]. В этой работе мы ставили своей целью обсудить основные особенности развития эхинококка и соответственно течения заболевания, а также важные моменты хирургического и консервативного лечения инвазии.
Биология паразита
Возбудителем эхинококкоза является цепень Echinococcus granulosus
, который паразитирует на плотоядных животных. Эхинококкоз относится к тяжелым паразитарным заболеваниям и в своем развитии всегда проходит стадию формирования кист. Эхинококкоз человека и животных одинаков, и для полного развития паразита обязательно необходим промежуточный хозяин.
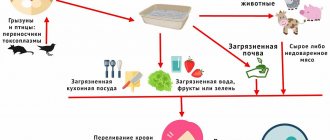
Промежуточные хозяева паразита — человек и сельскохозяйственные животные. Окончательные хозяева, например собаки, заражаются, поедая внутренности животных с эхинококковыми кистами. Содержащиеся в кисте зародышевые элементы (протосколексы и ацефалоцисты) прикрепляются к стенке тонкой кишки животного и вырастают во взрослые особи. Созревшие членики, содержащие 400—800 онкосфер, отрываются от брюшка протосколекса; инфицированные фекалии собак загрязняют траву, землю; яйца попадают в кишечник овец, свиней, верблюдов или человека, на шерсть собак. Человек может заразиться, гладя собаку, употребляя в пищу загрязненные овощи. Важно понимать, что роль мясных продуктов минимальна, так как и человек, и сельскохозяйственные животные являются промежуточными хозяевами, а термическая обработка мяса практически всегда приводит к гибели паразита. Возможность заражения через мясо играет роль только у лиц, занятых убоем скота, разделкой мяса и шкур [2, 4, 8].
Распространенное даже среди некоторых медицинских работников мнение о возможности заражения здорового человека от больного в корне неверно. В работе с заразившимися эхинококкозом и их окружением стоит обращать особое внимание на такого рода разъяснительные беседы, поскольку часто таких пациентов зачем-то изолируют. Однако, сталкиваясь со случаем заражения эхинококкозом одного из членов семьи, всегда имеет смысл обследовать и остальных. Это связано не с тем, что они заражают друг друга, а с тем, что члены одной семьи вместе могли употребить пищу, уже содержавшую яйца эхинококка.
После попадания яйца эхинококка (онкосферы) в организм промежуточного хозяина происходит следующее. Онкосферы покрыты оболочкой, которая растворяется под действием желудочного сока. Высвободившиеся паразиты пробуравливают слизистую оболочку кишечника и через систему воротной вены попадают в печень, где развиваются в зрелую кисту. Большинство паразитов задерживается в печеночных синусоидах, поэтому 70% эхинококковых кист формируются именно в печени. Отдельные яйца проходят через печень и, минуя сердце, задерживаются в легочном капиллярном русле, что приводит к образованию легочных кист (15—20%). Эхинококковое поражение сердца также возможно, но отмечается довольно редко — менее чем у 0,5% больных. Это связывают с высокой скоростью потока крови через орган. При попадании паразита в большой круг кровообращения образуются кисты (10—15%) в селезенке, головном и костном мозге и т. д. Как казуистические описаны наблюдения изолированного эхинококкоза подкожной клетчатки ног, связки матки, глаза, щитовидной и поджелудочной желез [1, 3, 7]. Таким образом, при подозрении на эхинококкоз в первую очередь целесообразно обследовать первый орган-мишень печень, а затем легкие.
Из зародыша эхинококка в течение нескольких месяцев развивается материнская киста, представляющая собой пузырь, заполненный жидкостью. Стенка эхинококковой кисты состоит из двух оболочек: наружной кутикулярной и внутренней герминативной (зародышевой). Кутикулярная и герминативная оболочки макроскопически представлены единой капсулой, поэтому чаще всего они фигурируют под единым понятием «хитиновая оболочка». Снаружи эхинококковая киста окружена плотной соединительнотканной фиброзной капсулой, образующейся из тканей органа в результате защитной реакции промежуточного хозяина против продуктов метаболизма паразита [3].
Диагностика эхинококкоза
В раннем периоде эхинококкоз протекает практически бессимптомно. В связи с этим больные зачастую обращаются за медицинской помощью, когда паразитарная киста достигает значительных размеров, сдавливая соседние органы, или в связи с прорывом кисты в плевральную полость или в бронхи и т. д.
Решающее значение в диагностике ранних стадий, а также в качестве подтверждающего метода при наличии радиологических признаков эхинококкоза имеют иммунологические исследования — выявление в крови специфических антител к эхинококку с помощью реакции иммуноферментного анализа (ИФА). Высокое содержание специфических антител наблюдается у 95% больных с активным процессом: при локализации живых кист паразита в печени, брюшной полости и забрюшинном пространстве, а также при множественном и сочетанном поражении внутренних органов. Имеет смысл выполнять не качественный, а количественный анализ на эхинококкоз в связи с высокой частотой ложноположительных результатов при качественном анализе.
Эозинофилия встречается в 18—83% наблюдений; некоторые авторы отмечают характерное для больных эхинококкозом повышение количества лейкоцитов, общего белка плазмы крови. Количество лимфоцитов крови обычно снижено; уровень всех классов иммуноглобулинов крови чаще повышен. Оговоримся, что все эти изменения состава крови характерны для активных форм и даже полиорганного поражения паразитом. При 1—2 даже зрелых кистах картина периферической крови, как правило, существенных изменений не претерпевает.
Ведущим методом лучевой диагностики эхинококкоза печени и прочих органов является ультразвуковое исследование (УЗИ). Метод общедоступен и позволяет диагностировать эхинококкоз в стадии, когда паразитарные кисты имеют еще небольшой размер, начиная с 1,5—2 см.
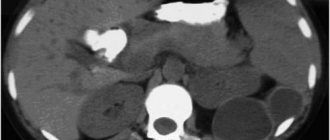
На сонограмме сама эхинококковая киста представляет собой гипоэхогенное (анэхогенное) образование с двойным контуром. Это и есть хитиновая оболочка, которая выглядит как гиперэхогенный внутренний слой кисты. Внутри нее нередко определяются множественные подвижные гиперэхогенные включения по типу осадка. Это зародышевые элементы эхинококка, так называемый «гидатидный песок». Фиброзная капсула выглядит как гиперэхогенный ободок и отделена от хитиновой оболочки гипоэхогенным слоем — «лимфатической щелью» (рис. 1).
Рис. 1. Сонограмма эхинококковой кисты печени. Определяется анэхогенное образование с базальным усилением, гипоэхогенным ободком и четким двухконтурным строением стенки.
Ленточная гиперэхогенная структура в просвете кисты (отслоившаяся хитиновая оболочка), как и дополнительные кистозные включения (дочерние кисты), патогномоничны только для эхинококковых кист (рис. 2).
Рис. 2. Сонограмма эхинококковой кисты с отслоившейся хитиновой оболочкой (ленточная гиперэхогенная структура, указана стрелками). Диагноз эхинококкоза правомочен уже при сочетании двух—трех из указанных признаков [3].
При размере кисты до 30—40 мм эти признаки слабо выражены, что чрезвычайно затрудняет дифференциальную диагностику, поэтому при небольших кистах, помимо ИФА крови на эхинококкоз, целесообразно выполнение магнитно-резонансной томографии (МРТ). Как правило, МРТ позволяет определить признаки, характерные для паразитарной кисты [9].
Лечение
Для химиотерапии эхинококковой инвазии разработан препарат альбендазол. Однако в качестве единственного метода лечения альбендазол эффективен лишь на ранних стадиях заболевания, пока не сформировалась плотная фиброзная капсула с лимфатической щелью вокруг собственно паразитарной кисты [4]. Эти структуры надежно защищают эхинококк от системных воздействий. В связи с этим наиболее распространенным методом лечения большинства больных эхинококкозом является хирургическое вмешательство [3, 7].
Для хирургического лечения эхинококкоза разработано три типа вмешательств: традиционные открытые, лапароскопические и миниинвазивные чрескожные. По данным мировой статистики, в настоящее время миниинвазивные вмешательства применяют почти у трети больных эхинококкозом [5, 7, 8]. При этом хирурги более склонны к щадящим вмешательствам в странах, относящихся к эндемичным, где число больных существенно больше. В тех странах, где болезнь встречается спорадически, все еще доминирует чрезмерно радикальный подход с преобладанием тотальной перицистэктомии либо резекции печени.
Привлекательная, на первый взгляд, методика лапароскопического удаления эхинококковых кист себя не всегда оправдывает. Дело в том, что различные технические приспособления, препятствующие попаданию гидатидной жидкости в брюшную полость, по мере спадения полости уже не позволяют надежно исключить риск обсеменения. С этим связана высокая частота рецидивов после операции. В последние годы показания к лапароскопической операции при эхинококкозе печени были пересмотрены, и техническая доступность кисты уже не считается одним из основных показаний к ней. Лапароскопические вмешательства целесообразны при технической возможности удаления кисты без ее вскрытия, т. е. при возможности выполнения так называемой идеальной эхинококкэктомии. Такая ситуация складывается при краевом либо экстраорганном расположении кисты, что встречается крайне редко [7, 10].
Чрескожная эхинококкэктомия на сегодняшний день является стандартом оперативного лечения больных эхинококкозом печени при кистах I—II типа по классификации Gharbi [6]. Методика сочетает в себе преимущества малотравматичного доступа и возможность эрадикации паразита [1, 5, 9]. По мере накопления опыта пересматриваются и противопоказания к чрескожным вмешательствам. Наш опыт свидетельствует, что традиционные противопоказания к чрескожной эхинококкэктомии, такие как расположение кисты поверхностно, подкапсульно, внепеченочно, близко к магистральным сосудам и протокам в ткани печени или вне ее, а также наличие небольшого количества дочерних кист внутри материнской, весьма относительны. Такие особенности несколько усложняют операцию, но при квалифицированном ее выполнении не влияют на результат [3, 5].
Главным и по сути единственным противопоказанием к чрескожной эхинококкэктомии является выход зародышевых элементов за пределы фиброзной капсулы — так называемое экзогенное почкование. При таком варианте кисты нет возможности воздействовать гермицидом на отпочковавшийся фрагмент, и это почти всегда приводит к рецидиву болезни.
Методика чрескожной эхинококкэктомии из печени
В зарубежной практике методика чрескожной эхинококкэктомии фигурирует под аббревиатурой PAIR — puncture, aspiration, injection, and respiration (пункция, аспирация, инъекция и реаспирация). Как нетрудно догадаться, это перечисление основных этапов операции [5].
Чрескожное вмешательство при эхинококкозе требует весьма тщательного соблюдения методики выполнения операции. Основными требованиями являются использование при первичном вхождении в кисту иглы-катетера и чреспеченочный доступ проведения инструмента. При первичной пункции живой эхинококковой кисты абсолютно недопустимо применение методики Сельдингера, т. е. введение катетера по проводнику после удаления пункционной иглы. Поскольку гидатидная жидкость находится в кисте под большим давлением, излияние ее с обсеменением полости в процессе замены иглы на катетер неизбежно. По этой же причине необходим чреспеченочный доступ к кисте, какой бы заманчивой и безопасной не казалась траектория пункции вне органа. Ткань печени служит дополнительным барьером между кистой и свободной брюшной полостью.
Итак, после пункции кисты иглой-катетером под контролем УЗИ выполняют противопаразитарную обработку эффективным гермицидом. Гидатидную жидкость полностью удаляют и отправляют на паразитологическое исследование для дополнительной верификации диагноза. Оставшуюся полость в соответствующем объеме по катетеру заполняют гермицидом. Одним из наиболее эффективных интраоперационных гермицидов с доказанным противопаразитарным действием на Echinococcus granulosus in vitro
и
in vivo
является 87% водный раствор глицерина с экспозицией не менее 7 мин. Именно этап удаления гидатидной жидкости и противопаразитарной обработки является наиболее ответственным во всей операции и требует скрупулезного соблюдения методики. Высок риск излияния жидкости в окружающее пространство с развитием в отдаленном периоде обсеменения и рецидива либо выраженной аллергической реакции у пациента во время операции вплоть до анафилаксии. В связи с этим целесообразна превентивная профилактика анафилактических реакций путем заблаговременного интраоперационного введения дозы кортикостероида. Экспозиция гермицида длительнее 7 мин не оправдана. Экспериментальные исследования на мышах подтвердили, что для полной гибели протосколексов экспозиции 87% водного раствора глицерина в течение 6—7 мин достаточно.
После полного удаления гермицида наступает этап собственно эхинококкэктомии, т. е. удаления всех элементов паразита с хитиновой оболочкой. После обработки глицерином, т. е. уничтожения живых протосколексов, уже возможна замена иглы-катетера на дренаж достаточного диаметра (не менее 16 Fr) по проводнику. Это позволяет при определенном опыте полностью удалить все элементы паразита и хитиновой оболочки в первые сутки после операции. Возможно ли оставление оболочки в уже обработанной гермицидом кисте? Возможно, но нецелесообразно, потому что почти всегда сохраняется остаточная полость, риск нагноения которой достоверно почти в 2 раза выше при оставленной оболочке. После удаления максимально возможного объема хитиновой оболочки дренаж из кисты можно извлекать и считать эхинококкэктомию завершенной.
После чрескожной эхинококкэктомии перед хирургом встает вопрос об остаточной полости после операции. Однозначного решения этой проблемы пока нет. Нами эмпирически установлено, что у детей практически всегда остаточная полость самостоятельно закрывается в течение первого года после операции. У взрослых сокращение объема полости происходит реже. При этом попытки повторных вмешательств с целью дополнительного склерозирования полости только усугубляют ситуацию.
Опыт показывает, что остаточная полость требует выжидательной тактики и динамического наблюдения. Чем больше сроки наблюдения, тем меньше число больных с остаточной полостью. В то же время чем чаще повторные вмешательства, тем ригиднее и устойчивее к воздействиям становятся стенки кисты. В принципе очевидно, что существование остаточной полости малых размеров, порядка 4—5 см, не оказывает существенного влияния ни на функцию печени, ни на организм в целом. Выработанного международного алгоритма в отношении остаточных полостей пока нет. На основании собственного опыта мы пришли к выводу, что при клинически значимой остаточной полости более эффективна ее микроволновая абляция, чем повторное чрескожное дренирование и склерозирование.
Стоит коснуться и традиционных открытых методов лечения эхинококкоза печени. С накоплением опыта сформировались четкие показания к выполнению лапаротомии при эхинококкозе. На сегодняшний день необходимость большой травматичной операции нередко обусловлена обсеменением брюшной полости в случае несоблюдения правил анти- и апаразитарности при предыдущем лапароскопическом или чрескожном вмешательстве [7, 9].
Общее стремление к минимизации травматичности операции коснулось и традиционного хирургического лечения при эхинококкозе печени. Доказано, что простая эхинококкэктомия, заключающаяся во вскрытии и противопаразитарной обработке кисты с последующим удалением оболочек и при необходимости капитонажем остаточной полости, дает столь же удовлетворительные отдаленные результаты в отношении рецидива заболевания, как и тотальная перицистэктомия или резекция печени, т. е. полное удаление кисты даже вместе с фиброзной капсулой [7].
Несмотря на усовершенствование методик вмешательства, соблюдение принципов анти- и апаразитарности выполнения хирургического вмешательства, внедрение различных химических и физических методов воздействия на паразита, использование совершенного инструментария, частота рецидивов заболевания остается высокой и достигает 5—33% [8, 10], поэтому огромное влияние на результаты лечения оказывает последующая химиотерапия, или противогельминтная терапия. Она необходима и для воздействия на отсевы эхинококка малых размеров, недоступные современным методам диагностики. Несколькими многоцентровыми исследованиями, в которых участвовала и наша клиника, доказано, что курс специфических противопаразитарных препаратов строго обязателен для предупреждения рецидива болезни даже после идеально выполненной операции [7—9].
Наиболее эффективными и общепринятыми препаратами, воздействующими на гидатидозный эхинококк, являются альбендазол и его аналоги [4, 9]. Досадно, что хирурги не очень охотно рекомендуют больным послеоперационное медикаментозное лечение. Преобладающая точка зрения о чрезвычайной токсичности препарата не соответствует действительности. Более того, химиотерапия оправдана и в качестве самостоятельного метода лечения при кистах размером до 3 см и менее, особенно при легочном эхинококкозе. Подчеркнем, однако, что при кисте большого размера показано обязательное оперативное лечение в том или ином объеме, поскольку применение в этом случае только альбендазола малоэффективно.
Таким образом, научные достижения последних лет кардинально изменили подходы к диагностике и выбору метода лечения больных эхинококкозом. Новые аспекты морфологии паразита показали, что результатом применения современных высокоинформативных инструментальных методов исследования является не просто констатация факта наличия кисты, но и указание в протоколе исследования ее характеристик, размера, характера содержимого, формы, описание формы дочерних кист, упоминание о наличии экзо- и эндогенно почкующихся кист, степени их проникновения в фиброзную капсулу. Наиболее эффективными в этом плане признаны УЗИ и МРТ. Выявление кистозных образований практически всегда требует проведения серологических реакций на эхинококкоз. Больные эхинококкозом независимо от размера и локализации кист не подлежат динамическому наблюдению и должны быть направлены в хирургический стационар, располагающий опытом лечения таких больных. Обязательным является комплексный подход, включающий применение послеоперационной противогельминтной терапии. Хирургическому лечению подлежат все больные с эхинококковыми кистами размером более 3 см. Выбор методики вмешательства определяется в зависимости от технической возможности стационара и характеристик самой кисты.
Авторы заявляют об отсутствии конфликта интересов.
Эхинококкоз печени.
На данный вид инфекции приходится от пятидесяти до семидесяти процентов всех случаев заболевания эхинококкозом. Личинки паразита попадают по кровотоку от стенок кишки в печень, где большинство из них оседает на мелких капиллярах. Со временем кисты медленно, но прогрессируют, тем самым прорываются во внутреннюю среду печени.
К наиболее ранним симптомам эхинококкоза печени можно отнести:
- Тяжесть и боль в эпигастральной области
- Тяжесть и боль в области правого подреберья
Связано это с развитием кисты именно в правой доле печени.
Актуальность проблем эхинококкоза и альвеококкоза
Актуальность проблем эхинококкоза и альвеококкоза связана с их широкой распространенностью, многообразием негативных воздействий на организм человека и выраженным полиморфизмом клинических проявлений. По данным Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, заболеваемость эхинококкозом на территории Российской Федерации в 2008 году увеличилась по сравнению с предыдущим годом на 5,4 %. Всего был зарегистрирован 551 случай гидатидного и альвеолярного эхинококкоза (0,39 на 100 тыс. населения) в 63 субъектах Российской Федерации против 527 случаев (0,37 на 100 тыс. населения) в 2007 году в 56 субъектах Российской Федерации. Среди детей до 14 лет зарегистрирован 71 случай эхинококкоза (0,34 на 100 тыс.), в 2007 году – 49 случаев (0,23 на 100 тыс. детей). Доля городских жителей в последние два года составляет 48% от общего числа заболеваний.
На территории Российской Федерации систематически регистрируются летальные исходы от эхинококкоза. За период с 1996 год по 2008 год зарегистрировано 109 летальных исходов, наибольшее число которых приходится на Красноярский край (21,1%) и Оренбургскую область (19,2%). По данным формы №5 вет. «Сведения о ветеринарно-санитарной экспертизе сырья и продуктов животного происхождения за 2008 год» на рынках выявлено 72 371 проб мяса с эхинококковыми пузырями в 46 субъектах Российской Федерации. Процент зараженности мяса крупного рогатого скота составил 2,31%, овец – 3,5%, свиней – 1,17%.
Проведен анализ госпитализации больных с эхинококкозом и альвеококкозом в КГБУЗ «Краевой онкологический диспансер им. А.И. Крижановского» с 2004 – 2008 гг.
За этот период было пролечено 47 первичных больных с данной патологией. Из них основная масса женщин (54%).
Наибольшее количество случаев зарегистрировано в городах Красноярске, Лесосибирске, Енисейске, Шарыпово, Ужуре и других городах Красноярского края. Случай эхинококкоза превышают альвеококкоз (60% и 40%, соответственно).
Проведено оперативное лечение 52% больным с благоприятным исходом (ремиссия) и неоперабельные случаи 46%, один смертельный случай. Пациенты наблюдаются у инфекциониста ККБ или по месту жительства с целью проведения противорецидивной терапии Альбендозолом.
Вверх
Эхинококкоз легких.
Развитие эхинококкоза легких встречается реже, чем инфекция в печени и имеет двадцать – тридцать процентов от всех случаев заражений. После попадания инфекции на легочную ткать заболевание начинает прогрессировать.
По мере своего роста, может вызывать:
- Грудную боль
- Кашель (от сухого кашля до мокрого с присутствием крови)
- Проявление отдышки
- В случаях развития особо крупной кисты замечаются деформации грудной клетки
1.Общие сведения
Эхинококк – один из наиболее опасных паразитов, личинка которого может передаваться человеку от зараженных животных (преимущественно псовых), с водой, немытыми ягодами и пр. На определенной стадии развития эхинококки образуют шарообразные кисты диаметром от 1-5 до 20 см (и более) в жизненно важных органах: печени, легких, почках, мозгу и пр. Чаще всего эхинококкоз регистрируется в животноводческих регионах, где складываются наиболее благоприятные условия для распространения гельминта, однако в эпоху тотальных миграций и путешествий заразиться можно, по сути, где угодно.
Легкие поражаются примерно в 15% всех случаев эхинококковой инвазии, и это вторая по частоте встречаемости (после печени) область основного очага. Тяжесть эхинококкоза легких обусловлена объективными трудностями диагностики, обилием осложнений и очевидной опасностью самой локализации кист в дыхательной системе.
Обязательно для ознакомления! Помощь в госпитализации и лечении!
Лечение эхинококкоза в клинике ЮДЖИНА.
Наша клиника специализируется на лечение эхинококкоза легких, печени и иных органов или тканей. Благодаря методике разработанной Евгением Ли, директором и новатором нашей клиники. Специально разработанный медикаментозный способ лечения позволяет раз и навсегда избавиться от эхинококкоза и образовавшихся кист без хирургического и химиотерапевтического вмешательства.
Также наши специалисты всегда рады помочь Вам и провести диагностику Вашего организма, что позволит ясно взглянуть на образовавшуюся проблему и незамедлительно приступить к эффективному лечению. Записаться на наш прием Вы можете двумя способами. Первый – позвонить нам по номеру указанному на сайте. Второй – оставить заявку, заполнив форму справа. Наши операторы всегда готовы помочь и проконсультировать Вас по возникшим у Вас вопросам.
Берегите свой организм и во время пресекайте возможные паразитические заболевания, а клиника ЮДЖИНА станет Вам в этом не заменимым помощником!
4.Лечение
Несмотря на сообщения об успешных курсах химиотерапии при достаточно малых кистах, консервативная терапия при эхинококкозе легких, в целом, неэффективна. На сегодняшний день возможно только хирургическое лечение. Разработаны и с успехом применяются несколько различных методик (эхинококкэктомия, перицистэктомия, в редких случаях и строго по показаниям – резекция легкого). В качестве предпочтительного выбора, если позволяет клиническая ситуация, практикуется т.н. идеальная энуклеация кисты, т.е. удаление эхинококковой капсулы без разрушения ее оболочки. Хирургическая операция проводится, как правило, на фоне интенсивной медикаментозной поддержки.
Методы профилактики эхинококкоза достаточно очевидны: выявление и устранение возможных очагов заражения, строгий контроль санитарного состояния животноводческих комплексов, планомерное уничтожение бродячих животных, прежде всего собак. Разработаны и опубликованы к выполнению рекомендации по регулярной дегельминтизации (а также сокращению численности) служебных собак. Основными мерами индивидуальной профилактики являются исключение употребления некипяченой воды и немытых ягод, обязательная гигиена рук после любого контакта с собаками и любыми другими животными (в особенности это касается детей).