Першение в горле, сухость, жжение, дискомфорт и резкая боль при глотании – наверняка с этими симптомами сталкивался каждый из нас, независимо от пола и возраста.
Особенно обидно, когда внезапная боль в горле нарушает заранее намеченные планы и мешает вести привычный образ жизни. И тогда может возникнуть желание расправиться с болезнью, начав лечиться при помощи антибиотиков. Но такая терапия показана только в том случае, если ее рекомендует врач, самолечение может принести вред. Давайте разберемся, почему.
Как работают антибиотики?
С открытием антибиотиков у человечества в XX веке появилась надежда если не на вечную жизнь, то хотя бы на полное избавление от всех заболеваний. Но этого не произошло. Ведь антибиотики способны бороться только с бактериальными заболеваниями. А против вирусов они бессильны.2
Это значит, что при ОРВИ, гриппе, тонзиллите, фарингите, ларингите и других заболеваниях, вызывающих боль горле, антибиотики могут понадобиться лишь в небольшом проценте случаев, а необходимость их приема может определить только врач.
Правда ли, что антибиотики лечат не всё?
– Постойте! – скажете вы. – Если антибиотики бесполезны, почему их так часто назначают врачи при болях в горле?
Ни один врач без проведения специальных анализов не может определить в 100% случаев, что явилось причиной появления боли в горле – бактерии или вирусы. Поэтому сегодня во всем мире нарастает тенденция чрезмерно частого назначения антибиотиков. Согласно статистике, 80-90% случаев острого воспаления глотки у взрослых людей вызвано вирусной инфекцией, и только у 10-20% к болезни привели бактерии.1 Проблема в том, что бактерии пошли в контрнаступление. Мутируя, некоторые из них научились приобретать устойчивость к лекарствам. То есть при воздействии антибиотика на популяцию происходит самый настоящий естественный отбор по дарвиновской модели. Можно сказать: «То, что бактерии не убивает, делает их сильнее».
Таким образом может развиваться резистентность – невосприимчивость бактерий к антибиотикам. К чему это может привести?
Чем опасна устойчивость к антибиотикам?
По мнению специалистов ВОЗ, резистентность к антибиотикам является сегодня одной из наиболее серьезных угроз для здоровья человечества, продовольственной безопасности и развития.1
И бороться с этой проблемой можно только путем отказа от приема антибиотиков «на всякий случай», для профилактики или надеясь быстрее избавиться от неприятных симптомов. Принимая антибиотики при боли в горле при отсутствии бактериальных заболеваний, вы не поможете себе, а наоборот, можете навредить. Помните: во многих случаях при боли в горле может помочь симптоматическое лечение.
Рейтинг лучших увлажняющих спреев
Препараты с морской водой, растительными маслами устраняют сухость слизистой, что предотвращает размножение болезнетворных микроорганизмов.
Лучшие спреи с увлажняющим действием:
- Аквалор. Популярное средство для быстрого и безопасного лечения болезней ротоглотки. Содержит атлантическую воду, экстракт ромашки и алоэ. Препарат устраняет отечность слизистых, способствует восстановлению поврежденных тканей. Преимущества – безопасен для маленьких детей, беременных и кормящих женщин.
- Аква марис. Спрей на основе морской воды избавляет от воспаления, препятствует развитию осложнений. Преимущества – безопасность, эффективность. Недостатки – цена.
- Каметон. Спрей содержит камфору, эвкалиптовое масло и левоментол. Комбинированное лекарство, антисептик, убирает признаки воспаления, увлажняет слизистые, улучшает отхождение мокроты. Преимущества – удобная насадка, улучшения заметны через на 2-3 день применения, цена. Недостатки – не подходит для лечения детей младше 5 лет, специфический вкус.
- Ингалипт. Препарат с лучшим соотношением цены и качества. Спрей борется с бактериями, купирует боль и першение, увлажняет слизистую. Преимущества – высокая эффективность, удобный распылитель, приемлемая стоимость. Недостаток – выраженный вкус мяты и эвкалипта.
- Аргенто-септ. Спрей с антибактериальным и увлажняющим действием, купирует даже сильную боль, отечность миндалин. Преимущества – безопасность, быстрое действие, приятное послевкусие. Недостаток – цена.
Увлажняющие спреи можно использовать для профилактики в период эпидемий простудных заболеваний.
При каких заболеваниях болит горло?
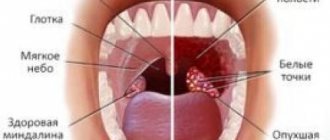
Неприятные ощущения царапания, саднения, чувство инородного тела в горле, боли при глотании пищи – все эти симптомы могут сопровождать фарингит, тонзиллит и ларингит. Эти вирусные заболевания являются достаточно распространенными, они приводят к появлению дискомфорта в горле и способны нарушить многие наши планы.
Фарингит – это острое или хроническое воспаление слизистой оболочки глотки, чаще всего вирусной природы. То есть его бессмысленно лечить антибиотиками, целесообразным будет симптоматическое лечение. Тонзиллит – это воспаление небных миндалин (их еще называют гланды), а ларингит – воспаление слизистой оболочки гортани и голосовых связок, чаще вирусной природы. При лечении этих болезней также успешно применяется симптоматическая терапия.
Антибактериальные препараты при этих заболеваниях требуются в 5-15% случаев, когда причиной заболевания являются стрептококки.2 Для определения возбудителя необходимо бактериологическое исследование мазка из зева, ожидание результата которого может занять некоторое время, иногда до нескольких дней. Поэтому при боли в горле во многих случаях врач может рекомендовать симптоматическую местную терапию, которая помогает бороться с дискомфортом.
Антибактериальная терапия при острых инфекциях ЛОР-органов
И
нфекционные заболевания ЛОР–органов – весьма обширная группа воспалительных заболеваний, каждое из которых человек переносит несколько раз в жизни. В эту группу входят воспалительные болезни околоносовых пазух (риносинуситы), глотки и миндалин (тонзиллофарингиты, ангины) и среднего уха (отиты). Значение этих заболеваний определяется их чрезвычайной распространенностью, особенно в детском возрасте. Так, в США ежегодно регистрируется 31 миллион случаев острого риносинусита (ОРС). По расчетным данным,
в России ОРС ежегодно переносят 10 млн. человек
, но и эта цифра выглядит заниженной, так как учитывает только тяжелые манифестированные формы. По данным Национального центра по статистике болезней в США, расходы, связанные с диагностикой и лечением ОРС, в 1996 году составили 5,8 млрд. долларов.
Острый средний отит (ОСО) – одно из самых распространенных заболеваний детского возраста
. К трехлетнему возрасту ОСО переносят 71% детей, а за первые 7 лет жизни до 95% детей имеют в анамнезе хотя бы один эпизод этого заболевания [10,11]. По данным HMO (Health Maintenance Organization), у 48% детей отмечаются однократные эпизоды острого перфоративного или неперфоративного среднего отита в первые 6 месяцев жизни или более 2 эпизодов за 12 месяцев жизни.
Точных сведений о распространенности ангин и острых тонзиллофарингитов (ОТФ) нет, однако ясно, что это тоже одни из самых распространенных инфекционных болезней человека. У взрослых типичным является поражение нёбных миндалин, у детей чаще встречается аденоидит – воспаление глоточной миндалины. В раннем детском (до 3 лет) и в преклонном (после 50 лет) возрасте частота возникновения ангин ниже, что связано соответственно с возрастным несовершенством или возрастной инволюцией лимфоидной ткани глотки.
В основе патогенеза ОРС, ОСО и ОТФ лежит воспалительная реакция, развивающаяся обычно на фоне острой респираторной вирусной инфекции (ОРВИ). Вирусное инфицирование слизистой оболочки является первой фазой заболевания. Исследования с использованием компьютерной и магнитно–резонансной томографии показали, что у 90% больных ОРВИ в околоносовых пазухах развивается катаральное воспаление слизистой оболочки, имеется застой секрета [6]. Это фактически означает, что катаральный синусит вирусной этиологии наряду с ринитом, ларингитом и ларинготрахеитом является одним из типичных проявлений ОРВИ. Однако лишь у 2% больных развивается вторичное гнойное воспаление, вызванное присоединением бактериальной инфекции, условия для которой возникают в поврежденной вирусом слизистой оболочке. В условиях нормально функционирующего мукоцилиарного транспорта бактерии не имеют возможности достаточно длительно контактировать с клетками эпителия полости носа. При поражении вирусом реснички слизистой оболочки не могут работать в полную силу, и скорость мукоцилиарного транспорта существенно снижается. В условиях стагнации секрета и снижения парциального давления кислорода в околоносовых пазухах создаются оптимальные условия для развития бактериальной инфекции.
Основными возбудителями ОРС считаются Streptococcus pneumoniae
и
Haemophilus influenzae
: они высеваются из пазух примерно у 70–75% больных [2,6]. Среди прочих возбудителей называют
Moraxella catarrhalis, Staphilococcus aureus, Streptococcus pyogenes, Streptococcus viridans
и др. Анаэробные бактерии выявляются при РС в 4–11% случаев, и основными из них являются анаэробные стрептококки. Однако спектр возбудителей ОРС может существенно варьировать в зависимости от географических, социально–экономических и прочих условий.
Аналогичный механизм лежит в основе патогенеза ОСО, причем ведущую роль в развитии заболевания играет нарушение проходимости слуховой трубы. Она ведет к созданию отрицательного давления в барабанной полости и транссудации жидкости. Образовавшийся экссудат изначально является стерильным, но после попадания в барабанную полость патогенных бактерий он принимает воспалительный характер. Результаты микробиологического исследования пунктата барабанной полости свидетельствуют о том, что, как и при ОРС, основными возбудителями ОСО являются Streptococcus pneumoniae и Haemophilus influenzae
– именно те микроорганизмы, различные штаммы которых заселяют носоглотку у большинства детей. Эти два микроорганизма составляют в сумме примерно 60% бактериальных возбудителей заболевания [7,11]. Реже высеваются
Moraxella catarrhalis
(3–10%),
Streptococcus pyogenes
(2–10%),
Staphylococcus aureus
(1–5%). Около 20% посевов из барабанной полости оказываются стерильными. Значительная часть ОСО имеет вирусную этиологию. Определенную роль в этиологии ОСО могут иметь
Mycoplasma pneumoniae
, которая, в частности, способна вызывать буллезный геморрагический мирингит,
Chlamydia trachomatis
и
Chlamydophila pneumoniae
.
Примерно 70% ОТФ вызываются вирусами (риновирусы, коронавирусы, респираторный синцитиальный вирус, аденовирус, вирусы гриппа и парагриппа), среди которых наиболее типичным возбудителем являются риновирусы. Основным бактериальным возбудителем ангин и ОТФ считается b-гемолитический стрептококк группы А (БГСА), наличие которого подтверждается примерно у 31% больных [9]. Среди прочих возможных возбудителей упоминают гемолитические стрептококки других групп, золотистый стафилококк, энтеробактерии, гемофильную палочку.
Существует несколько специфичных форм ОФТ, среди которых важное значение имеют следующие. Острый эпиглоттит – воспаление лимфоидной ткани надгортанника. Возбудителем заболевания чаще бывает Haemophilus influenzae
типа В, реже –
S. pneumoniae, S. aureus
и ряд других возбудителей. Заболевание проявляется высокой температурой, сильными болями в горле, иногда затруднением дыхания. При осмотре гортанным зеркалом или эндоскопом виден резко увеличенный отечный надгортанник, под слизистой оболочкой нередко видны очаги абсцедирования. В тяжелых случаях резко увеличенный надгортанник занимает весь просвет гортаноглотки и приводит к развитию стеноза гортани, который может потребовать трахеостомии.
Ангина боковых (тубофарингеальных) валиков глотки
чаще развивается у лиц, перенесших ранее тонзиллэктомию. В этом случае отмечается компенсаторная гиперплазия тубофарингеальных валиков, которые объединяют в себе трубные миндалины и скопления лимфоидной ткани в боковых стенках глотки, которые при воспалении ярко гиперемированы, отечны, содержат мелкие абсцессы, просвечивающие через слизистую оболочку. Клиническая картина почти не отличается от обычной ангины, за исключением характерной иррадиации болей в уши из–за вовлечения трубных миндалин.
Аденоидит
– воспаление глоточной миндалины обычно встречается у детей и проявляется затруднением носового дыхания, стеканием слизисто–гнойного отделяемого по задней стенке глотки, шейным лимфаденитом. Задняя риноскопия или, точнее, эндоскопия носоглотки позволяют установить правильный диагноз.
Основными целями лечения
при инфекциях ЛОР–органов являются:
- снижение длительности и выраженности симптомов заболевания;
- предупреждение развития осложнений (орбитальных, внутричерепных, ревматической лихорадки, флегмон и абсцессов);
- эрадикация возбудителя.
С этих позиций основным методом лечения инфекций ЛОР–органов является системная антибиотикотерапия
, которая базируется на знании типичных возбудителей или на тестировании чувствительности культуры конкретных микроорганизмов, выделенных из пораженной пазухи, глотки или полости среднего уха. Хотя микробиологические исследования и играют определенную роль в выборе оптимального антибиотика, в большинстве случаев этот выбор является эмпирическим. Выбор антибиотика, направленный на конкретного возбудителя, идентифицированного при бактериологическом исследовании, отнюдь не гарантирует успех в связи с высокой вероятностью попадания в исследуемый материал «путевой» микрофлоры при заборе материала [2]. Кроме того, клиническая картина среднетяжелых и тяжелых инфекций диктует необходимость системного назначения антибиотиков, не дожидаясь результатов микробиологического исследования, которое занимает несколько дней.
Прямая бактериоскопия может в какой–то степени предположить вид возбудителя. Наличие в препарате цепочек или пар мелких грамположительных кокков свидетельствует о том, что вероятным возбудителем является стрептококк (пневмококк), крупных грамположительных кокков – стафилококк. Выявление грамотрицательных бактерий обычно свидетельствует о наличии гемофильной палочки, разнообразных микроорганизмов – о смешанной аэробно–анаэробной инфекции. При выборе антибактериального препарата первостепенное значение имеет чувствительность к нему типичных возбудителей заболевания: S. pneumonia
и
H. influenzae
. Растущая в последние годы резистентность этих микроорганизмов ко многим основным антибиотикам является главной проблемой в рациональной антибиотикотерапии бактериальных инфекций. Уже сейчас почти 5% штаммов
H. influenzae
в России не чувствительны к незащищенным пенициллинам [3].
Острый риносинусит
. Эффективность и целесообразность антибиотикотерапии при ОРС зачастую обсуждается с критических позиций, и плацебо–контролируемые исследования нередко дают противоречивые результаты. Это обусловлено двумя основными факторами:
- преимущественно вирусной этиологией заболевания;
- выраженной тенденцией к спонтанному выздоровлению.
Два недавних исследования вообще не выявили статистически значимых различий между доксициклином и плацебо и амоксициллином и плацебо при лечении ОРС. В последнем из упомянутых исследований клиническая эффективность амоксициллина составила 83%, а плацебо – 77% [8]. В связи с этим считается, что лечению антибиотиками подлежат не все ОРС, а только их среднетяжелые и тяжелые формы
. Поскольку дополнительные методы исследования (РГ, КТ, УЗИ и диафаноскопия) не позволяют дифференцировать вирусное и бактериальное поражение ОНП и не являются показателями степени тяжести заболевания, основными критериями при решении вопроса о назначении антибиотика становятся общее состояние и жалобы больного, анамнез и наличие гнойного отделяемого в носовых ходах.
С клинической точки зрения признаками ОРС, вызванного типичными возбудителями (S. рneumoniae
и
H. influenzae
), являются наличие уровня жидкости на рентгенограмме, снижение обоняния и хороший эффект от традиционной терапии. Отличительными чертами ОРС, вызванного другими микроорганизмами, являются наличие зловонных выделений из носа, тотальное снижение пневматизации ОНП на рентгенограмме и более медленная положительная динамика рентгенологической картины на фоне проводимого лечения [5].
Микробиологическое исследование содержимого околоносовых пазух далеко не всегда выявляет истинного возбудителя ОРС, и результаты исследования чувствительности выявленного микроорганизма in vitro
не всегда коррелируют с клинической эффективностью конкретных антибиотиков. Причинами этого могут быть значительное усиление антибактериальной активности в результате однонаправленного эффекта антибиотика и его метаболита и способность препарата целенаправленно достигать бактерицидных концентраций в очаге инфекции. Эти качества характерны для
макролидных антибиотиков
, в частности, кларитромицина, клиническая эффективность которого существенно превышает результаты лабораторного исследования чувствительности.
С учетом спектра типичных возбудителей и российских данных об их антибиотикорезистентности препаратом первого выбора при ОРС является амоксициллин
. Адекватная доза для взрослых – 3–3,5 г/сут., для детей – 80–90 мг/кг/сут.; суточную дозу делят на три приема, независимо от еды. Эффект эмпирической антибиотикотерапии должен мониторироваться, и критерием эффективности является, в первую очередь, динамика основных клинических проявлений заболевания (головной боли, выделений, заложенности носа) и общего состояния больного. При отсутствии заметного клинического эффекта по прошествии трех дней следует сменить амоксициллин на антибиотик, активный против пенициллинрезистентных пневмококков и продуцирующих b-лактамазы штаммов гемофильной палочки. В этом случае, если лечение проводится амбулаторно, перорально назначают амоксициллин–клавуланат. Маленьким детям препарат назначают в виде порошка для приготовления суспензии. Другим вариантом лечения являются цефалоспорины, в частности, цефуроксим аксетил.
Помимо амоксициллина и цефалоспоринов, в лечении ОРС могут использоваться современные макролиды, например, кларитромицин (Фромилид)
, который является препаратом выбора при непереносимости препаратов пенициллинового ряда, когда из–за возможности перекрестной аллергии нельзя назначать и цефалоспорины. Исследования последних лет показывают, что по клинической эффективности и показателю эрадикации бактериального возбудителя кларитромицин ничем не уступает защищенным пенициллинам и цефалоспоринам. Кроме того, установлено, что кларитромицин обладает иммуностимулирующими свойствами. В частности, он повышает фагоцитарную активность нейтрофилов и макрофагов, увеличивает дегрануляцию фагоцитов, бактерицидную активность лейкоцитов, а также увеличивает активность Т–киллеров.
Кларитромицин обладает местным противовоспалительным действием, которое обусловлено торможением продукции цитокинов, уменьшением гиперсекреции слизи и мокроты в дыхательных путях и вязкости мокроты. Эти свойства кларитромицина могут оказывать дополнительный эффект (помимо антибактериального) при лечении хронических инфекций ЛОР–органов, таких как отит, синусит.
В большинстве исследований отмечается хорошая переносимость кларитромицина. По сводным данным контролируемых исследований, при лечении кларитромицином нежелательные явления наблюдались у 19,6% пациентов, среди которых чаще регистрировались тошнота (3%), диарея (3%), диспепсия (2%), боли в животе (2%), головная боль (1%). В сравнительных исследованиях показано, что частота побочных явлений при применении кларитромицина была одинаковой с азитромицином, рокситромицином, амоксициллином и меньшей по сравнению с эритромицином.
Фромилид (кларитромицин) выпускается в таблетках для приема внутрь (250 и 500 мг).У взрослых при остром тонзиллофарингите кларитромицин назначают внутрь в дозе 250 мг каждые 12 ч; длительность лечения составляет 10 дней. При более тяжелом течении синусита, а также подозреваемой или документированной инфекции, вызванной H. influenzae
, дозу кларитромицина целесообразно увеличить до 500 мг каждые 12 ч. У детей кларитромицин назначают из расчета 7,5 мг/кг 2 раза в день.
Если больной госпитализирован и предпочтительным является внутримышечный путь введения, возможно назначение ингибиторозащищенного антибиотика пенициллиновой группы – ампициллин–сульбактама либо цефалоспоринов: цефотаксима или цефтриаксона. Оптимальными препаратами для внутривенного введения являются амоксициллин–клавуланат, кларитромицин и цефалоспорины.
Препаратами второго выбора, которые назначают в случае неэффективности первого курса анибиотикотерапии, в настоящее время являются фторхинолоны III–IV поколений: левофлоксацин, моксифлоксацин, спарфлоксацин. Спектр антимикробного действия этой группы препаратов максимально адаптирован к возбудителям инфекций ВДП, и их калькулируемая бактериологическая эффективность приближается к 100%, что подтверждается и исследованиями, проведенными в России. При разработке новых фторхинолонов был устранен недостаток препаратов I–II поколения – низкая эффективность в отношении S. pneumonia
, характерная, в частности, для ципрофлоксацина. Главным побочным эффектом фторхинолонов III–IV поколения является их негативное действие на растущую соединительную и хрящевую ткань, поэтому эти препараты противопоказаны детям и подросткам. В этой ситуации препаратами второй линии у больных моложе 16 лет опять становятся современные макролидные антибиотики.
Острый средний отит
. Далеко не все формы ОСО требуют назначения антибиотиков, так как при неосложненном течении этого заболевания 80–90% детей выздоравливают и без антибактериальной терапии. В этих случаях бывает достаточным назначение анальгетиков, препаратов местного действия, тепловых процедур, туалета и анемизации слизистой оболочки полости носа. При снижении температуры, уменьшении болей в ухе и симптомов интоксикации можно ограничиться одной симптоматической терапией. Больные ОСО, не получающие системную антибиотикотерапию, должны находиться под наблюдением врача для того, чтобы в случае отсутствия клинического улучшения в течение первых 24–48 часов была возможность провести повторное обследование и соответствующим образом скорректировать лечение. Считается обязательным назначение антибиотиков во всех случаях ОСО у детей менее двух лет (при отоскопически подтвержденном диагнозе!), а также пациентам с иммунодефицитными состояниями [1]. Лечение антибиотиками снижает риск развития мастоидита и внутричерепных осложнений ОСО.
Как и при ОРС, первоначальный выбор антибиотика при ОСО обычно бывает эмпирическим. Стандартный протокол антимикробной терапии, приводимый во многих клинических рекомендациях, мало отличается от того, что было сказано по поводу лечения ОРС. С учетом типичных возбудителей и российских данных об антибиотикорезистентности препаратом первого выбора при ОСО является амоксициллин. Адекватная доза для детей – 80–90 мг/кг/сут., для взрослых – 3–3,5 г/сут., разделенная на три приема, независимо от еды. При отсутствии достаточного клинического эффекта по прошествии трех дней следует сменить амоксициллин на антибиотик, активный против пневмококков с высоким уровнем пенициллинорезистентности и b-лактамазопродуцирующих штаммов гемофильной палочки: либо амоксициллин–клавуланат, либо цефалоспорины (цефуроксим аксетил внутрь или цефтриаксон в/м 1 раз в сутки в течение трех дней).
Острый тонзиллофарингит/ангина
. Антибактериальная терапия при этих заболеваниях имеет следующие цели:
- снижение выраженности симптомов болезни и ее продолжительности;
- снижение риска развития ревматической лихорадки;
- уменьшение частоты гнойных осложнений (паратонзиллит, флегмона шеи);
- профилактика распространения стрептококковой инфекции.
У пациентов с болями в горле, насморком, кашлем, гиперемией глотки и отсутствием лихорадки, как правило, имеет место вирусная инфекция, при которой нет необходимости в назначении антибиотиков. Решение вопроса о назначении системной эмпирической антибиотикотерапии при ОТФ базируется на наличии четырех основных клинических критериев болезни:
налета на миндалинах, болезненности шейных лимфоузлов, повышения температуры и отсутствии кашля. Больным с экссудативным ОТФ, лихорадкой и шейным лимфаденитом при отсутствии кашля (3–4 упомянутых признака) показано системное назначение антибиотика ввиду высокой вероятности БГСА–инфекции. При наличии 1 или 2 из упомянутых признаков антибактериальная терапия назначается только при положительном результате культурального исследования либо положительном ответе экспресс–анализа. Последний метод диагностики БГСА–инфекции основан на идентификации стрептококкового антигена в мазках из глотки путем ферментативной или кислотной экстракции антигена с последующей его агглютинацией, демонстрирующей образование комплекса «антиген–антитело».
Антибактериальная терапия при ОТФ направлена на эрадикацию основного возбудителя ангин и метатонзиллярных осложнений – БГСА. Препаратом выбора является феноксиметилпенициллин [4,12] достоинствами которого являются узкий и целенаправленный спектр действия, хорошая переносимость, минимальное воздействие на нормальную микрофлору желудочно–кишечного тракта и низкая цена. При рецидивирующих ангинах/ОФТ лечение рекомендуют начинать с амоксициллина–клавуланата или макролидных антибиотиков (азитромицина, кларитромицина, мидекамицина), которые дают, по крайней мере, не меньший процент эрадикации возбудителя. Эрадикация БГСА обычно достигается и пероральным приемом цефалоспоринов, однако более широкий спектр действия и более сильное воздействие на нормальную микрофлору кишечника ставят их в разряд альтернативных лекарственных средств. В случае клинической неэффективности первого курса эмпирической антибиотикотерапии необходимо микробиологическое исследование мазков из зева и определение чувствительности выявленного возбудителя. При выраженной клинической симптоматике и симптомах интоксикации показано парентеральное введение антибиотиков.
Известно, что БГСА вызывает не более трети ОТФ и далеко не всегда его присутствие в глотке коррелирует с тяжестью клинической картины. Лишь у 30–50% людей микробиологическая идентификация БГСА в глотке подтверждается клиническими проявлениями
. В связи с этим Американская академия педиатрических инфекций не рекомендует проведение повторных курсов антибиотикотерапии пациентам, у которых из зева высевается БГСА. Исключение составляют только дети с отягощенным семейным анамнезом по ревматизму [12]. Разнообразие форм воспалительных заболеваний глотки и их возбудителей делает обоснованным назначение препаратов с более широким, чем у пенициллина, спектром антимикробного действия – в первую очередь, современных макролидов (кларитромицин).
Особого внимания требует лечение гортанной ангины (эпиглоттита). Для предотвращения развития стеноза гортани требуется срочная госпитализация и парентеральное назначение цефалоспоринов (цефотаксим, цефтриаксон) или амоксициллина–клавуланата. При наличии явного абсцедирования надгортанника (оно подтверждается при непрямой ларингоскопии) обязательно вскрытие абсцесса гортанным ножом.
Литература:
1. Косяков С.Я., Лопатин А.С. Современные принципы лечения острого среднего, затянувшегося и рецидивирующего острого среднего отита. РМЖ 2002; 10, №20: 903–909.
2. Лопатин А.С. Острые воспалительные заболевания околоносовых пазух. Справочник поликлинического врача 2002; №1: 29–32.
3. Страчунский Л.С., Каманин Е.И., Тарасов А.А. Влияние антибиотикорезистентности на выбор антимикробных препаратов в оториноларингологии. Consilium Medicum 2002: 3, №8: 352–357.
4. Страчунский Л.С., Козлов С.Н. Современная антимикробная терапия. Руководство для врачей. СD. – 2002.
5. Тарасов А.А. Особенности клинической картины и обоснование выбора антибиотиков при остром бактериальном синусите различной этиологии. Автореф. дис. канд. мед. наук. Смоленск, 2003.
6. Antimicrobial Treatment Guidelines for Acute Bacterial Rhinosinusitis / Sinus and Allergy Partnership. Otolaryngol. Head Neck Surg 2000; 123, N1, Part 2: S1–S32.
7. Bergeron MG, Ahroheim C, Richard JE et al. Comparative efficacies of erythromycin–sulfisoxazole and cefaclor in acute otitis media: a double blind randomized trial. Pediatr Infect Dis J 1987; 6: 654–660.
8. van Buchem FL, Knottnerus JA, Schrijnemaekers VJ, Peeters MF. Primary–care–based randomised placebo–controlled trial of antibiotic treatment in acute maxillary sinusitis. Lancet 1997; 349: 683–687.
9. Dagnelie CF. Sore Throat in General Practice. A Diagnostic and Therapeutic Study. Thesis. Rotterdam, 1994.
10. Daly KA, Brown JE, Lindgren BR et al. Epidemiology of otitis media onset by six months of age. Pediatrics 1999; 103: 1158–66.
11. Healy GB. Otitis media and middle ear effusions. In: Ballenger JJ, Snow JB, Ed. Otorhinolaryngology: Head and Neck Surgery. 15th edition. Baltimore: Williams & Wilkins, 1996: 1003–1009.
12. Principles of appropriate antibiotic use for acute pharyngitis in adults: Background. Ann Emerg Med 2001; 37: 711–719.
Как правильно лечить больное горло?
Чтобы облегчить боль в горле, выбирайте Стрепсилс® Интенсив (таблетки для рассасывания медово-лимонные), которые содержат флурбипрофен – лекарственное средство, обладающее обезболивающим действием.
Препарат оказывает местное обезболивающее и противовоспалительное действие на слизистую оболочку полости рта и горла: уменьшает отек, затруднение при глотании, боль и ощущение раздражения в горле4.
Препарат не содержит антибиотиков и соответственно, не повышает риск развития резистентности. В составе препарата – натуральный мед. Стрепсилс® Интенсив (таблетки для рассасывания медово-лимонные), помогают устранить боль в горле при инфекционно-воспалительных заболеваниях полости рта и глотки вне зависимости от причины ее возникновения (будь то вирусы, бактерии или грибы).
Тантум Верде
Активное вещество этого спрея для горла – бензидамин, который относится к нестероидным противовоспалительным средствам. «Тантум Верде» снимает воспаление, местно обезболивает и является антисептиком широкого спектра действия. Применять спрей для горла «Тантум Верде» можно у взрослых и детей с 3 лет. Спрей от горла «Тантум Верде» — это удобный флакон из пластика с тонким носиком, который можно складывать. Чтобы распылить жидкость, достаточно нажать на зеленую помпу сверху – раствор распыляется струйно. У этого спрея для горла вкус сладковатый, травяной, слегка с горчинкой. Брызгать горло «Тантум Верде» можно каждые полтора-три часа (правда, дозировка отличается в зависимости от возраста). Несомненный плюс «Тантум Верде», кроме его эффективности, это экономный расход – хватает этого спрея для горла надолго. При незапущенном процессе вылечить горло полностью можно за три дня. «Тантум Верде» обычно хорошо переносится, но иногда возможны сухость в горле или жжение.
Тантум Верде
Анджелини, Италия
Тантум Верде — нестероидное противовоспалительное средство для местного применения. Действующее вещество — бензидамина гидрохлорид, производное индозолов. При локальном использовании обладает противовоспалительными и обезболивающими свойствами благодаря подавлению синтеза простагландинов и стабилизации мембран клеток. Всасывается через слизистые оболочки хорошо, накапливается в воспаленных тканях. Элиминируется пищеварительной системой (с калом) и почками (с мочой).
от 207
5.0 2 отзыва
1482
- Нравится
- Написать отзыв