Синонимы: EO
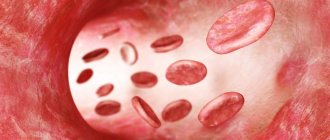
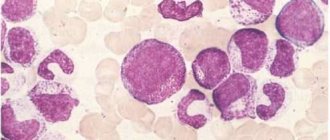
Эозинофилы состоят из двудольного ядра и трех типов эозинофильных гранул (липидные тельца, эозинофильные, мелкие и первичные). В них содержатся белковые структуры, при помощи которых обезвреживаются чужеродные клетки. Эозинофилы — это достаточно крупные клетки: их диаметр достигает 20 мкм.
Эозинофилы получили свое название благодаря тому, что при окраске по Романовскому они легко окрашиваются эозином (кислым красителем), при этом другие виды красителей на них никак не действуют. Сам эозин был изобретен в 1873 году немецким ученым Г. Каро и из-за своего ярко-розового цвета назван в честь древнегреческой богини рассвета Эос (в немецкой версии название звучит как «эосин»).
Что такое эозинофилы?
Содержание статьи
Эозинофилы – разновидность зернистых лейкоцитов или гранулоцитов. В состав их клетки входит двудольное ядро и три типа эозинофильных гранул – липидные тельца. В них содержатся белковые структуры, обезвреживающие чужеродные тела и вещества. Эозинофилы — крупные клетки диаметром до 20 мкм.
Название свое эозинофилы получили потому, что при окраске по Романовскому они легко окрашиваются красителем эозином. Это краситель был изобретен в 1873 году немецким ученым Г. Каро и из-за своего ярко-розового цвета назван в честь древнегреческой богини рассвета Эос – в немецкой версии «эосин».
Эозинофилы образуются в красном костном мозге в течение 3-4 дней. После этого попадают в кровоток, накапливаясь в слизистых кишечника, дыхательных путей и капиллярах. Там они живут и функционируют 10-14 дней. В периферической крови концентрация эозинофилов незначительна. В костном мозге и других тканях их больше примерно в 200 раз.
Роль и функции в организме
Эозинофилы как разновидность лейкоцитов ответственны за защиту от чужеродных агентов, в роли которых могут выступать микроорганизмы, химические вещества, токсины. Эозинофилы нередко называют клетками-чистильщиками, у которых есть особая задача. Они считаются наиболее чувствительными к паразитарным инфекциям и патологическим бактериям. Обычно они начинают свою работу после лимфоцитов и нейтрофилов. Их опция в этом случае — растворять остатки патогенных микроорганизмов.
Также эти клетки участвуют в реакции «антиген — антитело», за счет чего контролируют выделение гистамина, больше известного как вещество, вызывающее аллергию. Благодаря этому эозинофилы помогают снизить агрессивность ответа иммунной системы на чужеродные белки. Такие клетки крови также могут проникать через сосудистые стенки и передвигаться по тканям к очагу повреждения или воспаления.
Из числа менее известных зон ответственности эозинофилов — профилактика тромбообразования. При этом есть у них и обратная сторона. Эти клетки крови могут стать опасными, например, когда они связаны с патологическими изменениями. Такое бывает при болезни Леффлера. Это заболевание аллергического характера, когда в крови увеличивается число эозинофилов, а также в легких образуются инфильтраты, которые, впрочем, быстро исчезают.
Кровный интерес. Шесть наивных вопросов про анализы Подробнее
Показания к анализу
Общий анализ крови с подсчетом количества эозинофилов назначается большинству людей, обратившихся в поликлинику.
Спектр показаний очень широк, но в современной клинической практике исходное количество эозинофилов чаще всего используется:
- как биомаркер для оценки эффективности препаратов, назначаемых пациентам с бронхиальной астмой;
- при подтверждении предварительного диагноза;
- проверке эффективности назначенного терапевтического курса;
- оценке состояния здоровья человека при прохождении профосмотров или медкомиссий;
- в послеоперационном периоде;
- при подозрении на развитие инфекционных, онкологических и аутоиммунных заболеваний.
Часто задаваемые вопросы
h25,0,0,0,0—>
Вопрос: Можно ли избавиться от эозинопении с помощью трав? Если да, то каких?
p, blockquote21,0,0,0,0—>
Ответ: Лечить нужно не само отклонение в ОАК, а его причины. Не факт, что проблема вызвана угнетенным состоянием иммунитета. Самолечением лучше не заниматься. Есть риск пропустить опасное заболевание и даже усугубить его течение. Если человек знает наверняка, что нарушения вызваны стрессовыми ситуациями или дефицитом питательных веществ в рационе, высокими нагрузками, есть смысл прибегнуть к общеукрепляющим мерам. Нормализовать работу защитных сил помогают рациональное питание, умеренные физические нагрузки, закаливание, частые пешие прогулки. Когда очень хочется прибегнуть к фитотерапии, можно воспользоваться травами с адаптогенными свойствами. К таковым относят эхинацею пурпурную, родиолу розовую, элеутерококк и женьшень. Их экстракты можно приобрести в аптеке в готовом виде.
p, blockquote22,0,0,0,0—>
- Почему в крови эозинофилы понижены, о чем это говорит?
Вопрос: Как подготовиться к анализу, чтобы исключить ложноположительный результат? Сдаю ОАК в 3 раз, в предыдущие 2 врач засомневался, что результат правильный.
p, blockquote23,0,0,0,0—>
Ответ: За 3 дня до исследования нужно прекратить принимать лекарства и подвергать себя значительным физическим нагрузкам. Желательно отказаться от жирной пищи, умерить количество белковых продуктов в рационе. Стоит исключить алкогольную продукцию и различные «вредные» продукты (фастфуд, полуфабрикаты, чипсы, сухарики). Последний прием пищи должен состояться за 8‒12 часов до забора биоматериала. Запрещено употреблять любую еду или напитки, кроме чистой воды (утренний кофе также придется пропустить). Лучше не курить непосредственно в день анализа. Стоит ограничить себя от стрессов, перегрева или перемерзания по дороге в медучреждение.
p, blockquote24,0,0,1,0—>
Вопрос: Можно ли сдавать ОАК во время месячных? Как они могут повлиять на показатели?
p, blockquote25,0,0,0,0—>
Ответ: Сдавать анализ во время менструации без особой необходимости не стоит. В этот период любой из показателей может выйти за пределы нормы, что не связано с заболеванием. Врачи рекомендуют воздержаться от любых лабораторных тестов за 3 дня до, непосредственно во время кровотечения и 2‒3 дня после. Однако относительно эозинофилов есть другая версия. Считается, что значение этих кровяных телец может снижать прогестерон. Если сомнения вызывают именно эозинофилы, стоит сдать анализ после месячных, однако до овуляции (7‒13 день цикла).
p, blockquote26,0,0,0,0—>
Вопрос: Можно ли понизить уровень эозинофилов препаратами, использующимися при аллергии до критических значений?
- Почему в крови эозинофилы повышены, о чем это говорит?
p, blockquote27,0,0,0,0—>
Ответ: Антигистаминные средства мало влияют на картину крови, если использовать их правильно и соблюдать рекомендованные дозы. Важно соблюдать продолжительность курса, вовремя делать перерывы или менять медикаменты. Существенные отклонения в картине крови способны вызвать гормональные средства, поэтому с ними нужно соблюдать осторожность и применять только по назначению врача.
p, blockquote28,0,0,0,0—>
Вопрос: Помогут ли растительные средства из группы иммуностимуляторов (например, Иммунал или Иммупрет) повысить уровень эозинофилов?
p, blockquote29,0,0,0,0—>
Ответ: Помогут, если отклонение вызвано перенесенным инфекционным заболеванием, истощением организма, стрессами. Если природа нарушений заключается в гнойных процессах, злокачественных или наследственных патологиях, стимуляторы иммунитета не помогут, а при заболеваниях костного мозга или желез внутренней секреции могут даже навредить.
p, blockquote30,0,0,0,0—>
Нормы эозинофилов в крови
| Возраст | Нормальный уровень эозинофилов в крови |
| Дети младше 5 лет | 0,5 – 7% |
| Дети 5 – 14 лет | 1 – 5% |
| Взрослые | 0,5 – 5% |
У женщин в первые дни менструации уровень эозинофилов немного превышает норму, а после овуляции их количество бывает немного ниже нормы.
Повышенный уровень эозинофилов в крови называется эозинофилией.
Последствия отклонения от нормы
Изменение нормального уровня эозинофилов в крови не является критерием, по которому можно составить представление о возможных патологических изменениях в организме. Проще говоря, сам по себе уровень эозинофилов в крови мало что значит — нужно обращать внимание на болезнь, которая вызвала его изменение. Поэтому последствия могут быть самыми разнообразными — от совершенно незначительных (как в случае с физической нагрузкой) до смертельно опасных (например, при онкологии).
Сама по себе эозинофилия в редких случаях может привести к повреждению тканей, в которых наблюдается наибольшее скопление эозинофилов. Механизм подобных повреждений на сегодняшний день до конца не изучен, однако установлено, что наиболее сильное повреждающее действие эозинофилы проявляют при таких состояниях, как эозинофильный фибропластический эндокардит и идиопатический гиперэозинофильный синдром. Характер повреждений напрямую зависит от продолжительности эозинофилии и выраженности эозинофильной инфильтрации тканей.
Стадии эозинофилии
| Стадия | Уровень стадии | Количество эозинофилов в крови от общего числа лейкоцитов |
| Первая | Легкая | не более 10% |
| Вторая | Средняя | 10% – 15% |
| Третья | Тяжелая | свыше 15% |
Анализ крови на эозинофилы
Чтобы определить уровень эозинофилов, используется общий анализ крови, всем нам хорошо знакомый еще с детства. Эозинофилы сами по себе не дают точного представления о характере патологических изменений в организме, однако в комплексе с другими значениями лейкоцитарной формулы позволяют специалисту судить о характере патологии. В бланке анализа эозинофилы обозначаются как ЕО. Их содержание обозначается в процентах от общего числа лейкоцитов. Используется также формула для подсчета абсолютного числа эозинофилов в периферической крови и выглядит она следующим образом: количество лейкоцитов * 10 в 9 степени. Для общего анализа кровь чаще всего берут из пальца, но венозная кровь тоже подходит.
Рисунок 1. Причины эозинофилии (повышенного количества эозинофилов в крови). Изображение: kavusta / Depositphotos
Причины повышенного содержания эозинофилов в крови
Повышение эозинофилов или эозинофилия наблюдается при следующих заболеваниях и состояниях:
- заболевания и состояния, сопровождающиеся аллергическими процессами в организме – вздутие живота, бронхиальная астма, крапивница, отек Квинке, сывороточная болезнь, лекарственная болезнь и др.;
- паразитарные заболевания – аскаридоз, лямблиоз, токсокароз, трихинеллез, описторхоз, эхинококкоз, малярия и др.;
- сопутствующие тканевые заболевания и системные васкулиты – ревматоидный артрит, мезотелиальный периартериит, склеродермия, системная красная волчанка и др.;
- дерматологические заболевания – дерматиты, экземы, крокусы кожи, пузырчатка и др.;
- некоторые инфекционные заболевания – туберкулез, скарлатина, сифилис;
- заболевания крови, сопровождающиеся распространением одной или нескольких кроветворных бактерий – хронический миелолейкоз, эритремия, лимфогранулематоз;
- прием сульфаниламидов, антибиотиков и адренокортикотропных гормонов.
Длительная (более шести месяцев) высокая эозинофилия неясной этиологии называется гиперэозинофильным синдромом. Уровень эозинофилов в крови превышает 15%. Эта патология очень опасна, она вызывает поражение внутренних органов – сердца, почек, костного мозга, легких и т. д.
Если в крови повышено содержание моноцитов и эозинофилов, это может указывать на инфекционный процесс в организме, заболевание крови или раннюю стадию рака.
Иногда количество моноцитов увеличивается после выздоровления от различных заболеваний.
Задачи эозинофилов
Главная задача деятельности эозинофилов – ликвидация чужеродных вредоносных агентов. Их уничтожение происходит на внеклеточном уровне, в их возможности входит устранение также довольно крупных организмов. Воздействие начинается при выделении содержимого внутриклеточных гранул. По сравнению с нейтрофилами способность к фагоцитозу у рассматриваемых нами агентов меньше, но все же она присутствует. Это не является их основной задачей, но они могут уничтожать и поглощать микробы.
Перечислим основные функции эозинофильных гранулоцитов:
- Воздействуют токсически на гельминтов.
- Устраняют действие биологически активных веществ, вызвавших аллергию.
- Помогают устранить последствия деятельности биоактивных веществ, которые были произведены тучными клетками и базофилами. Последние являются главными возбудителями аллергической реакции. Они также влияют на развитие тяжелых форм болезни – отека Квинке и анафилактического шока.
- Развивают реакцию высокой чувствительности.
- Пробуждают активность к убиванию бактерий.
- Ликвидируют инородные клетки, поглощая их.
Эозинофилы сражаются с аллергенами, приводя к стабилизации состояния ребенка или взрослого
Как снизить количество эозинофилов в крови?
В первую очередь важно устранить причину возникновения эозинофилии, то есть заболевание, вызвавшее изменение лейкоцитарной формулы.
Возможные варианты лечения:
- противоаллергическая терапия – прием антигистаминных препаратов: хлоропирамин, цетиризин, левоцетиризин, деслоратадин и лоратадин и др.;
- антибактериальная терапия — прием антибиотиков: амоксициллин, цефтриаксон, азитромицин, эритромицин и т.д.;
- противовоспалительная терапия – прием препаратов при воспалительных процессах, например глюкокортикостероидов – преднизолон;
- химиотерапия – для устранения злокачественных новообразований;
- гормональная терапия;
- антигельминтная терапия – прием альбендазола, левамизола, бефения гидроксинафтоата, пиперазина, тетрахлорэтилена, мебендазола. Выбор медикамента зависит от вида паразитов и стадии инвазии.
Дополнительно можно предпринять следующие меры:
- Нормализовать образ жизни. Важно избегать частого приема алкоголя и отказаться от сигарет.
- Избегать хронической интоксикации. У людей, работающих на вредных производствах или живущих в экологически неблагополучных регионах, в результате постоянной химической интоксикации количество эозинофилов в крови растет.
- Придерживаться здорового питания. Не следует злоупотреблять острыми, копчеными, консервированными и жирными продуктами. Чтобы повысить уровень эозинофилов, следует ограничить количество мяса, птицы и рыбы в рационе, употреблять преимущественно их нежирные сорта. В меню должны входить йогурт, сыры, овощи, фрукты, бобы, отрубной и цельнозерновой хлеб.
Этиология
Повышение эозинофилов у ребенка патологические причины имеет следующие:
- аллергические реакции;
- глистные инвазии;
- нехватка магния;
- иммунодефицитные состояния;
- системные заболевания;
- инфекционные и вирусные заболевания;
- кожные болезни хронического характера;
- нарушение функционирования щитовидной железы;
- заболевания верхних дыхательных путей, чаще всего пневмония;
- обширные термические ожоги;
- отравление токсическими веществами;
- врожденные заболевания сердечно-сосудистой системы;
- повышение тонуса блуждающего нерва;
- полицитемия;
- туберкулез;
- васкулит;
- инфекционный мононуклеоз;
- доброкачественные опухоли;
- онкологические процессы.
Кроме того, повышены эозинофилы в крови у малыша могут быть при длительном приеме препаратов такого типа, как сульфаниламиды, нитрофураны, гормоны и антибиотики.
Причины того, что эозинофилы выше допустимого количества, можно установить только путем проведения диагностических мероприятий, так как специфической клинической картины этот процесс не имеет.
Как повысить количество эозинофилов в крови?
Снижение уровня эозинофилов в крови — признак ослабления иммунитета. Как и в случае с эозинофилией, следует выявить первичную патологию и устранить ее, а также скорректировать образ жизни:
- свести к минимуму вредные привычки;
- обеспечить адекватный уровень физической активности;
- позаботиться о нормальном режиме дня;
- больше употреблять продуктов, содержащих витамины В12, С, D – мясо, рыба, творог, шиповник, смородина, чеснок, либо использовать аптечные поливитамины.
- желательно исключить продукты с высоким аллергенным потенциалом: молоко, сою, пшеницу, яйца, морепродукты, арахис.
Изменение уровня содержания эозинофилов в крови может быть вызвано как физиологическими причинами – физическая нагрузка, стрессы, переедание, так и различными заболеваниями. Иногда одно и то же состояние, например, аллергия или инфекционный процесс может вызывать как снижение, так и повышение количества эозинофилов в крови и других биологических жидкостях.
IgE, тучные клетки, базофилы и эозинофилы
IgE, тучные клетки, базофилы и эозинофилы являются важными элементами аллергического воспаления. Аллерген-специфический IgE, синтезируемый в ответ на аллергены в окружающей среде и у восприимчивых людей, становится фиксированным к высокоаффинным рецепторам на клеточных мембранах, особенно тучных клеток и базофилов. Если эти связанные с рецептором молекулы IgE агрегируются при повторном воздействии специфического аллергена, эти тучные клетки и базофилы продуцируют медиаторы, которые приводят к аллергическому ответу. Основным среди клеток, привлеченных к сайтам высвобождения медиатора, является эозинофилы.
IgE
Реагиновое антитело IgE (иммуноглобулин Е) имеет приблизительную молекулярную массу 190 кДа, не обладает трансплацентарным переносом и, в отличие от других иммуноглобулинов, не активирует комплемент по классическому пути. IgE является термолабильным и не будет сенсибилизироваться после того, как его нагревают до 56 ° C в течение нескольких часов. IgE в основном известен своей способностью связываться с высокой аффинностью с его специфическим рецептором (R) FcϵRI, обнаруженным в его полной форме (α 2 ) на мембранах тучных клеток и базофилов. Концентрация IgE в сыворотке крови является самой низкой из пяти изотипов человеческого иммуноглобулина (0-0,0001 г / л, что составляет 0,004% от общего сывороточного иммуноглобулина) и сильно зависит от возраста. Концентрация IgE в сыворотке является низкой в сыворотке пуповины (<2 кЕд / л, <4,8 мг / л) и увеличивается с возрастом до достижения человеком 10–15 лет. . У людей с аллергической предрасположенностью наблюдается более ранний и более крутой подъем. Уровень общего сывороточного IgE снижается со второго по восьмое десятилетия жизни. По оценкам, специалистов около 50% общего IgE организма находится во внутри сосудов. IgE имеет период полураспада от 1 до 5 дней в периферической крови.
Первоначально В-клетки продуцируют антитела IgM, но после соответствующих стимулов изменяют изотип продуцируемого антитела, сохраняя антигенную специфичность посредством совместного использования одной и той же вариабельной (VDJ) области. Это «переключение изотипа» является эффективным в том смысле, что оно позволяет одному клону B-клеток продуцировать антитела с той же специфичностью, но различными эффекторными функциями, находящимися в константной части тяжелой цепи. Этот процесс состоит из сплайсинга и воссоединения геномной ДНК для сопоставления элементов VDJ с экзонами С-области, которые кодируют, в случае IgE, ϵ-цепь, определяющую изотип IgE. Для синтеза IgE требуются два типа сигналов. Сигнал 1 обеспечивается цитокинами интерлейкина (IL) -4 и IL-13, которые активируют транскрипцию в определенном локусе иммуноглобулина. Второй сигнал обеспечивается путем лигирования CD40 на В-клетках, что, в свою очередь, активирует рекомбинацию переключателя ДНК. Оба сигнала представлены В-клетками Т-клетками.
Процесс начинается, когда аллерген связывается с аллерген-специфическим IgM на В-клетке, которая затем обрабатывает аллерген. Когда В-клетка затем представляет фрагменты этого аллергена в контексте молекул МНС класса II в комплексе рецептор-CD3 Т-клетки на клетке Т H 2, Т-клетка быстро экспрессирует лиганд IL-4 и CD40 (CD40L, CD154) , CD40L включает CD40, экспрессируемый в В-клетке. Это взаимодействие приводит к экспрессии B7 на B-клетках, которая связывается с CD28 на T-клетке, что приводит к активизации IL-4, происходящего из T-клеток.
Сообщалось, что тучные клетки и базофилы человека секретируют IL-4, IL-13 или оба, а также экспрессируют некоторые CD40L. Таким образом, эти наблюдения предполагают, что эти клетки могут взаимодействовать с В-клетками, чтобы обеспечить сигналы для синтеза или амплификации IgE. Поскольку производство IL-4 или IL-13 базофилов и тучных клеток зависит от агрегации Fc-RI через антиген-специфический IgE, этот механизм более привлекателен для амплификации синтеза IgE. Этот механизм, по-видимому, не является аллерген-специфичным, а скорее вызывает поликлональный ответ. Эта гипотеза согласуется с наблюдением, что ответ IgE в гипер-IgE-состояниях является поликлональным.
Существует два различных рецептора IgE: низкоаффинный рецептор IgE (FcϵRII; CD23), присутствующий в В-клетках, и высокоаффинный рецептор IgE (FcϵRI). Fc-RI на тучных клетках и базофилах представляет собой тетрамер (α 2 ), тогда как он экспрессируется в тримерной форме ( 2 ) на антигенпрезентирующих клетках, таких как моноциты, клетки Лангерганса и дендритные клетки периферической крови. Плотность экспрессии человеческого Fc-RI базофила человека коррелирует с уровнями IgE в сывороткепоскольку связывание IgE с Fc-RI стабилизирует рецептор на клеточной поверхности. Взаимодействия Fc-RI-IgE также могут способствовать выживанию тучных клеток.
На общий уровень IgE влияют возраст, генетическая предрасположенность, этническая принадлежность, иммунный статус, время года и некоторые заболевания. Повышенные уровни IgE обнаруживаются при паразитарных заболеваниях, таких как шистосомоз и анкилостома; инфекции, такие как аллергический бронхолегочный аспергиллез и вирус мононуклеоза Эпштейна-Барра; кожные заболевания, такие как буллезный пемфигоид; опухолевые заболевания, такие как болезнь Ходжкина и миелома IgE; иммунодефицитные заболевания, такие как синдром Вискотта-Олдрича, синдром гипериммуноглобулинемии E, гипоплазия тимуса (синдром Ди Джорджа) и клеточный иммунодефицит с иммуноглобулинами (синдром Незелофа); и ряд других заболеваний, таких как нефротический синдром, муковисцидоз, болезнь Кавасаки и узловой инфантильный полиартериит. В совокупности такая информация диктует, что измерение общего уровня IgE в сыворотке имеет ограниченную ценность в качестве скрининг-теста на аллергическое заболевание.
Базофилы
Базофилы представляют собой гранулоциты, которые, как полагают, представляют отдельное происхождение от тучных клеток, несмотря на тот факт, что два типа клеток имеют много общих черт, таких как экспрессия высокоаффинного рецептора IgE (FcϵRI), метахроматическое окрашивание, экспрессия цитокинов T H 2 и высвобождение гистамина. Базофилы составляют менее 1% лейкоцитов периферической крови, что делает их одним из наименее распространенных клеточных линий в периферической крови. Количество базофилов в периферической крови незначительно повышено (приблизительно в 2 раза) при аллергической астме. Базофилы имеют сегментированное ядро с высококонденсированным хроматином и обычно идентифицируются по метахроматическому окрашиванию основными красителями, такими как толуидиновый синий. Недавно были разработаны два моно-специфических антитела к базофильным гранулам, BB-1 и 2D7, которые позволяют однозначно идентифицировать базофилы в тканях и значительно расширяют наше понимание роли базофилов при аллергических заболеваниях и астме. Базофилы экспрессируют различные рецепторы цитокинов (IL-3R, IL-5R, GM-CSFR), рецепторы хемокинов (CCR2, CCR3), рецепторы комплемента (CD11b, CD11c, CD35, CD88), рецепторы простагландина (CRTH2) и иммуноглобулин Fc-рецепторы (FcϵRI, FcγRII).
Базофилы развиваются из плюрипотентных стволовых клеток CD34 + , дифференцируются и созревают в костном мозге, а затем циркулируют по периферии. IL-3 является доминирующим цитокином, управляющим дифференцировкой базофилов и достаточным для дифференцировки стволовых клеток в базофилы. Общее мнение заключается в том, что базофилы представляют собой отдельную клеточную линию от тучных клеток и отличаются от общего предшественника базофил-эозинофилов; Это убеждение подтверждается происхождением смешанных колоний базофилов и эозинофилов из отдельных клеток-предшественников..
Как и в случае с тучными клетками, базофилы экспрессируют полный и функциональный рецептор Fc-RI (αβ 2 ), поперечное сшивание которого приводит к активации базофилов, экзоцитозу гранул. и освобождение посредника. C3a и C5a также могут активировать базофилы через рецепторы комплемента C3aR и C5aR соответственно. Активация через любой из этих рецепторов приводит к высвобождению гистамина, синтезу эйкозаноидов и экспрессии генов IL-4 и IL-13 . Примирование является способностью молекул, которые не могут максимально активировать базофилы самостоятельно, чтобы усилить Fc-RI-опосредованную активацию. Медиаторы с такой праймирующей активностью включают CC-хемокины (эотаксины, белок 3 хемоаттрактанта моноцитов, белок 4 хемоаттрактанта моноцитов, RANTES), N-формил-метионил-лейцил-фенилаланин, IL-3, IL-5, GM-CSF и высвобождающий гистамин. фактор. Присутствие таких медиаторов в местах воздействия аллергена может снизить порог развития аллергического воспаления.
Базофилы продуцируют много медиаторов, сходных с тучными клетками, таких как гистамин, лейкотриены, IL-4 и IL-13. И наоборот, медиаторы тучных клеток PGD 2 и IL-5 не продуцируются базофилами. Из вновь синтезированных эйкозаноидных медиаторов базофилы в основном генерируют LTC 4 . В дополнение к гистамину гранулы базофилов содержат ряд других предварительно образованных медиаторов, таких как сульфат хондроитина, основной основной белок и кристаллический белок Шарко-Лейдена. Как правило, базофилы содержат только небольшие количества триптазы; однако, по-видимому, существует много различий между людьми в отношении экспрессии триптазы базофилов. В дополнение к их роли в непосредственной гиперчувствительности, базофилы могут способствовать аллергическому воспалению с помощью ряда неклассических механизмов. Базофильная экспрессия IL-4 и CD40L индуцирует переключение B-клеток IgE in vitro и может содержать альтернативный механизм, стимулирующий переключение класса IgE. Альтернативно, быстрая и обильная экспрессия IL-4 базофилами была предложена в качестве источника IL-4, который может дополнительно стимулировать дифференцировку клеток T H 2.
Физиологическая роль базофилов не известна, хотя, по-видимому, как и другие лейкоциты, они выполняют роль в защите хозяина. Долгое время считалось, что базофилы играют роль в отторжении клещей и являются заметным компонентом воспалительного ответа на многих паразитов. Эта предполагаемая роль в защите хозяина от паразита подтверждается недавним открытием функциональных гомологов паразита гистамин-рилизинг-фактора в трансляционно-контролируемом семействе опухолевых белков. Хотя базофилы обладают многими характеристиками, которые предполагают, что они способствуют аллергическому воспалению, точная роль базофилов в патогенезе астмы неясна. После заражения аллергеном базофилы являются преобладающим типом клеток, экспрессирующих IL-4, в астматических дыхательных путях человека, мононуклеарных клетках периферической крови.
Эозинофилы
Эозинофилы представляют собой гранулоциты, которые были впервые описаны для окрашивания кислотными анилиновыми красителями, такими как эозин. Хотя эти клетки редко встречаются в периферической крови здоровых людей, эозинофилия в крови и тканях является отличительным признаком инфекции гельминтами, аллергии и астмы. Из-за большого количества доказательств, подтверждающих критическую роль в патогенезе астмы, эозинофил превратился в главную терапевтическую мишень для иммунологической терапии астмы.
Эозинофилы обычно имеют двухъядерное ядро с высококонденсированным хроматином и цитоплазмой, содержащим два основных типа гранул: специфические и первичные гранулы. Конкретные гранулы имеют характерный ультраструктурный вид, состоящий из электронно-плотного кристаллоидного ядра. Эти гранулы содержат много катионных белков, которые придают эозинофилам свои уникальные свойства окрашивания. Первичные гранулы подобны тем, которые обнаружены в других линиях гранулоцитов, и обнаруживаются на ранних стадиях развития эозинофилов. Эозинофилы также содержат липидные тела, которые играют роль в генерации эйкозаноидных медиаторов.
Поскольку нет специфического для эозинофилов маркера клеточной поверхности, их связывание с эозино-подобными красителями остается наиболее распространенным методом обнаружения. Разработка моноклональных антител к различным белкам гранул эозинофилов стала дополнительным средством иммунохимической идентификации этих клеток. Эозинофилы экспрессируют широкий спектр молекул клеточной поверхности, включая цитокиновые рецепторы (IL-3R, IL-5R и GM-CSFR), хемокиновые рецепторы (CCR1 и CCR3), FcγRII (CD32), FcαRI (секреторный IgA) рецепторы комплемента (C3aR, C5aR, CD88 и CD35), молекулы адгезии (очень поздний антиген [VLA] -4 и α 4 β 7 интегрин), CD9 и CD69. CD69 является маркером активации эозинофилов и активируется на эозинофилах, выделенных из участков аллергического воспаления. Эозинофильная экспрессия FcϵRI минимальна и имеет неясное функциональное значение.
Эозинофилы развиваются и созревают в костном мозге из клеток-предшественников CD34 + и высвобождаются в периферическую кровь в виде зрелых клеток. IL-5, основной эозинофильный активный цитокин, оказывает глубокое положительное влияние на дифференцировку и пролиферацию предшественников эозинофилов в костном мозге. Таким образом, IL-5 продуцируется периферически в местах аллергического воспаления, или инфекция гельминтами действует дистально на костный мозг. Кроме того, аллергенная стимуляция или экспериментальное введение эотаксина вызывает высвобождение в костном мозге зрелых эозинофилов, а также предшественников эозинофилов.
После высвобождения из костного мозга эозинофилы циркулируют в периферической крови, а затем поступают в ткани с периодом полувыведения из периферической крови от 8 до 18 часов. Хотя эозинофилы наиболее известны как лейкоциты периферической крови, подавляющее большинство эозинофилов находится в кишечнике и легких. Эозинофилы также являются основным источником цистеинил лейкотриена LTC 4 и его активных метаболитов LTD 4 и LTE 4 . Эозинофилы, наряду с тучными клетками и базофилами, являются основными LTC 4 -синтез-продуцирующими клетками в слизистой оболочке бронхиальной астмы. Эозинофилы способны продуцировать ряд цитокинов, включая IL-1, трансформирующий фактор роста β, IL-3, IL-4, IL-5, IL-8 и TNF-α. Однако эозинофилы обычно продуцируют меньшее количество цитокинов, чем другие воспалительные клетки, такие как Т-клетки. Как таковой, относительный вклад выработки эозинофильных цитокинов в генерацию аллергического воспаления еще предстоит определить.
Количество эозинофилов в периферической крови увеличивается при аллергических заболеваниях, астме и гельминтозах, а тканевая эозинофилия часто обнаруживается в местах воспаления, связанных с этими заболеваниями. Несмотря на их активность in vitro против паразитов, исследования in vivo на мышах, нокаутированных по гену IL-5, в целом не подтверждают существенную роль эозинофилов в устранении паразитарных инфекций. При аллергических заболеваниях и астме эозинофилы играют провоспалительную роль, в которой, как полагают, эозинофильные медиаторы, такие как МВР, вызывают воспаление слизистой оболочки и, как следствие, гиперчувствительность бронхов. Кортикостероиды сильно снижают количество эозинофилов в периферической крови и тканях, что еще более подтверждает центральную роль эозинофилов в патогенезе астмы. Поскольку эозинофилы считаются конечной эффекторной клеткой астмы, ряд исследовательских методов лечения был нацелен на эозинофилы. Недавно исследование фазы II анти-IL-5 при астме у человека не продемонстрировало улучшения ни в отношении воздушного потока, ни в поздних фазах аллергических реакций, несмотря на снижение эозинофилов периферической крови на 90%. Последующее исследование анти-IL-5 продемонстрировало аналогичное снижение уровня эозинофилов в периферической крови на 90%, но снижение эозинофилов слизистой бронхов только на 55%. Эти данные демонстрируют, что одного анти-IL-5 может быть недостаточно для устранения легочной эозинофилии и что необходимо изучить дополнительные стратегии против эозинофилов, чтобы определить их терапевтический потенциал при лечении астмы.