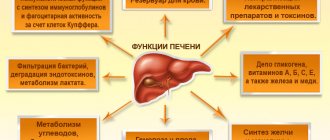
Лечебные свойства и воздействие на организм
Расторопша содержит ряд активных компонентов, которые обуславливают ее целебное действие:
- силимарин – комбинация из 4 флавонолигнанов;
- флавоноиды;
- алкалоиды;
- сапонины;
- витамины А, Д, Е, К;
- смолы;
- дубильные вещества;
- тирамин;
- микроэлементы (калий, кальций, бор, магний, цинк, селен, марганец).
— 42%
Natrol, Молочный чертополох, 525 мг, 60 капсул
★★★★★
806 руб. 466 руб.
Подробнее
Остановимся на главных:
- Силимарин. Официально признан лекарственным препаратом с мощным гепатопротекторным действием. Вещество преобразует свободные радикалы в неактивную форму, тем самым защищает клеточные мембраны от повреждения, усиливает отток желчи, а также стимулирует регенерацию клеток печени. За счет нормализации структуры гепатоцитов и замедления прогрессирования фиброза улучшаются все функции органа, особенно, дезинтоксикационная и белковосинтезирующая. Силимарин также предупреждает размножение вируса гепатита C, снижает вероятность развития гепатоцеллюлярного рака.
- Жирорастворимые витамины A и Е. Защищают клетки от повреждений, предупреждая развитие онкологических заболеваний. Они также улучшают состояние кожи, волос, ногтей, положительно влияют на зрительный аппарат, нервную систему.
- Холекальциферол. Способствует усвоению кальция, укрепляет иммунитет.
- Витамин K. Нормализует свертывающую способность крови.
- Микроэлементы. Являются участниками важнейших биохимических реакций в организме: регулируют синтез некоторых гормонов, передачу нервных импульсов, активность иммунных клеток, репродуктивную функцию, производят противовоспалительный эффект.
Больше подробностей о лечебных свойствах расторопши можно узнать из видео:
Расторопша — лечебные свойства и противопоказания
Флавоноиды расторопши пятнистой в лечении заболеваний печени
П
репараты расторопши пятнистой затруднительно классифицировать в какой–либо конкретной группе лекарственных средств.
Упоминая о расторопше, нередко говорят, что она обладает «гепатопротекторными» свойствами.
Однако правомерность выделения отдельного фармакологического класса «гепатопротекторов» вызывает сомнения. Само понятие «гепатопротекторы» по определению является нестрогим и достаточно произвольно трактуется разными специалистами. В наиболее распространенном понимании это класс препаратов, которые независимо от механизма действия повышают функциональную способность клеток печени к синтезу, дезинтоксикации и выведению различных биологических продуктов, поддерживают устойчивость гепатоцитов к различным патогенным воздействиям.
Общий характер названия «гепатопротекторы», по–видимому, отражает недостаточную глубину наших знаний о патогенезе болезней печени, о механизмах повреждения, регенерации, фиброза и злокачественной трансформации гепатоцитов.
Во многих справочниках и руководствах к классу «гепатопротекторов» относят активаторы синтеза белков (бемитил), витамины, предшественники нуклеиновых кислот, препараты, стимулирующие реакции детоксикации в печени (аспарагин, глутамин, цитруллин), метаболиты митохондриального дыхания (яблочная кислота, сукцинат натрия, цитохром, карнитин, аминалон), препараты, снижающие проапоптотическое воздействие желчных кислот (урсодезоксихолевая кислота), донаторы сульфгидрильных групп (S–аденозил–L–метионин), препараты эссенциальных фосфолипидов, липоевую кислоту.
В то же время уместно напомнить, что ряд препаратов этого типа (преимущественно растительного происхождения) исторически прочно заняли свое место в терапии внутренних болезней.
Среди «гепатопротекторов» весьма заметную долю занимают препараты, содержащие естественные или полусинтетические флавоноиды расторопши пятнистой (Silybum marianum)
. Главным действующим компонентом в них является силимарин.
Силимарин представляет собой смесь трех основных изомерных соединений – силикристина, силидианина и силибинина. Последний превалирует по количественному содержанию и обладает наиболее высокой биологической активностью.
Действительно ли препараты расторопши пятнистой способны оказывать лечебное воздействие при заболеваниях печени?
Положительное воздействие силимарина при болезнях печени традиционно связывают с выраженным антиоксидантным потенциалом, а также так называемым «мембраностабилизирующим» действием.
Роль окислительного стресса в патогенезе заболеваний печени интенсивно изучается в последние годы. Выработка активных форм кислорода (перекисей, супероксид–анион–радикалов) – обычное явление в процессе клеточного дыхания, однако содержание их чрезмерно возрастает в условиях алкогольной интоксикации, при повреждении печени и воспалении, дефиците антиоксидантов, гипоксии, воздействии некоторых лекарств. Повышенная выработка свободных радикалов сопровождается повреждением клеточных органелл и макромолекул (ДНК, белков и липидов, антиоксидантных систем). При окислительном стрессе продукты перекисного окисления играют важную роль в фиброгенезе, активируя звездчатые клетки печени и повышая продукцию внеклеточного матрикса.
К внутриклеточным «защитным молекулам», препятствующим развитию реакций перекисного окисления, относятся ферменты супероксиддисмутаза, каталазы, глутатионпероксидаза, металлосвязывающие белки, молекулы – «уборщики свободных радикалов» (глутатион, убихиноны, мочевая кислота, аскорбиновая кислота и токоферол, липоевая кислота, селен, рибофлавин, цинк, каротиноиды). Обмен различных антиоксидантов тесно взаимосвязан.
В условиях воспаления печени источником выработки активных форм кислорода служат клетки воспалительного инфильтрата.
Кроме того, одним из универсальных механизмов повреждения клеток при заболеваниях печени служит нарушение функции митохондрий.
При воздействии на клетку некоторых веществ, таких как фактор некроза опухоли–a (TNFa), этанол, а также в условиях избыточного накопления железа и меди происходит нарушение процесса окислительного фосфорилирования в митохондриях, что сопровождается развитием энергетического дефицита и гибелью клеток.
Дезорганизация мембран митохондрий в условиях перекисного окисления может сопровождаться «утечкой» цитохрома С в цитоплазму, активацией процесса программированной гибели клеток.
Несмотря на то, что современные научные данные, касающиеся значения свободнорадикальных процессов в патогенезе заболеваний печени, нередко оказываются противоречивыми, все же в определенных клинических ситуациях отрицательная патогенетическая роль нарушения функции митохондрий, клеточного дыхания и развития перекисного окисления липидов не вызывает сомнений. Это прежде всего алкогольная болезнь печени, неалкогольный стеатогепатит, внутрипеченочный холестаз беременных, некоторые случаи токсического поражения печени.
Антиоксидантный эффект силимарина обусловлен его взаимодействием со свободными радикалами в печени и превращением их в менее агрессивные соединения. Тем самым прерывается процесс перекисного окисления липидов и не происходит дальнейшего разрушения клеточных структур. Способность взаимодействия с активными формами кислорода обусловлена наличием фенольной структуры в молекуле силибинина.
Антиоксидантное действие силимарина и торможение реакций перекисного окисления отчетливо продемонстрировано in vitro. Флавоноиды расторопши проявляют в 10 раз более высокую антиоксидантную активность, чем токоферол.
Благодаря наличию антиоксидантных свойств препараты расторопши проявляют противовоспалительную активность
. Лечебное действие силибинина продемонстрировано в моделях токсического поражения печени у крыс, вызванного введением тетрахлорметана. В остром эксперименте при разовом введении тетрахлорметана назначение флавоноидов расторопши сопровождалось отчетливым снижением степени выраженности цитолиза и холестаза. В хроническом эксперименте с тетрахлорметаном введение силибинина также способствовало значительному снижению выраженности цитолиза и холестаза.
Отнюдь не случайно рабочим вредных химических производств рекомендуется профилактический прием силимарина 1 раз в день.
Наиболее разительное лечебное действие оказывают флавоноиды расторопши при алкогольной болезни печени.
Венгерский исследователь Muzes G. и соавт. в двойном слепом исследовании показали, что силимарин оказывает положительный клинический эффект при алкогольной болезни печени
, по–видимому, обусловленный антиоксидантным действием данного вещества. Назначение силимарина в суточной дозе 420 мг в сутки в течение 6 мес. сопровождалось биохимическими изменениями в организме, которые косвенно свидетельствуют о нарастании антиоксидантного потенциала клеток и сыворотки крови. Так, отмечалось значительное возрастание активности супероксиддисмутазы в энтероцитах и лимфоцитах (при исходно сниженных значениях), повышение активности глутатионпероксидазы и содержания веществ с сульфгидрильными группами в сыворотке. Одновременно имело место существенно снижение концентрации веществ, проявляющих свойства окислителей (малондиальдегида и др.), в сыворотке крови.
При вирусном гепатите С, по мнению Berkson B.M., назначение «тройной антиоксидантной схемы» (тиоктовая кислота, силимарин, селен) представляет собой достаточно дешевый и безопасный метод патогенетического лечения вирусного гепатита С и торможения прогрессирования поражения печени до стадии цирроза. Антиоксидантный эффект терапии способствует подавлению воспалительно–некротической реакции в печени, торможению развития фиброза и снижает риск злокачественной трансформации гепатоцитов.
Интересны также данные об иммуномодулирующих свойствах флавоноидов расторопши при алкогольной болезни печени. Длительное их назначение (около 6 мес.) способствует снижению активности цитотоксического звена (содержания цитотоксических лимфоцитов CD8+), снижению продукции g-глобулинов и повышению скорости бласттрансформации лимфоцитов.
Ряд авторов считает целесообразным назначение силимарина пациентам, страдающим гепатитом С, при необходимости приема препаратов, способных снижать антиоксидантный потенциал гепатоцитов (например, ацетаминофена).
При внутрипеченочном холестазе беременных применение силимарина позволяет добиться уменьшения выраженности кожного зуда.
Силимарин «стабилизирует» мембраны гепатоцитов, снижая восприимчивость клеток к некоторым патогенным воздействиям.
Блокада фосфодиэстеразы под действием флавоноидов расторопши способствует замедлению распада циклического аденозинмонофосфата (цАМФ), и, как следствие, понижению содержания кальция внутри клеток, угнетению кальций–зависимого процесса активации фосфолипаз.
Силибинин обладает способностью блокировать соответствующие участки связывания на клеточной мембране и транспортные системы, способствующие переносу токсических веществ через мембрану. Это является главным механизмом лечебного действия силибинина при отравлении бледной поганкой (противодействие яду a-амантину). Для лечения пациентов с подобными отравлениями разработана легкорастворимая форма силибинина для внутривенного введения (дигидросукцината натриевая соль).
Важной направленностью метаболического действия флавоноидов расторопши также является способность стимулировать синтез белков и поддерживать процесс регенерации гепатоцитов. Силибинин стимулирует РНК–полимеразу I в ядре клетки, активирует транскрипцию и скорость синтеза РНК.
При этом скорость транскрипции ДНК в малигнизированных клетках, а также скорость их деления не повышается, что исключает возможность стимуляции опухолевого роста при назначении препаратов расторопши.
Имеются данные о замедлении темпов прогрессирования фиброза печени на фоне длительного приема силибинина.
К сожалению, противовоспалительное и антифибротическое действие препаратов расторопши в настоящее время не подтверждены результатами мультицентровых рандомизированных контролируемых исследований, а имеющиеся данные получены по результатам отдельных наблюдений. Эффективность силимарина должна быть оценена согласно принципам медицины, основанной на доказательствах.
Производные расторопши пятнистой целесообразно назначать пациентам, страдающим заболеваниями печени (преимущественно хроническими): стеатозом печени, острым или хроническим гепатитом, циррозом различной этиологии. Следует соблюдать осторожность при их назначении больным с отчетливо выраженным внутрипеченочным холестазом: имеются сведения о возможности нарастания застоя желчи под действием препаратов.
Отмечено, что как острые, так и хронические заболевания печени достаточно часто сопровождаются развитием сопутствующей дискинезии желчевыводящих путей. Дискинезия желчевыводящих путей и является ведущей причиной появления болевых ощущений в эпигастральной области и правом подреберье при стеатозе, гепатите и циррозе печени, нередко с характерной иррадиацией в правую половину грудной клетки, правую лопатку и отчетливой связью с приемом жирной, жареной пищи.
Развитие нарушений моторики желчных путей нередко диктует необходимость назначения пациенту препаратов, обладающих мягким спазмолитическим действием на гладкомышечные клетки билиарной системы.
Силимарин непосредственно обладает желчегонными свойствами благодаря наличию у него одновременно холеретического и холекинетического действия. Холерез развивается благодаря повышению секреции желчных кислот и электролитов гепатоцитами. Холекинетический эффект связан со снижением тонуса сфинктеров желчевыводящих путей.
Однако многие из препаратов, главным действующим началом которых являются флавоноиды расторопши, содержат в своем составе компоненты других лекарственных растений, обладающие комбинированным воздействием на состав и отток желчи: умеренным желчегонным, спазмолитическим, противовоспалительным и антисептическим действием.
Главное действующее вещество из семейства лекарственных флавоноидов расторопши – силибинин – входит в состав различных препаратов: Сибектан, Легалон, Сиромин и др. Различия между этими препаратами состоят в количественных соотношениях флавоноидов, а также в сочетаниях расторопши с другими средствами, как правило, обладающими желчегонным или антисептическим эффектом.
Препарат Сибектан
содержит в своем составе сухой экстракт из пижмы, плодов расторопши пятнистой, зверобоя и березы.
Трава зверобоя содержит дубильные вещества группы катехинов (танины, флавоноиды, эфирные масла), которые оказывают вяжущее и противовоспалительное действие на слизистую оболочку желудочно–кишечного тракта.
Цветки пижмы также содержат различные флавоноиды, эфирные масла и органические кислоты, которые оказывают желчегонное действие (повышают сократительную активность желчного пузыря).
Экстракт листьев березы также оказывает антисептическое, мягкое желчегонное и отчетливое мочегонное действие.
Сибектан успешно применяется в терапии хронического холецистита, гипотонической дискинезии желчного пузыря. Его назначают при гепатитах и циррозах печени с целью профилактики прогрессирования процесса.
Учитывая наличие в составе препарата веществ с достаточно выраженной холекинетической активностью, способных усиливать моторную функцию желчного пузыря, Сибектан следует назначать с осторожностью при желчно–каменной болезни.
Препараты флавоноидов расторопши пятнистой назначают главным образом перорально, за полчаса до приема пищи. Они быстро и полно всасываются из желудочно–кишечного тракта. Связывание с белками плазмы слабое. Выводятся преимущественно с желчью, в меньшей степени – с мочой; период полувыведения составляет около 6 ч. Активно включаются в энтерогепатическую циркуляцию, что представляется выгодным фармакокинетическим параметром.
Продолжительность курсов лечения – от 25 дней до 1,5 месяцев. Возможны повторные курсы.
В многочисленных исследованиях установлено, что препараты расторопши относятся к категории малотоксичных веществ и в терапевтических дозах не оказывают повреждающего действия на основные органы и системы организма животных и человека.
При назначении следует учитывать возможность развития аллергических реакций на растительные компоненты.
Литература:
1. ФАРМиндекс: ПРАКТИК, выпуск 3 – СПб.: ООО «ФАРМиндекс», 2002 –136 с.
2. Berkson BM. A conservative triple antioxidant approach to the treatment of hepatitis C. Combination of alpha lipoic acid (thioctic acid), silymarin, and selenium: three case histories. Med Klin 1999 Oct 15;94 Suppl 3:84–9.
3. Deak G, Muzes G, Lang I, et al. Immunomodulator effect of silymarin therapy in chronic alcoholic liver diseases. Orv Hetil 131:1291–1292;1990.
4. Feher J, Deak G, Muzes G, et al. Liver–protective action of silymarin therapy in chronic alcoholic liver diseases. Orv Hetil 130:2723–2727; 1989.
5. Ferenci P, Dragosics B, Dittrich H, Frank H, et al. Randomized controlled trial of silymarin treatment in patients with cirrhosis of the liver. J Hepatol 9:105–113; 1989.
6. Lang I, Nekam K, Deak G, et al. Immunomodulatory and hepatoprotective effects of in vivo treatment with free radical scavengers. Ital J Gastroenterol 22:283–7; 1990.
7. Magliulo E, Gagliardi B, Fiori GP. Results of a double blind study on the effect of silymarin in the treatment of acute viral hepatitis, carried out at two medical centres. Med Klin 73:1060–1065; 1978.
8. Muzes G, Deak G, Lang I, et al. Effect of silimarin (Legalon) therapy on the antioxidant defense mechanism and lipid peroxidation in alcoholic liver disease (double blind protocol). Orv Hetil 131:863–866; 1990.
9. Reyes H, Simon FR. Intrahepatic cholestasis of pregnancy: an estrogen–related disease. Semin Liver Dis 13:289–301; 1993.
10. Salmi HA, Sarna S. Effect of silymarin on chemical, functional, and morphological alterations of the liver. A double–blind controlled study. Scand J Gastroenterol 17:517–521; 1982.
Показания к приему
Согласно инструкции по применению масло расторопши в капсулах показано при следующих заболеваниях и патологических состояниях:
- болезни печени (гепатит различной этиологии, цирроз, алкогольная или неалкогольная жировая инфильтрация, желчекаменная болезнь, дискинезия желчного пузыря);
- гастрит или язва желудка;
- колит, энтероколит;
- гипертония;
- атеросклеротическое поражение сосудов;
- ишемическая болезнь сердца;
- сахарный диабет;
- дерматиты;
- дефицит витаминов A, Е.
Применяют силимарин и как гепатопротектор при проведении химиотерапии злокачественных опухолей. Положительное влияние также зафиксировано при тяжелом токсическом поражении печени: капсулы с маслом расторопши можно принимать как антидот при отравлении, вызванном бледной поганкой.
Местно масло расторопши применяется в таких сферах:
- стоматология (стоматиты, гингивиты);
- оториноларингология (фарингиты, ангины, риниты);
- гинекология (кольпит, эрозии, сухость влагалища);
- косметология (в качестве компонента питательных масок).
Jarrow Formulas, Расторопша пятнистая, 150 мг, 100 вегетарианских капсул
★★★★★
622 руб.
Подробнее
Особенности
Масло расторопши — это уникальный природный продукт по своему составу. Он отличается огромным ассортиментом целебных свойств. Кроме того важно, что средство имеет минимальное количество противопоказаний. Наиболее часто используют масло расторопши в качестве гепапротекторного средства. Кроме того оно усиливает защиту организма от различных внешних негативных факторов.
Масло расторопши отличается желтовато-зелёным оттенком. Природный продукт имеет приятный вкус и запах. Польза масла расторопши связана с насыщенным составом. Продукт содержит флавоноиды группы силимарина. Эти вещества благоприятно воздействует на работу печени, способствуя обновлению и восстановлению ее клеток. Силимарин снижает риски повреждения печени токсическими веществами.
Кроме этого в масле расторопши содержатся все существующие жирорастворимые витамины. Это:
- Витамин D, способствующий усвоению фосфора и кальция, а также укрепляющий иммунитет.
- Витамин К, который регулирует свертываемость крови.
- Токоферолы, защищающие организм от действия свободных радикалов и поддерживающие правильную работу репродуктивной и сердечно-сосудистой системы.
- Каротиноиды, обеспечивающие рост, поддерживающие функцию зрения и нормализующие обмен веществ.
Важными компонентами в составе масла расторопши являются:
- Витамины группы В. Они участвуют во многих процессах в организме человека, в частности способствуют синтезу гемоглобина. Кроме того данные вещества нормализуют работу нервной системы.
- Ненасыщенные жирные кислоты. Эти вещества предотвращают развитие инсультов и инфарктов минимизируют риски возникновение атеросклероза.
В составе масла расторопши содержатся соединения важных для организма минералов, в частности цинка, селена, магния и др. Они важны для правильности протекания различных процессов, а поддерживают внутренние органы и системы в хорошем состоянии.
Противопоказания и меры предосторожности
К абсолютным противопоказаниям относятся:
- аллергия на компоненты препарата;
- острый холецистит или панкреатит;
- клиническая депрессия;
- эпилепсия;
- бронхиальная астма.
При беременности или лактации принимать капсулы можно только по согласованию с врачом. Масло также обладает слабительным эффектом, поэтому при любых заболеваниях, связанных с диареей, употреблять расторопшу в капсулах необходимо с осторожностью, в небольших количествах. При хронической сердечной недостаточности или нарушении функции почек требуется контроль уровня калия в крови.
Следует также соблюдать осторожность и при наличии желчекаменной болезни. Из-за выраженного желчегонного действия силимарина прием расторопши рекомендуется комбинировать со спазмолитиками, расслабляющими сфинктер Одди. Это поможет предупредить застревание камня в протоке и развитие желчной колики.
Внимание! Перед началом лечения необходимо провести УЗИ гепатобилиарной зоны для оценки количества и размеров конкрементов.
Любые желчегонные средства противопоказаны при наличии единичных крупных камней или более 3 мелких. Песок или эхогенная взвесь в желчном пузыре поддаются лечению, поэтому не являются противопоказанием.
Формы выпуска
Капсулы с расторопшей могут содержать экстракт или масло из семян растения. Основное действующее вещество первого – силимарин, его используют для защиты или восстановления печени.
Масло имеет более богатый состав, включающий полиненасыщенные жирные кислоты, жирорастворимые витамины, а соответственно много показаний. Однако при приеме этой формы выпуска часто наблюдаются побочные эффекты в виде диареи или дискомфорта в правом подреберье, вызванные мощным холеретическим действием. Капсулы с маслом можно употреблять только при полностью сохраненной функции поджелудочной железы: дефицит вырабатываемой ею липазы приведет к плохой усвояемости и стеаторее.
Инструкция по применению капсул с экстрактом расторопши
Таблица 1 – Основные препараты с экстрактом расторопши
| Название | Цена упаковки (от), руб. | Форма выпуска | Ежедневная дозировка, шт. |
| Экстракт расторопши (Эвалар, РФ) | 100 | Таблетки | 1 (30 мг) |
| Расторопша-экстра (Фармакор Продакшн, РФ) | 180 | Капсулы | 1 (220 мг) |
| Молочный чертополох (Jarrow Formulas, США) | 1069 | 1-3 (150-450 мг) | |
| Молочный чертополох (Natrol, США) | 484 | 2 (525 мг) | |
| Силимарин, экстракт молочного чертополоха (Now Foods, США) | 588 | 2-6 (300 мг) |
Согласно рекомендациям гастроэнтерологов, препараты с силимарином следует принимать внутрь, после еды. Лечебные дозировки составляют около 500 мг в сутки, профилактические – 200-300.
Клинические исследования показали, что ежедневный прием до 900 мг действующего вещества абсолютно безопасен. При повышении количества до 1500 мг в день у 2-10% людей могут развиваться побочные эффекты.
Курс лечения составляет не менее 3 месяцев.
Опыт применения препарата Простопин у больных хроническим простатитом с патоспермией
В.В. Евдокимов, М.Н. Коршунов, Е.С. Коршунова, А.С. Кондратьев, Е.И. Дубков ФГУ «НИИ Урологии» Минздравсоцразвития России, Москва
В настоящее время доля мужского фактора в бесплодном браке составляет почти 50%. Многочисленные исследования показали, что последние десятилетия отмечены падением уровня мужской фертильности [2, 9, 20]. Многофакторность данной проблемы стала очевидной. Рассматриваются, в первую очередь, внешние и внутренние факторы патологического воздействия. К внешним влияниям относят: электромагнитное излучение мобильных телефонов, компьютеров, загрязнение почвы, воды, воздуха. В перечне внутренних факторов выделяют инфекционные заболевания репродуктивной системы, травмы половых органов и др. В последние два десятилетия появился ряд фундаментальных и прикладных работ по изучению регуляции функциональной активности мужской репродуктивной системы [3, 4, 13, 21]. Выработана парадигма многоуровневой системы репродукции, включающей иммунный, генетический, гормональный и другие компоненты.
Многофакторность патогенеза мужской инфертильности обуславливает трудности диагностики и лечения мужского бесплодия. Выбор адекватной терапии зависит от точного понимания физиологических механизмов нарушения сперматогенеза [24, 25, 26]. Проводятся широкие исследования по коррекции различных видов патоспермии с использованием различных фармакологических препаратов [12].
Хронический простатит – одно из наиболее трудных для диагностики и лечения урологических заболеваний. Ряд исследователей полагают, что в большинстве случаев этиология, патогенез и патофизиология хронического простатита остаются неизвестными [8, 11, 15, 17]. До сих пор неясно, может ли процесс быть исходно абактериальным, или же заболевание, начавшись в результате проникновения инфекционных агентов в предстательную железу, в дальнейшем протекает без их участия, т.е. проходит инфекционную и постинфекционную фазы. Очевидно, что нельзя отождествлять высеваемые из секрета простаты микроорганизмы с этиологическим фактором заболевания, т.к. в большинстве случаев эта флора является сапрофитной. Безусловно признанными причинами бактериального воспаления предстательной железы являются Е.соli, Proteus, Klebsiella, Pseudomonas. Грамположительные энтерококки, внутриклеточные инфекции (хламидии, уреаплазмы, микоплазмы), туберкулез многим исследователям кажутся сомнительными патологическими агентами в развитии хронического простатита [7, 21].
Частота отдельных видов простатита по обобщенным данным литературы составляет: острый бактериальный простатит – 5–10%, хронический бактериальный простатит – 6–10%, хронический абактериальный простатит – 80–90% [1, 5].
Национальным институтом здоровья США признано, что абактериальный простатит по частоте превышает бактериальный по меньшей мере в 8 раз. По данным ВОЗ только в США ежегодно хроническим простатитом заболевает около 3 миллионов мужчин трудоспособного возраста, при этом у 40% из них выявляется хламидийная инфекция [23]. Этиологическое значение этой и других инфекций полового тракта в развитии хронического абактериального простатита не доказано [22].
Нельзя не отметить, что у больных хроническим абактериальным простатитом нередко выявляется патоспермия различной степени выраженности [12]. Известно, что развитие разнообразных по генезу расстройств репродуктивной функции у мужчин сопровождается повышенным образованием активных форм кислорода [2]. В частности, при хронических воспалительных заболеваниях предстательной железы происходит накопление активных форм кислорода с активацией свободно-радикального окисления биополимеров, как следствие, повреждение сперматозоидов и последующее снижение их функциональной активности [12].
Усиление процессов перекисного окисления липидов на фоне сниженной антиоксидантной защиты в эякуляте является, по крайней мере, одной из причин развития субфертильности.
Лечение патоспермии, независимо от этиологических факторов, не всегда эффективно, что не удовлетворяет обе стороны – ипациента, иврача. Вэтой связи поиск препаратов, воздействующих на сперматогенез, является актуальной задачей.
С 2002 года в России выпускается лекарственный препарат Простопин, применяющийся в разных областях медицины [6, 10, 14, 16, 18, 19]. Простопин представляет собой ректальные суппозитории бурого цвета со специфическим запахом прополиса. Препарат включает в свой состав активированный прополис (нативный и экстракты), молочко маточное пчелиное, пергу сушеную, пыльцу цветочную (обножку), мёд натуральный, воск пчелиный, ланолин безводный, масло какао. На сегодняшний день установлено противовоспалительное и противоотечное действие Простопина, однако менее изучено его влияние на процессы сперматогенеза, в частности, на фертильные параметры эякулята.
Цель
Оценить эффективность применения препарата Простопин при патоспермии у больных хроническим простатитом.
Материалы и методы
На базе консультативной поликлиники ФГУ «НИИ урологии» Минздравсоцразвития проведено проспективное, несравнительное исследование влияния препарата Простопин на репродуктивную функцию мужчин, страдающих хроническим простатитом. Группу пациентов составили 25 мужчин в возрасте от 20 до 45 лет (средний возраст 32,5 лет). Клинический диагноз хронический абактериальный простатит поставлен на основании жалоб пациента (боли в промежности и уретре, учащённые позывы к мочеиспусканию, стёртый оргазм) и клинического обследования, включавшего УЗИ простаты, исследования секрета предстательной железы и посева эякулята. При УЗИ выявлено увеличение объёма простаты (в среднем до 29,7±6,7 см3 ), отёчность ткани и изменение эхогенности рисунка в железе, что свидетельствовало о застойном процессе в органе. В анализе секрета простаты обнаружено незначительное повышение лейкоцитов до 10-12 в поле зрения и уменьшение количества лецитиновых зёрен. Посев спермы роста микрофлоры не выявил. Анализ эякулята, проведенный до назначения курса терапии, обнаружил снижение подвижности сперматозоидов, что оценивалось по стандартам ВОЗ как астенозооспермия [23]. Всем больным назначали Простопин в виде монотерапии. Курс лечения продолжался 1 месяц, во время которого каждый пациент получал по 2 свечи в сутки (утром и перед сном).
Результаты и обсуждение
По окончании месячного курса лечения все пациенты отметили уменьшение или исчезновение болей в промежности, при УЗИ выявлено уменьшение объёма предстательной железы в среднем с 29,7±6,7 до 16,6±4,7 см3 , изменение показателей эякулята. В таблице приведены результаты основных параметров фертильности. Установлено достоверное повышение объёма спермы, числа живых сперматозоидов, общей и активной подвижности сперматозоидов. Полученный эффект в отношении данных параметров эякулята может быть обусловлен биологическими свойствами препарата Простопин. Выявлено снижение концентрации сперматозоидов. По нашему мнению, данные изменения могут быть обусловлены усилением либидо и активацией половой жизни, отмеченными 18 из 25 больных. Необходимо заметить, что как до, так и после лечения, концентрация сперматозоидов не выходила за границы референтных показателей (ВОЗ, 2001 г.). Мы полагаем, что необходимо продолжить дальнейшие исследования свойств Простопина в группе с большим количеством больных и более длительным периодом использования препарата.
Таблица. Основные показатели эякулята до и после лечения (n=25).
| Показатель | До лечения | После лечения | Нормы ВО |
| Объем эякулята, мл | 3,4±1,2 | 4,2±1,4* | 2-6 |
| Концентрация сперматозоидов, млн/ мл | 71,4±33,7 | 60,9±22,5 | более 20 |
| Живые сперматозоиды, % | 62, 2±5,9 | 65,9±2,3** | 70 |
| Общая подвижность сперматозоидов, % | 31,9±9,6 | 39,4±12,4* | 50 |
| Активная подвижность сперматозоидов, % | 12,0±4,9 | 16,3±6,9* | 25 |
| Нормальные формы сперматозоидов, % | 34,1±10,6 | 39,0±8,2 | 30 |
*- различие достоверно по сравнению с соответствующим показателем до лечения (р<0,05). **- различие достоверно по сравнению с соответствующим показателем до лечения (р<0,01).
Выводы
Таким образом, полученные результаты свидетельствуют о том, что назначение Простопина в виде монотерапии является эффективным, безопасным и доступным методом лечения патоспермии у больных хроническим простатитом. Простопин способствует улучшению параметров эякулята, что позволяет его рекомендовать для повышения фертильности при патоспермии разной этиологии.
Список литературы
1. Белозеров М.Н., Морозова Л.В. Комплексный подход в лечении хронического простатита в амбулаторных условиях. Матер. конг- ресса «Мужское здоровье» М., 2008, 91-92. 2. Божедомов В.А. Мужское иммунологическое бесплодие. Дисс. докт.мед.наук М., 2001. 3. Брагина Е.Е., Абдумаликов Р.А. Руководство по сперматологии. М., 2002.
Проблемы репродукции, 2005, №2, 19-22. 5. Гориловский Л.М., Зингеренко М.Б. Хронический простатит. Лечащий врач. 2003; 7. 6. Денисов А.К., Калмыков А.А., Сараф А.С. Простопин – современный высокоэффективный препарат для лечения острых и хронических урологических и проктологических заболеваний вирусно-бактериального генеза. Трудный пациент. 2007; 3: 39–41. 7. Ильин И.И. Негонококковые уретриты у мужчин. – М., Медицина, 1991. 8. Коган М.И., Шангичев А.В. Оценка лечения хронического простатита в амбулаторных условиях. – Матер. Конгресса «Мужское здоровье», М., 2008, 91-92. 9. Кулаков В.И. Бесплодный брак. Современные подходы к диагностике и лечению. М. ГЭОТАР-Медиа, 2005, 616. 10. Кучерский В.М., Калмыков А.А., Дубков Е.И. Современные проблемы в лечении хронического простатита. – РМЖ. 11. Лоран О.Б., Пушкарь Д.Ю., Сегал А.С. Наше понимание простатита. – Фарматека. 2002; 10: 69–75. 12. Луцкий Д.Л., Полунин А.И. Исследование спермоплазмы при хроническом неспецифическом простатите и уретрите. – Андрол. и генит. хирургия, 2002, №3, 32 – 33. 13. Нишлаг Э., Бере Г.М. Андрология: мужское здоровье и дисфункция репродуктивной системы. М., МИА, 2005, 554. 14. Перепанова Т.С.. Хазан П.Л. Профилактика и лечение инфекционно-воспалительных осложнений в урологической клинике. Все- российская научно-практическая конференция. М., 2007, 105-106. 15. Перепанова Т.С. Современное ведение пациентов с хроническим простатитом. – Эффективная фармакотерапия в урологии. 2009, №2, 2 – 7. 16. Простопин.- Пособие для врачей. М.: 2007: 20. 17. Пушкарь Д.Ю., Зайцев А.В., Раснер П.И. Оптимизация алгоритма диагностики и лечения хронического бактериального проста- тита. – РМЖ. 2008; 16: 17: 34–38. 18. Сараф А.С., Суворов А.Н. Комплексный природный препарат в виде суппозиториев для лечения урологических, проктологических и гинекологических заболеваний и способ его получения. Описание к патенту на изобретение. 2000. 19. Сараф А.С., Калмыков А.А., Денисов А.К. Об эффективностиприменения нового оригинального отечественного препарата Про- стопина для лечения острого и хронического простатита и доброкачественной гиперплазии предстательной железы. – Трудный пациент. 2007; 12: 5–7. 20. Тер-Аванесов Г.В. Андрологические аспекты бесплодного брака. М., 2002. 21. Тиктинский О.Л. Руководство по андрологии. Л., 1990. 22. Ткачук В.Н. Хронический простатит. М., 2006. 23. Руководство ВОЗ по лабораторному исследованию эякулята человека и взаимодействия сперматозоидов с цервикальной слизью. 4-е изд. М., 2001. 24. Comhaire F, Decleer W. Quantifying the effectiveness and cost-efficiency of food supplementation with antioxidants for male infertility. Reprod Biomed Online. 2011 May 19. 25. Foster R, DaCosta V, Everett D, Christie L, Harriott J, Wynter S, Frederick J, Walters Y. Successful treatment of severe male factor infertili ty in Jamaica with intracytoplasmic sperm injection. West Indian Med J. 2011 Jan;60(1):41-5. 26. Rozen S. Defending male fertility. Sci Transl Med. 2011 Jul 20;3(92):92ps31.
Тематики и теги
Биннофарм
Комментарии
Для отправки комментариев необходимо войти или зарегистрироваться
Побочные эффекты и аллергия
Масло расторопши – одно из самых гипоаллергенных препаратов, однако, в редких случаях, и оно может вызывать гиперчувствительность. При появлении красных, зудящих высыпаний на коже, отека век, губ, языка, затрудненного дыхания, прием препарата нужно немедленно прекратить, а также принять антигистаминное средство.
К прочим побочным эффектам относятся:
- тошнота;
- слабость;
- отсутствие аппетита;
- головная боль;
- вздутие живота;
- дискомфорт в правом подреберье;
- диарея.
Отзывы о применении
Написать отзыв и поделиться своим мнением о лечении молочным чертополохом можно в специальной форме:
| Оставить свой отзыв | |
| 1 2 3 4 5 | |
| Отправить Отменить | |
Отправить свой отзыв
Расторопша в капсулах
Средний рейтинг: Кол-во отзывов: 0
Отзывы покупателей, принимавших препараты с расторопшей, в основном положительные.
Плюсы:
- эффективность (снижение трансаминаз, билирубина в крови, улучшение показателей функции печени);
- безопасность даже при длительном лечении.
Минусы:
- появление тошноты;
- горечи во рту;
- послабление стула (для пациентов с запорами это может быть плюсом).
Лекарственное взаимодействие
При лечении дозировками, составляющими менее 1500 мг силимарина в сутки, расторопша не влияет на лекарства и не теряет свойства при взаимодействии с другими препаратами. Но врачи все же советуют:
- Для усиления эффекта и профилактики диспепсии у пациентов с дисфункцией желчного пузыря или сфинктера Одди прием капсул с маслом рекомендуется сочетать с папавериноподобными спазмолитиками. Наиболее удачными являются комбинации с дымянкой лекарственной, тысячелистником, фенхелем, Мебеверином, Одестоном.
- Хорошо сочетаются пищевые добавки с другими гепатопротекторами: эссенциальными фосфолипидами, производными аминокислот, липоевой кислотой.
- При подозрении на дефицит липазы поджелудочной железы масляные капсулы необходимо дополнять ферментными препаратами для полноценного всасывания жиров.
Рекомендации
Рекомендуемая дозировка предполагает трехразовый прием капсул в сурки. Единоразовое количество – 4 капсулы. Прием масла расторопши обязательно нужно согласовать с доктором. Длительность курса – не дольше 2 месяцев. После перерыва разрешается повторить прием капсул масла расторопши. Но при этом не рекомендуется использовать биологически активную добавку чаще 3 раз в год. Если не наблюдается положительного эффекта при приеме средства в течение первых недель, то следует отказаться от него.
Масло расторопши нужно хранить при температуре не выше 18°C в сухом месте. Важно исключить доступ детей к биологически активной добавке. Срок годности природного продукта составляет 2 года. Просроченное средство принимать категорически запрещено.


![Таблица 1. Сравнение результатов лечения Трибестаном мужчин с олигоастенозооспермией [7] с модиф.](https://ms-pi.ru/wp-content/uploads/tablica-1-sravnenie-rezultatov-lecheniya-tribestanom-muzhchin-s-oligoastenozoospermiej-7-330x140.jpg)