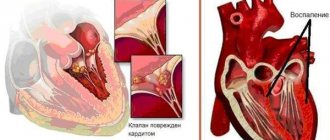
Сердечная недостаточность (СН) — патологическое состояние, обусловленное несостоятельностью сердца как насоса, обеспечивающего адекватное кровообращение. Проявление и следствие патологических состояний, поражающих миокард или затрудняющих работу сердца: ишемической болезни сердца, пороков сердца, артериальной гипертензии, диффузных заболеваний легких, миокардита, дистрофии миокарда (в том числе тиреотоксической, спортивной и др.), миокардиопатий (в том числе алкогольной) и др.
Сердечная недостаточность острая бывает либо собственно острая, либо это могут быть острые проявления хронической СН.
Что это такое
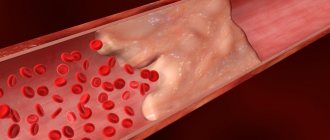
Коронарная недостаточность (КН) — это такое состояние, при котором ток крови по коронарным (венечным) артериям, не соответствует энергетическим потребностям сердца. При этом наступает ишемия миокарда — повреждение клеток сердца вследствие недостатка кислорода и питательных веществ. Ишемия — локальный процесс, который происходит в том месте миокарда (сердечной мышцы), где было нарушено его питание. Сам процесс ухудшения кровотока чаще всего объясняется сужением просвета приносящего кровь сосуда. Глобально это может произойти по 2 причинам:
- обтурация (закупорка) просвета артерии;
- спазм вследствие сокращения стенок сосуда.
Также возможна комбинация этих причин.
При этом человек не может заметить никаких изменений в своем состоянии до тех пор, пока уровень стеноза (сужения просвета артерии) не достигнет критических значений. Или же до той поры, пока потребность сердца в питании не сделает стеноз значимым. Когда эти условия выполняются, в участке сердечной мышцы развивается ишемия — возникают приступ стенокардии, инфаркт миокарда или даже внезапная кардиальная смерть. Таким образом, можно сказать, что клинически коронарная недостаточность проявляет себя различными формами ишемической болезни сердца (ИБС).
Число больных ИБС в России по данным исследований превышает 7,5 млн человек — это очень высокий показатель. При этом распространенность среди людей пенсионного возраста на 16% выше, чем у людей трудоспособного возраста. То есть встречаемость заболевания с возрастом прогрессирует. Мужчины заболевают раньше и чаще, чем женщины.
На какие классы делится сердечная недостаточность?
Существует несколько классификаций сердечной недостаточности:
- Классификация по В. Х. Василенко, Н. Д. Стражеско, Г. Ф. Ланга;
- Классификация острой сердечной недостаточности по шкале Killip;
- И самая распространенная, классификация Нью-Йоркской кардиологической ассоциации.
Согласно функциональной классификации Нью-Йоркской кардиологической ассоциации (NYHA), сердечная недостаточность подразделяется на классы I-IV в зависимости от выраженности симптомов и ограничения физической активности.
Сердечная недостаточность делится на четыре класса в зависимости от выраженности симптомов:
- NYHA I: болезнь сердца без каких-либо ограничений физической активности. Нормальная активность не вызывает повышенного утомления, сердцебиения или затруднения дыхания.
- NYHA II: болезнь сердца, вызывающая умеренное ограничение в повседневной деятельности. Никаких симптомов в состоянии покоя.
- NYHA III: болезнь сердца, вызывающая заметное ограничение в повседневной деятельности. Простые действия, такие как чистка зубов, прием пищи или разговор, вызывают утомление, сердцебиение или затруднение дыхания. Симптомов в покое нет.
- NYHA IV: сердечные заболевания, вызывающие симптомы в состоянии покоя (и при любой степени легкой физической активности).
Сердечная недостаточность значительно снижает качество жизни. Больные часто испытывают большое разочарование в связи с физическими ограничениями и имеют тенденцию уходить из общественной жизни. По этой причине психологические расстройства, такие как депрессия, часто присутствуют в дополнение к ожидаемым физическим симптомам.
Причины
Коронарная недостаточность чаще всего возникает по причине обтурации или спазма венечных сосудов сердца или их ветвей. Рассмотрим более подробно каждый из этих случаев, а также несколько более редких ситуаций.
Снимок — коронарография сосудов сердца. Источник: Image by Mario Ohibsky from Pixabay
Обтурация артерии
Наиболее важной и частой причиной коронарной недостаточности является атеросклероз коронарных артерий. Атеросклеротические бляшки выступают внутрь просвета сосуда и препятствуют току крови. При этом развивается хроническая коронарная недостаточность, которая чаще всего дает о себе знать приступами стенокардии.
Атеросклеротические бляшки также могут оторваться или способствовать повреждению внутренней поверхности сосуда и спровоцировать таким образом его тромбоз, что станет причиной острой коронарной недостаточности. Ее частым проявлением становится инфаркт миокарда. Подробнее об атеросклерозе можно узнать здесь.
Спазм артерии
Коронарная недостаточность также возникает по причине резкого и продолжительного спазма коронарных артерий. Приводить к этому могут сильный стресс, психические и физические перегрузки. Часто перечисленные факторы дополняют уже имеющееся атеросклеротическое поражение сосуда, что выливается в стенокардию или инфаркт миокарда. Возможна, однако, и чисто спастическая коронарная недостаточность.
Другие причины
Существуют и другие, более редкие, причины нарушения кровоснабжения миокарда:
- Врожденные аномалии коронарных сосудов;
- Гипертрофическая кардиомиопатия — состояние, при котором имеющихся сосудов недостаточно для удовлетворения потребностей разросшегося миокарда (следствие гипертонической болезни);
- Новобразования в грудной клетке, сдавливающие сосуды извне (опухоль).
Факторы риска
Некоторые факторы повышают риск коронарной недостаточности:
- Мужской пол и возраст старше 45 лет — факторы которые никак не откорректировать.
- Курение — влияет как на развитие атеросклероза, так и на процессы тромбообразования. В сигаретном дыме содержатся никотин и оксид углерода, которые оказывают отрицательное влияние на деятельность сердечно‐сосудистой системы.
- Низкая физическая активность, сидячий образ жизни, лишний вес и ожирение — способствуют тромбозам, атеросклерозу, гипертонической болезни, которые могут привести к коронарной недостаточности.
- Употребление большого количества пищи с высоким содержанием жира и холестерина — способствует атеросклерозу.
- Хронический стресс — провоцируетдлительный спазм коронарных артерий.
- Наследственность — риск развития патологии выше, если она была у родственников.
Диагностика коронарной сердечной недостаточности
В большинстве случаев уже при визуальном осмотре больного врач может заподозрить развитие острой коронарной недостаточности. Но для подтверждения диагноза необходимо не только учесть совокупность клинических признаков, обусловленных коронарной недостаточностью, но и провести диагностическое обследование, которое включает в себя:
- Общий анализ крови (главный показатель – повышенное число эритроцитов, свидетельствующее о наличии в организме воспалительного процесса).
- Биохимический анализ крови (позволяет понять причину заболевания).
- Анализ крови на свертываемость (изучается консистенция кровотока, склонность к тромбообразованию).
- Коронарографию (главный диагностический метод, направленный на оценку состояния коронарных артерий).
- Рентгенографию, УЗИ грудной клетки (позволяют определить наличие у пациента других возможных болезней сердечно-сосудистой системы и установить причину коронарной недостаточности).
- Электрокардиографию (дает возможность судить об исправности сократительной функции миокарда и работе сердца).
- Компьютерную томографию (направлена на выявление стеноза венечных артерий, разных по размеру атеросклеротических бляшек).
- Магнитно-резонансную томографию сердца (позволяет делать снимки в разных плоскостях, измерять артериальный кровоток, изучать наполнение желудочков и предсердий).
Симптомы
Симптомы коронарной недостаточности могут отличаться от случая к случаю. Также нередки ситуации, когда пациенты не чувствуют ничего странного в своем состоянии, пока однажды не случается, например, инфаркт миокарда.
Среди наиболее характерных для коронарной недостаточности симптомов:
Боли стенокардического характера — давящие, сжимающие, жгучие боли за грудиной продолжительностью до 10 минут. Часто появляются во время физической нагрузки. Могут начаться за грудиной, а затем распространиться на шею, спину, плечи, руки, челюсти;
- Головокружение;
- Холодный пот;
- Боли в области желудка;
- Одышка, особенно при нагрузках;
- Нарушения сна;
- Слабость.
Важно! При обнаружении подобных симптомов, особенно на фоне непривычной физической активности, — нужно незамедлительно вызвать скорую помощь. Также это нужно сделать, если стенокардия уже диагностирована, но симптомы не купируются нитроглицерином и длятся дольше 15 минут.
Источник: Pavel Danilyuk: Pexels
Перечисленная симптоматика характерна для хронического (обратимого) варианта коронарной недостаточности, который проявляется стенокардией. При остром (необратимом) варианте описанные симптомы выражены ярче и длятся значительно дольше — до нескольких суток (при инфаркте миокарда). Боль не купируется нитроглицерином и может быть настолько выраженной, что приходится прибегать к наркотическим препаратам.
Несмотря на то, что главным симптомом инфаркта чаще всего является сильная загрудинная боль (80% случаев), существуют и другие проявления заболевания:
- Кашель и одышка;
- Резкая боль в верхней части живота;
- Симптомы поражения головного мозга.
Редко встречается бессимптомная форма инфаркта миокарда. Область поражения в сердце при этом не столь обширна, а изменения фиксируют инструментально постфактум.
Симптомы хронической и острой коронарной недостаточности сердца
Среди главных признаков синдрома коронарной недостаточности:
- учащенное сердцебиение;
- бледность кожных покровов, появление капель пота на лбу;
- сильная боль за грудиной, имеющая приступообразный характер;
- одышка, возникающая по непонятным причинам;
- боль в области груди;
- приступы стенокардии/тахикардии;
- сухой кашель.
Симптоматика усугубляется после выполнения физической работы, переедания, подъема по лестнице, эмоциональных переживаний (паника, испуг). Также она может обостряться в стадии покоя.
У некоторых больных коронарной недостаточностью возникают:
- тошнота;
- рвота;
- частые позывы к мочеиспусканию;
- метеоризм.
Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу. Легче предупредить болезнь, чем бороться с последствиями.
Хроническая форма
Типичным проявлением хронического варианта коронарной недостаточности является стенокардия. Чаще всего она обусловлена атеросклеротическим поражением венечных артерий сердца, что вызывает сужение их просвета. При физической нагрузке миокард требует больше крови, в то время как пропускания способность артерии уменьшена — возникает ишемия с характерными симптомами.
Когда приступы предсказуемы и повторяются в ответ на нагрузку одинаковой тяжести, говорят о стабильном варианте стенокардии. Течение ее относительно благоприятное и хорошо поддается контролю. Существуют и другие варианты:
- Нестабильная стенокардия — форма стенокардии, при которой бляшка в коронарном сосуде подвергается изъязвлению, в просвете постепенно нарастает тромб, отчего приступы постоянно прогрессируют и приводят в итоге к инфаркту миокарда.
- Стенокардия Принцметала (вазоспастическая стенокардия) — возникает в результате внезапного спазма коронарных артерий.
Мы писали о стенокардии подробнее тут.
До этого момента речь шла по большей части об абсолютной коронарной недостаточности, когда непосредственной причиной патологического состояния были патологические процессы в коронарных сосудах. Но существует также относительная форма, возникающая на фоне гипертрофической кардиомиопатии, о которой говорили в причинах коронарной недостаточности. При этом процессе миокард увеличивается в размерах из-за возросшей нагрузки, в то время как новые сосуды не возникают. В этом случае также развивается ишемия плохо кровоснабжаемых участков.
Коронарная недостаточность – что это такое
- Острая коронарная сердечная недостаточность. Характеризуется несоответствием кровотока метаболической потребности миокарда (параллельно могут диагностироваться измененные венечные артерии сердца, наблюдаться приступы стенокардии, тяжелые расстройства сердечного ритма, изменения ЭКГ). Болезнь, протекающая по острому типу, нередко провоцирует развитие инфаркта миокарда.
- Хроническая коронарная недостаточность. Характеризуется продолжительным (постоянным) недостаточным кровоснабжением миокарда. Предпосылкой для возникновения патологии служит изменение коронарного русла.
Также коронарная недостаточность сердца может протекать в:
- абсолютной форме (кровоток по коронарным сосудам резко ограничен);
- относительной форме (потребность миокарда в кислороде значительно повышается, но ограничения коронарного кровотока отсутствуют).
Внезапная коронарная смерть
О внезапной коронарной смерти (ВКС) говорят, когда человек умирает в течение не более 6 часов на фоне кажущегося благополучия по причине кардинального сбоя в работе сердца. При этом больной теряет сознание и падает.
Как правило, непосредственной причиной ВКС становится желудочковая тахикардия и фибрилляция желудочков. Это тяжелые нарушения ритма, при которых эффективность сокращения миокарда падает настолько, что кровь не поступает к жизненно важным органам в достаточном объеме.
ВОЗ рекомендует не менее 150 минут физической активности в неделю — это поможет снизить риск ВКС. Источник: Mario Ohibsky from Pixabay
Однако предшествует этим аритмиям чаще всего тяжёлый приступ острой коронарной недостаточности. Обширное поражение миокарда в результате этого приступа не только само по себе снижает сократительную способность желудочков сердца, но также способствует возникновению аритмий.
Иногда летальный исход удается предотвратить при своевременно оказанной помощи, однако это более характерно для внезапной сердечной смерти аритмогенного характера. В этом случае развивающаяся аритмия имеет первостепенное значение, а коронарные причины вторичны. Больные сахарным диабетом находятся в группе повышенного риска ВКС.
Важно! Если вы увидели, как человек внезапно потерял сознание, то должны вызывать скорую помощь и, при владении соответствующими навыками, выполнить первичные реанимационные мероприятия. К сердечно-легочной реанимации следует прибегать, если вы не обнаружили пульса и/или дыхания у пострадавшего.
Несмотря на такую угрозу у больных с коронарной недостаточностью, при грамотно подобранном лечении и четком выполнении назначений врача вероятность ВКС становится значительно ниже. Также важно своевременное обращение за медицинской помощью. Известно, что за несколько недель до приступа больные иногда жалуются на боль за грудиной, ухудшение настроения, быструю утомляемость. Это означает, что можно предпринять какие-либо лечебные меры до наступления приступа.
Опасность коронарной недостаточности
Коронарная недостаточность может привести к двум угрожающим жизни состояниям:
- нестабильной стенокардии;
- инфаркту миокарда.
Учитывая симптомы заболевания, врачи могут определить, насколько высок риск внезапной коронарной смерти (наступает в течение шести часов с момента начала сердечного приступа).
Высокий риск летального исхода – если присутствует любой из следующих признаков:
- Приступ стенокардии длится больше 20 минут.
- Развился отек легких (больной постоянно стоит, тяжело дышит, выделяется пенистая розовая мокрота).
- На ЭКГ снижен или увеличен подъем сегмента ST более 1 мм над изолинией.
- Стенокардия, пониженное давление в артериях.
- По лабораторным анализам – вираж уровня маркеров некроза (отмирания) миокарда.
Средний риск внезапной смерти при коронарной недостаточности ставится, если наблюдает любой из симптомов:
- Приступ длится меньше 20 минут.
- Стенокардия покоя – менее 20, прекратилась после рассасывания «Нитроглицерина».
- Ночью постоянно возникают приступы загрудинной боли.
- Возраст больного – старше 65 лет.
- Тяжелая стенокардия, первые симптомы которой проявились в течение последних двух недель.
- На ЭКГ зубцы Q более 3 мм, динамические изменения зубца Т до показателя нормы, снижение сегмента ST в покое.
Низкий риск внезапной смерти можно предположить при следующей симптоматике:
- Приступы возникают даже после несложной физической работы.
- В последнее время приступы стали более частыми и тяжелыми.
- Стенокардия впервые появилась от двух недель до двух месяцев назад.
- На ЭКГ отсутствуют новые изменения (по сравнению с результатами, которые были получены ранее) либо наблюдается нормальная для возраста больного кривая.
Диагностика
Признаки коронарной недостаточности можно заподозрить самостоятельно, обнаружив у себя симптомы стенокардии, хотя бессимптомное течение вплоть до инфаркта миокарда — не редкость.
В клинической практике используют следующие диагностические методы:
- Коронарография — золотой стандарт в диагностике патологии сосудов сердца, позволяет визуализировать сужения просвета в коронарных артериях, их обтурацию. Методика инвазивная — катетер для введения контрастного вещества ставят через лучевую или бедренную артерии, поэтому исследование выполняют в операционной под местной анестезией.
- Оптическая когерентная томография коронарных артерий — один из новых и точных методов визуализации проблемных участков в венечных сосудах сердца. Метод также инвазивный и выполняется схожим с коронарографией образом.
- Различные варианты эхокардиографии (Эхо-КГ) — позволяют визуализировать участки миокарда с нарушенной сократительной способностью, а также многие сопутствующие нарушения.
- Сцинтиграфия миокарда — позволяет выявить участки миокарда с нарушенным кровообращением, для чего используются специальные радионуклиды.
- Нагрузочные тесты (тредмил-тест, велоэргометрия) — процедуры позволяют оценить изменения на ЭКГ, свидетельствующие об ишемии миокарда, во время физической нагрузки.
Также исследуют образцы крови, обращая внимание на:
- Липидограмму — определение холестерина и соотношения липидов в крови для выявления предрасположенности к ИБС.
- Глюкозу крови — для исключения сахарного диабета.
- Определение уровня эритроцитов и гемоглобина — для исключения железодефицитной анемии.
- Биохимические маркеры — исследование уровней различных ферментов, которые могут свидетельствовать в пользу инфаркта.
Важно: повышенный уровень холестерина в крови может значительно увеличить риск появления атеросклеротических бляшек. Как раз они могут стать одной из причин коронарной недостаточности. Холестерин может быть слишком высоким из-за поступления большого количества липопротеинов низкой (ЛПНП) и малого поступления липопротеинов высокой плотности (ЛПВП). Врач-диетолог поможет скорректировать рацион так, чтобы «хороших», низкой плотности поступало больше, чем «плохих».
Группа риска по развитию сердечной коронарной недостаточности
Наиболее часто сердечная коронарная недостаточность диагностируется у людей:
- с наследственной предрасположенностью;
- с ожирением;
- которые много курят;
- у которых повышен уровень холестерина в крови;
- болеющих сахарным диабетом;
- занимающихся сидячей работой, ведущих малоподвижный образ жизни;
- болеющих артериальной гипертензией.
При сочетании нескольких факторов риска вероятность образования тромбов значительно повышается. Это значит, что исключить на 100% в будущем у больного наступление внезапной коронарной смерти нельзя.
Лечение
При назначении лечения в первую очередь рекомендуют гипохолестериновую диету, умеренную регулярную физическую активность и снижение массы тела. При наличии вредных привычек необходимо от них избавиться. Это называется модификацией образа жизни. Не стоит недооценивать пользу таких рекомендаций, в данном случае они во многом определяют успех лечения и предупреждения будущих осложнений.
Источник: Michal Jarmoluk from Pixabay
Патогенез
Механизм формирования недостаточности коронарных сосудов определяется взаимодействием ряда факторов:
- наличие атеросклеротической бляшки;
- спазм коронарных артерий;
- внекоронарный тромбоз.
Доподлинно известно, что появление атеросклеротической бляшки является морфологической основой ишемического повреждения миокарда в 90% случаев. Выраженные приступы стенокардии возникают при поражении коронарных сосудов на 70-80%. При спазме артерии происходит сокращение гладкомышечной сосудистой стенки, что создаёт препятствие нормальному кровотоку в миокарде. На спазм коронарной артерии оказывает влияние симпатическая нервная система.
Важнейшее значение имеет тромбоз венечных сосудов. Тромбы формируются в основном на поверхности атеросклеротической бляшки в месте нарушения целостности и структуры эндотелиального слоя в виде деструкции и изъязвления бляшки.
Медикаментозное лечение
Медикаментозное лечение включает несколько групп препаратов:
- Бета-блокаторы и антагонисты кальция — эти две группы снижают потребление миокардом кислорода и способствуют расширению коронарных сосудов. Также эти препараты эффективны и при частых сопутствующих состояниях (гипертонической болезни и аритмиях).
- Статины — препараты, способствующие нормализации липидного спектра крови. Препятствуют росту атеросклеротических бляшек.
- Антиагрегантные препараты — снижают риск тромбоза коронарных артерий, препятствуя свертыванию крови.
- Нитраты — данная группа препаратов устраняет симптомы приступов стенокардии.
Стадии заболевания
Стадии развития и степень тяжести застойной СН. Из многочисленных признаков СН, перечисляемых при описании той или иной стадии, необходимо выделить немногие, каждый из которых достаточен для определения конкретной стадии. Стадия I: субъективные симптомы СН при умеренных или более значительных нагрузках.
Стадия IIА:
- выраженные субъективные симптомы СН при незначительных нагрузках;
- ортопноэ;
- приступы удушья;
- рентгенографические, в части случаев — и электрокардиографические признаки вторичной легочной гипертензии;
- повторное появление отеков;
- повторное увеличение печени;
- кардиомегалия без других признаков этой стадии;
- мерцательная аритмия без других признаков этой стадии.
Стадия IIБ:
- повторные приступы сердечной астмы;
- постоянные периферические отеки;
- существенные полостные отеки — постоянные или появляющиеся повторно;
- стойкое увеличение печени, которая в ходе лечения может сократиться, но остается увеличенной;
- атриомегалия;
- кардиомегалия в сочетании хотя бы с одним из признаков предыдущей стадии;
- мерцательная аритмия в сочетании хотя бы с одним из признаков предыдущей стадии.
Стадия III, терминальная:
- тяжелые субъективные расстройства при минимальных нагрузках или в покое;
- неоднократные в течение недели эпизоды сердечной астмы;
- дистрофические изменения органов и тканей.
Если имеется хотя бы один достаточный признак более тяжелой стадии, то должна быть установлена именно эта стадия. Приоритет отдается клиническим критериям. Отрицательные результаты инструментальных исследований часто оказываются непоказательными. Такие наиболее очевидные конечные проявления СН, как снижение минутного объема, недостаточное кровоснабжение органов и тканей и недостаточное обеспечение их кислородом могут отсутствовать не только в покое, но и при доступной больному нагрузке. Подобно артериальному давлению соответствующие показатели могут не выходить за широкие пределы вариантов нормы и при тяжелой СН — вплоть до последних дней и часов жизни больного (компенсация на патологическом уровне).
Хирургическое лечение
К хирургическому лечению прибегают, когда уровень нарушения кровотока в коронарных артериях становится критическим и медикаментозно его компенсировать невозможно. В данном случае речь идет о двух операциях: аорто-коронарное шунтирование (АКШ) и стентирование коронарных артерий.
Аорто-коронарное шунтирование — операция открытого типа, при которой доступ к сердцу осуществляется через вскрытие грудной клетки. Суть состоит в возобновлении кровотока в венечной артерии после места сужения. Осуществляется это за счет соединения пораженной артерии и здорового крупного сосуда посредством другого сосуда, образуя некий «обходной мостик» для течения крови. Необходимый соединительный сосуд (шунт) могут взять с голени, предплечья и других мест.
Важно знать, что реабилитационный период продолжителен из-за долгого срастания грудины. Хоть операция и сложная, в России она практикуется давно и, как правило, проходит благоприятно.
Стентирование коронарных артерий — малоинвазивная операция, при которой суженный участок коронарной артерии расширяют изнутри с помощью специальной металлической сетки. Доступ к сердцу осуществляется чаще всего через бедренную артерию ноги. Данное оперативное вмешательство проходит легко и практически не имеет реабилитационного периода.
Диагностика и лечение острого коронарного синдрома: от понимания принципов к реализации стандартов
Определение
Согласно определению, приведенному в руководстве Американской коллегии кардиологов и Американской ассоциации сердца 2000 г., понятие «острый коронарный синдром» включает любые группы симптомов, позволяющие подозревать острый инфаркт миокарда (ИМ) или нестабильную стенокардию (НС). К основным клиническим вариантам ОКС относятся:
- ИМ с подъемом сегмента ST;
- ИМ без подъема сегмента ST;
- ИМ, диагностированный по изменениям ферментов или биомаркерам;
- ИМ, диагностированный по поздним ЭКГ–признакам;
- НС.
Следует подчеркнуть, что диагноз ОКС является временным, «рабочим» и используется для выделения категории больных с высокой вероятностью ИМ или НС при первом контакте с ними. Лечение больных с ОКС начинают до получения информации, необходимой и достаточной для уверенной постановки нозологического диагноза. После идентификации какого–либо из перечисленных выше клинических состояний на основе результатов диагностических тестов производится коррекция терапии.
Патогенез
Ведущим патогенетическим механизмом ОКС является тромбоз пораженной атеросклерозом коронарной артерии
. Тромб образуется в месте разрыва атеросклеротической бляшки. Вероятность разрыва бляшки зависит от ее расположения, размера, консистенции и состава липидного ядра, прочности фиброзной капсулы, а также выраженности местной воспалительной реакции и напряжения стенки сосуда. Непосредственными причинами повреждения оболочки бляшки являются механическое воздействие кровотока и ослабление фиброзной капсулы под влиянием протеолитических ферментов, выделяемых макрофагами. Содержимое бляшки характеризуется высокой тромбогенностью – его воздействие на кровь приводит к изменению функциональных свойств тромбоцитов и запуску коагуляционного каскада. Определенную роль в развитии ОКС играет спазм коронарной артерии в месте расположения поврежденной бляшки. В случаях, когда нарушение проходимости коронарной артерии вызывается ее спазмом и/или формированием тромбоцитарного агрегата (то есть является обратимым), развивается клиническая картина НС. Образование красного тромба, не полностью перекрывающего просвет сосуда, ведет к развитию ИМ без зубца Q. При полной тромботической окклюзии коронарной артерии формируется ИМ с зубцом Q.
Диагностика
Распознавание ОКС базируется на трех группах критериев. Первую группу составляют признаки, определяемые при расспросе и физикальном исследовании больного, вторую группу – данные инструментальных исследований и третью – результаты лабораторных тестов.
Типичными клиническими проявлениями ОКС являются ангинозная боль
в покое продолжительностью более 20 мин, впервые возникшая стенокардия III функционального класса, прогрессирующая стенокардия. К атипичным проявлениям ОКС относят разнохарактерные болевые ощущения в грудной клетке, возникающие в покое, боль в эпигастрии, острые расстройства пищеварения, боль, характерную для поражения плевры, нарастающую одышку. Физикальное исследование больных с ОКС нередко не выявляет каких–либо отклонений от нормы. Его результаты важны не столько для диагностики ОКС, сколько для обнаружения признаков возможных осложнений ишемии миокарда, выявления заболеваний сердца неишемической природы и определения экстракардиальных причин жалоб больного.
Основным методом инструментальной диагностики ОКС является электрокардиография
. ЭКГ больного с подозрением на ОКС, по возможности, следует сопоставлять с данными предыдущих исследований. При наличии соответствующей симптоматики для НС характерны депрессия сегмента ST не менее чем на 1 мм в двух и более смежных отведениях, а также инверсия зубца T глубиной более 1 мм в отведениях с преобладающим зубцом R. Для развивающегося ИМ c зубцом Q характерна стойкая элевация сегмента ST, для стенокардии Принцметала и развивающегося ИМ без зубца Q – преходящий подъем сегмента ST (рис. 1). Помимо обычной ЭКГ в покое, для диагностики ОКС и контроля эффективности лечения применяется холтеровское мониторирование электрокардиосигнала.
Рис. 1. Варианты ОКС в зависимости от изменений ЭКГ
Из биохимических тестов, применяемых для диагностики ОКС, предпочтительным считается
определение содержания в крови сердечных тропонинов T и I
, повышение которого представляет собой наиболее надежный критерий некроза миокарда. Менее специфичным, но более доступным для определения в клинической практике критерием является повышение в крови уровня креатинфосфокиназы (КФК) за счет ее изофермента МВ–КФК. Увеличение содержания МВ–КФК (предпочтительно массы, а не активности) в крови более чем вдвое по сравнению с верхней границей нормальных значений при наличии характерных жалоб, изменений ЭКГ и отсутствии других причин гиперферментемии позволяет с уверенностью диагностировать ИМ. Повышение уровня МВ–КФК и сердечных тропонинов регистрируется через 4–6 часов от начала формирования очага некроза миокарда.
Наиболее ранним биомаркером ИМ является миоглобин
– его содержание в крови повышается спустя 3–4 часа после развития ИМ. Для исключения или подтверждения диагноза ИМ рекомендуются повторные анализы крови в течение 6–12 часов после любого эпизода сильной боли в грудной клетке. Перечисленные тесты приобретают особенно важное значение при дифференциальной диагностике ИМ без зубца Q и НС.
Традиционные биомаркеры некроза миокарда, такие как аспарагиновая аминотрансфераза, лактатдегидрогеназа и даже общая КФК, в связи с недостаточной чувствительностью и специфичностью не рекомендуются для диагностики ОКС. В условиях практического здравоохранения средства, затрачиваемые на приобретение реактивов для их определения, целесообразно направить на внедрение рекомендованных диагностических тестов.
Оценка риска
В течение первых 8–12 часов после появления клинической симптоматики ОКС необходимо обеспечить сбор диагностической информации в объеме, достаточном для стратификации риска. Определение степени непосредственного риска смерти или развития ИМ принципиально важно для выбора лечебной тактики в отношении больного с ОКС без стойкого подъема сегмента ST.
К критериям высокого непосредственного риска смерти и развития ИМ относятся:
повторные эпизоды ишемии миокарда (повторяющиеся ангинозные приступы в сочетании и без сочетания с преходящей депрессией или подъемом сегмента ST); повышение содержания сердечных тропонинов (при невозможности определения – МВ–КФК) в крови; гемодинамическая нестабильность (артериальная гипотензия, застойная сердечная недостаточность); пароксизмальные желудочковые нарушения ритма сердца (желудочковая тахикардия, фибрилляция желудочков); ранняя постинфарктная стенокардия.
Признаками низкого непосредственного риска смерти и развития ИМ являются:
отсутствие повторных приступов боли в грудной клетке; отсутствие депрессии или подъема сегмента ST – изменения только зубца Т (инверсия, уменьшение амплитуды) или нормальная ЭКГ; отсутствие повышения содержания сердечных тропонинов (при невозможности их определения – МВ–КФК) в крови.
С целью подтверждения диагноза ИБС и оценки отдаленного прогноза у больных с низким непосредственным риском развития ИМ и смерти спустя 3–5 дней после эпизода с симптоматикой ОКС рекомендуется выполнение стресс–теста
. У больных с высоким непосредственным риском развития ИМ и смерти проведение стресс–теста для оценки прогноза и определения лечебной тактики считается возможным не ранее чем через 5–7 дней после стойкой стабилизации состояния. При подозрении на безболевую ишемию миокарда проведению стресс–теста должно предшествовать холтеровское мониторирование ЭКГ. Стандартный нагрузочный тест подразумевает регистрацию ЭКГ во время физической нагрузки на велоэргометре или тредмиле. У ряда больных тест с физической нагрузкой может быть недостаточно информативен. В этих случаях возможно выполнение
стресс–эхокардиографии с физической нагрузкой
. Фармакологические стресс–тесты с применением эхокардиографии или сцинтиграфии миокарда показаны пациентам, у которых имеются ограничения физической активности.
К критериям высокого риска неблагоприятного исхода, определяемым по результатам стресс–тестов, относятся: развитие ишемии миокарда при низкой толерантности к физической нагрузке; обширный стресс–индуцированный дефект перфузии; множественные стресс–индуцированные дефекты перфузии небольшого размера; выраженная дисфункция левого желудочка (фракция выброса менее 35%) в покое или при нагрузке; стабильный или стресс–индуцированный дефект перфузии в сочетании с дилатацией левого желудочка.
Пациентам, отнесенным к категории высокого риска по клиническим признакам, данным инструментальных и лабораторных тестов, а также больным с НС, перенесшим ранее коронарную баллонную ангиопластику (КБА) или коронарное шунтирование (КШ), показана коронарография
. На результатах последней основывается выбор дальнейшей тактики лечения больного – в частности, оценка целесообразности выполнения и определение вида операции реваскуляризации миокарда. Больным с упорно рецидивирующим болевым синдромом и выраженной гемодинамической нестабильностью коронарографическое исследование рекомендуется проводить в максимально сжатые сроки после появления клинической симптоматики ОКС без предварительного проведения стресс–тестов.
Медикаментозное лечение
С учетом представлений о механизмах развития главным направлением патогенетической терапии ОКС следует считать воздействие на систему свертывания крови
. К средствам, влияющим на процесс тромбообразования, относятся три группы лекарственных препаратов: тромболитики, антикоагулянты и антиагреганты.
Тромболитическая терапия (ТЛТ)
Показанием к ТЛТ является ангинозная боль длительностью более 30 мин, сохраняющаяся несмотря на прием нитроглицерина, в сочетании с элевацией на 1 мм и более сегмента ST не менее чем в 2–х смежных отведениях ЭКГ или появлением полной блокады левой ножки пучка Гиса. Анализ результатов плацебо–контролируемых исследований (GISSI–1, ISIS–2, ASSET, LATE) показал, что ТЛТ, выполненная в первые 6 часов после появления клинической симптоматики развивающегося ИМ, уменьшает смертность в течение первого месяца после развития ИМ в среднем на 30%. Проведение ТЛТ в сроки 6–12 часов от момента возникновения ангинозной боли уменьшает смертность в среднем на 20% и считается допустимым при наличии клинических и ЭКГ признаков расширения зоны некроза миокарда. ТЛТ, выполненная позже 12 часов от момента развития ИМ, позитивного влияния на смертность не оказывает. При отсутствии стойкой элевации сегмента ST, которая рассматривается как признак закупорки коронарной артерии фибринсодержащим тромбом, применение ТЛТ также нецелесообразно.
Абсолютными противопоказаниями к ТЛТ являются геморрагический инсульт в анамнезе, ишемический инсульт или динамическое нарушение мозгового кровообращения в течение последнего года, внутричерепная опухоль, активное внутреннее кровотечение, расслаивающая аневризма аорты.
Исследование GUSTO
доказало, что ускоренный режим введения
альтеплазы
является наилучшей стратегией тромболитической терапии в настоящий момент для пациентов с ИМ.
Схема ускоренного введения альтеплазы (100 мг) при ИМ в течение 6 часов от начала развития симптомов при массе тела более 65 кг следующая: 15 мг альтеплазы болюсно в течение 1-2 мин., затем инфузионно внутривенно 50 мг в течение 30 мин. и затем 35 мг в течение 60 мин. До начала внутривенное введение гепарина 5000 МЕ + внутривенная инфузия гепарина 1000 МЕ/ч в последующие двое суток.
Антикоагулянты
Из соединений, относящихся к данной фармакологической группе, в лечении больных с ОКС применяется главным образом нефракционированный гепарин
(НФГ). В отличие от тромболитических средств НФГ вводится не только больным со стойкой элевацией сегмента ST, но и пациентам с другими вариантами ОКС. Основными противопоказаниями к гепаринотерапии являются активное кровотечение и заболевания, сопровождающиеся высоким риском его возникновения.
Схема введения НФГ больным с ОКС без стойкого подъема сегмента ST: внутривенно – болюс 60–80 ЕД/кг (но не более 5000 ЕД), затем инфузия 12–18 ЕД/кг/ч (но не более 1250 ЕД/кг/ч) в течение 48 часов. Оптимальная скорость введения гепарина определяется по величине активированного частичного тромбопластинового времени (АЧТВ). Использование с этой целью времени свертывания крови не рекомендуется. Условием результативности гепаринотерапии считается увеличение АЧТВ в 1,5–2,5 раза по сравнению с нормальным значением этого показателя для лаборатории данного лечебного учреждения. АЧТВ рекомендуется определять через 6 часов после начала инфузии и затем – через 6 часов после каждого изменения скорости введения гепарина. Если при двух последовательных определениях АЧТВ сохраняется в желаемых пределах, следующий анализ может быть выполнен через 24 часа. Определение АЧТВ перед началом гепаринотерапии необязательно.
В случаях ОКС со стойким подъемом сегмента ST при отсутствии противопоказаний гепарин показан всем больным, не получавшим ТЛТ, а также больным, у которых планируется проведение реваскуляризации миокарда. НФГ рекомендуется вводить подкожно по 7500–12500 ЕД 2 раза в день или внутривенно. Рекомендуемая продолжительность терапии гепарином при его подкожном введении составляет 3–7 дней. Внутривенный путь введения НФГ является предпочтительным для больных с повышенным риском тромбоэмболических осложнений (обширный ИМ, передняя локализация ИМ, мерцательная аритмия, тромбоэмболии в анамнезе, документированный тромб в левом желудочке).
Целесообразность применения НФГ в сочетании с ТЛТ оспаривается. Согласно современным представлениям, если тромболизис проводится неспецифичными фибринолитическими препаратами (стрептокиназа, анистреплаза, урокиназа) на фоне применения ацетилсалициловой кислоты в полной дозе, введение гепарина необязательно. При применении альтеплазы внутривенное введение гепарина считается оправданным. Гепарин вводится внутривенно болюсом 60 ЕД/кг (но не более 4000 ЕД), затем – со скоростью 12 ЕД/кг/ч (но не более 1000 ЕД/кг/ч) в течение 48 часов под контролем АЧТВ, которое должно превышать контрольный уровень в 1,5–2 раза. Начинать гепаринотерапию рекомендуется одновременно с введением альтеплазы. Наличие критериев высокого риска развития тромбоэмболических осложнений рассматривается, как показание к гепаринотерапии больных, которым проводился тромболизис, вне зависимости от вида тромболитического препарата.
Низкомолекулярные гепарины (эноксапарин, фраксипарин) обладают рядом преимуществ по сравнению с НФГ: эти препараты имеют большую продолжительность действия и более предсказуемый антикоагулянтный эффект, вводятся подкожно в фиксированной дозе, не требуя применения инфузионного насоса и лабораторного контроля. Результаты исследований FRIC
,
FRAXIS
,
TIMI 11B
показали, что низкомолекулярные гепарины обладают не меньшей, но и не большей, чем НФГ, способностью снижать риск развития ИМ и смерти у больных с НС и ИМ без зубца Q. Лишь эноксапарин, по данным исследования
ESSENCE
, сильнее, чем НФГ, уменьшал риск развития суммы «коронарных событий» (смерть, ИМ, рецидив стенокардии) и частоту экстренных операций реваскуляризации миокарда. Объединенные результаты исследований ESSENCE и TIMI 11B подтвердили клинические преимущества эноксапарина перед НФГ. Длительность лечения больных ОКС низкомолекулярными гепаринами в среднем составляет 5–7 суток. Исследования FRIC, FRAXIS и TIMI 11B показали, что более продолжительное их применение не приводит к дополнительному снижению частоты «коронарных событий», но увеличивает риск кровотечений. Вместе с тем результаты, полученные в исследованиях TIMI 11B и FRISC II, позволяют предполагать, что увеличение длительности гепаринотерапии может оказаться полезным для пациентов, готовящихся к операции реваскуляризации миокарда.
Стоимость низкомолекулярных гепаринов превосходит стоимость НФГ. Вместе с тем их эффективное клиническое применение не требует дорогостоящего инструментального и лабораторного обеспечения. Если медицинское учреждение не располагает необходимыми материально–техническими ресурсами и не способно обеспечить введение НФГ в соответствии с изложенными выше требованиями, для лечения больных с ОКС рекомендуется использовать низкомолекулярные гепарины.
В последние годы было выполнено 4 крупных исследования (OASIS–2, ASPECT, APRICOT–2, WARIS), результаты которых дают основание полагать, что прогноз больных, перенесших ОКС, может быть существенно улучшен за счет включения в состав комплексной терапии непрямого антикоагулянта варфарина. Продолжительное (от 3 месяцев до 4 лет) применение варфарина (в дополнение к ацетилсалициловой кислоте) способствовало снижению частоты реокклюзий инфаркт–зависимой коронарной артерии у больных ИМ после успешной ТЛТ, уменьшению риска развития ИМ, мозгового инсульта и смерти без достоверного увеличения частоты геморрагических осложнений. Однако широкое применение варфарина во вторичной профилактике ИБС ограничивается необходимостью регулярного контроля антикоагуляционного эффекта по величине международного нормализованного отношения.
Антиагреганты
Наиболее широко используемым в клинической практике антиагрегантом является ацетилсалициловая кислота. Препарат показан при всех вариантах ОКС. Его применение отчетливо снижает риск смерти и развития ИМ. Так, по данным исследования ISIS II, в течение 35 суток после развития ИМ по сравнению с группой больных, получавших плацебо, летальность при лечении только ацетилсалициловой кислотой снижалась на 23%, только стрептокиназой – на 25% и ацетилсалициловой кислотой в сочетании со стрептокиназой – на 42%. Минимальная доза ацетилсалициловой кислоты, обеспечивающая уменьшение риска развития смерти и ИМ у больных с НС, составляет 75 мг/сут.
Среди противопоказаний к применению ацетилсалициловой кислоты в клинической практике чаще всего встречаются обострение язвенной болезни, геморрагические диатезы и повышенная чувствительность к салицилатам. В случаях непереносимости ацетилсалициловой кислоты рекомендуется применение препаратов из группы тиенопиридинов (тиклопидин, клопидогрель). Их основным недостатком является медленное развитие антиагрегационного эффекта. При ОКС с целью ускорения развития лекарственного воздействия в первые двое суток терапии допускается увеличение дозы тиклопидина до 1000 мг/сут с последующим переходом на прием стандартной дозы 500 мг/сут. В случаях индивидуальной непереносимости или развития побочных эффектов (аллергические реакции, желудочно–кишечные расстройства, нейтропения) тиклопидин может быть заменен на клопидогрель – 300 мг однократно, затем по 75 мг/сут.
Весьма перспективной считается концепция комбинированной антиагрегационной терапии, то есть одновременного блокирующего воздействия на различные пути активации тромбоцитов. В исследовании CURE
было показано, что лечение больных, перенесших ОКС без подъема сегмента ST, комбинацией ацетилсалициловой кислоты и клопидогреля по сравнению с терапией только ацетилсалициловой кислотой приводит к достоверно более выраженному снижению риска развития сердечно–сосудистых событий при отсутствии разницы по количеству жизнеугрожающих кровотечений.
Наиболее сильным антиагрегационным эффектом обладают блокаторы IIb/IIIa рецепторов тромбоцитов
(абциксимаб, эптифибатид, тирофибан, ламифибан), которые способны блокировать агрегацию тромбоцитов, вызываемую любым физиологическим индуктором. По данным многочисленных исследований (EPILOG, EPISTENT, EPIC, CAPTURE, PRISM–PLUS, PURSUIT, PARAGON и др.), внутривенное введение этих препаратов больным с ОКС без подъема сегмента ST в дополнение к ацетилсалициловой кислоте и НФГ значимо улучшало результаты КБА как в сочетании, так и без сочетания с установкой стента. Абциксимаб был эффективен только у больных, которым проводилась реваскуляризация миокарда, тирофибан и эптифибатид – как при проведении реваскуляризации, так и при медикаментозном лечении. Дополнительное снижение числа неблагоприятных исходов было особенно выраженным при добавлении антагонистов гликопротеиновых рецепторов IIb/IIIa к стандартному антитромботическому лечению у больных с повышенным уровнем сердечных тропонинов. В то же время длительное применение этих препаратов внутрь, по данным исследований OPUS–TIMI и SYMPHONY, не оказывало положительного влияния на результаты лечения больных с ОКС. Основным показанием к применению антагонистов гликопротеиновых рецепторов IIb/IIIa у больных с ОКС является отсутствие стойкого подъема сегмента ST в сочетании с высоким непосредственным риском смерти или развития ИМ при запланированном проведении процедуры реваскуляризации миокарда в ближайшие 24 часа.
Рекомендуемые дозы антагонистов гликопротеиновых рецепторов IIb/IIIa: абциксимаб – внутривенно болюс 0,25 мг/кг с последующей инфузией 0,125 мкг/кг/мин в течение 12–24 часов; эптифибатид – внутривенно болюс 180 мг/кг c последующей инфузией 2,0 мкг/кг/мин в течение 72–96 часов; тирофибан – внутривенная инфузия 0,4 мкг/кг/мин в течение получаса, затем 0,1 мкг/кг/мин в течение 48–96 часов.
Нитраты
На начальном этапе лечения больных с ОКС препараты нитроглицерина и изосорбида–динитрата применяются внутривенно. Начальная скорость инфузии составляет 10 мкг/мин. Каждые 3–5 мин скорость введения увеличивают на 10 мкг/мин. Выбор скорости инфузии и темпа ее увеличения определяется изменениями выраженности болевого синдрома и уровня артериального давления (АД). Не рекомендуется снижать систолическое АД более чем на 15% от исходного при нормотензии и на 25% при гипертензии. При достижении желаемого эффекта скорость инфузии стабилизируется, а затем постепенно снижается. В случае избыточного снижения АД продолжительность введения препаратов на каждой ступени дозирования и интервалы между ними увеличиваются. Помимо снижения АД, к наиболее частым побочным эффектам, препятствующим проведению эффективной антиангинальной терапии, относится головная боль. После завершения внутривенного введения препараты органических нитратов (предпочтительно производные изосорбида–динитрата или изосорбида–5–мононитрата) назначаются внутрь по асимметричной схеме с обеспечением «безнитратного» интервала.
b–адреноблокаторы
Препараты этой группы рекомендуется применять у всех больных с ОКС при отсутствии противопоказаний, к которым относятся бронхиальная астма, тяжелая обструктивная дыхательная недостаточность, брадикардия в покое менее 50 ударов в минуту, синдром слабости синусового узла, атриовентрикулярная блокада II–III степени, хроническая сердечная недостаточность IV функционального класса, выраженная артериальная гипотензия. Начинать лечение предпочтительно с внутривенного введения b–адреноблокаторов при постоянном мониторировании ЭКГ
. После внутривенной инфузии рекомендуется продолжить лечение b–адреноблокаторами путем приема внутрь. По данным мета–анализа выполненных к настоящему времени исследований, продолжительное лечение b–адреноблокаторами больных, перенесших ИМ с зубцом Q, позволяет уменьшить смертность на 20%, риск внезапной смерти на 34% и частоту нефатального ИМ на 27%. Наиболее эффективными и безопасными считаются b1–селективные соединения без собственной симпатомиметической активности.
Схемы применения: пропранолол
– внутривенно медленно 0,5–1,0 мг, затем внутрь по 40–80 мг каждые 6 часов;
метопролол
– внутривенно 5 мг за 1–2 мин трижды с интервалами между инъекциями по 5 мин, затем (через 15 минут после последней инъекции) внутрь по 25–50 мг каждые 6 часов;
атенолол
– внутривенно 5 мг за 1–2 мин дважды с интервалом между инъекциями 5 мин, затем (через 1–3 часа после последней инъекции) внутрь по 50–100 мг 1–2 раза в день. Индивидуальная доза b–адреноблокаторов подбирается с учетом частоты сердечных сокращений, целевое значение которой составляет 50–60 ударов в мин.
Антагонисты кальция
Производные дигидропиридина, бензодиазепина и фенилалкиламина, наиболее широко применяемыми представителями которых являются препараты первого поколения – соответственно нифедипин, дилтиазем и верапамил, различаются по выраженности вазодилатирующего действия, отрицательного инотропного и отрицательного дромотропного эффектов. Мета–анализы результатов рандомизированных исследований выявили дозозависимое негативное влияние нифедипина короткого действия на риск смерти больных с НС и ИМ. В связи с этим короткодействующие производные дигидропиридина не рекомендуются для лечения больных с ОКС. В то же время, по данным некоторых исследований, продолжительное применение дилтиазема (MDPIT, DRS) и верапамила (DAVIT II) препятствует развитию повторного ИМ и смерти у больных, перенесших ИМ без зубца Q. У больных с ОКС дилтиазем и верапамил применяются в случаях, когда имеются противопоказания к применению b–адреноблокаторов (например, обструктивный бронхит), но при отсутствии дисфункции левого желудочка и нарушений атриовентрикулярной проводимости. Рекомендуемые дозы препаратов составляют 180–360 мг/сут.
Ингибиторы ангиотензинпревращающего фермента
Положительное влияние ингибиторов ангиотензинпревращающего фермента (АПФ) на выживаемость больных, перенесших ИМ (в особенности осложненный застойной сердечной недостаточностью), доказана в ряде контролируемых исследований – GISSI–3
,
ISIS–4
,
AIRE
,
SAVE
,
TRACE
и др. Обширный ИМ с патологическим зубцом Q является показанием к применению ингибиторов АПФ даже при отсутствии клинических и эхокардиографических признаков дисфункции левого желудочка. Чем раньше начинается лечение ингибиторами АПФ, тем сильнее выражено их тормозящее влияние на процесс постинфарктного ремоделирования сердца. С другой стороны, как показали результаты исследования CONSENSUS II, которое было прервано досрочно в связи с тем, что смертность в группе больных, получавших эналаприл, превысила смертность больных контрольной группы, ингибиторы АПФ должны применяться в терапии больных ИМ с большой осторожностью. По возможности, терапию следует начинать после стабилизации гемодинамики в первые 48 часов от момента развития ИМ. Рекомендуются следующие начальные дозы препаратов: каптоприл – 25 мг/сут, эналаприл и лизиноприл – 2,5 мг/сут, периндоприл – 2 мг/сут. Увеличение дозы должно проводиться постепенно под контролем АД и функции почек. При достижении оптимальной дозы терапия должна продолжаться в течение многих лет.
Немедикаментозное лечение
КБА или КШ выполняются больным с рецидивирующей ишемией миокарда для предотвращения ИМ и смерти. Выбор метода реваскуляризации миокарда зависит от степени, протяженности и локализации стеноза коронарной артерии, количества пораженных сосудов, которые определяются по результатам ангиографии. Операция АКШ при НС и в остром периоде ИМ сопряжена с повышенным риском операционной летальности. Данная методика реваскуляризации миокарда оправдана при поражении ствола левой коронарной артерии или многососудистом поражении. У больным с поражением одного, реже двух сосудов реваскуляризация миокарда обычно достигается путем КБА.
Как указывалось выше, улучшение результатов КБА, а также процедуры стентирования коронарной артерии (исследование EPISTENT) может быть достигнуто с помощью блокаторов IIb/IIIa рецепторов. КБА все более широко применяется при лечении больных с элевацией сегмента ST вместо ТЛТ. Это позволяет не только получить дополнительное снижение больничной летальности, но и значительно уменьшить риск осложнений, обусловленных медикаментозным воздействием на свертывающую систему крови.
Тактика медицинской помощи больным с ОКС
Объем инструментальных и лабораторных исследований, а также выбор методов медикаментозного и немедикаментоного лечения больного с симптоматикой ОКС определяется условиями оказания медицинской помощи и возможностями конкретного медицинского учреждения. Предварительный диагноз устанавливается на основании жалоб больного. Следует подчеркнуть, что отсутствие патологических изменений на ЭКГ не исключает ОКС. При подозрении на связь болей в грудной клетке с острой коронарной недостаточностью больной должен быть срочно госпитализирован – по возможности, в специализированное отделение (палату) интенсивного наблюдения и терапии, где выполняются необходимые диагностические исследования.
Алгоритм медицинской помощи больным с ОКС представлен на рисунке 2. Первыми медикаментозными средствами, которые следует применить при подозрении на ОКС, являются ацетилсалициловая кислота – 325 мг внутрь (для ускорения всасывания таблетку следует разжевать) и нитроглицерин – 0,5 мг под язык (при необходимости возможен прием до 3 таблеток с интервалом 5 мин). Больные со стойкой элевацией сегмента ST или появлением блокады левой ножки пучка Гиса получают ТЛТ или подвергаются первичной КБА. Больные с депрессией сегмента ST, инверсией зубца Т или отсутствием изменений ЭКГ получают гепаринотерапию, b–адреноблокаторы, при сохранении болевого синдрома – нитраты внутривенно. В случаях непереносимости b–адреноблокаторов или наличии противопоказаний к их применению назначаются антагонисты кальция. Всем больным обеспечивается многоканальное мониторирование ЭКГ. После получения дополнительной информации (результаты клинического наблюдения, данные ЭКГ в динамике, анализ содержания сердечных тропонинов, КФК и МВ–КФК в крови) проводятся уточнение диагноза и оценка риска негативного развития событий, на основании чего принимаются дальнейшие тактические решения. Больным, у которых развился ИМ, но в остром периоде не была выполнена КБА, перед выпиской из стационара проводится проба с физической нагрузкой для определения прогноза и показаний к хирургическому лечению.
Рис. 2. Алгоритм медицинской помощи больным с ОКС
Больным с высоким непосредственным риском развития ИМ и смерти, при возможности, следует начать введение блокаторов IIb/IIIa рецепторов, выполнить коронарографию, КБА и продолжить терапию блокаторами IIb/IIIa рецепторов. В случаях, когда введение препаратов данной группы и выполнение процедуры реваскуляризации миокарда невозможно, осуществляется гепаринотерапия (НФГ или низкомолекулярные гепарины) в сочетании с ацетилсалициловой кислотой, b–адреноблокаторами и при необходимости нитратами внутривенно. После стабилизации состояния данной категории больных показано проведение пробы с физической нагрузкой для определения прогноза и показаний к КБА или КШ. Лечение больных с низким риском развития ИМ и смерти включает прием внутрь ацетилсалициловой кислоты, b–адреноблокаторов или антагонистов кальция и нитратов. При отсутствии изменений ЭКГ и повышения содержания в крови биохимических маркеров некроза миокарда по результатам двух определений введение НФГ или низкомолекулярных гепаринов может быть прекращено. Спустя 5–7 дней больным данной категории показано выполнение пробы с физической нагрузкой для уточнения диагноза ИБС, прогноза и дальнейшей тактики лечения.
Большая часть неблагоприятных событий приходится на первые месяцы после развития ОКС. В лечении больных, перенесших ОКС, помимо средств непосредственного воздействия на коронарное кровообращение, необходимо проведение мероприятий, направленных на ослабление действия модифицируемых факторов риска прогрессирования ИБС. Больные должны прекратить курение. В случаях, когда применение b–адреноблокаторов или антагонистов кальция и ингибиторов АПФ в средне–терапевтических дозах не позволяет скорректировать повышенное АД, следует увеличить дозы применяемых препаратов или назначить дополнительно антигипертензивные лекарственные средства. Больные должны соблюдать гиполипидемическую диету. Статины, согласно современным представлениям, показаны больным, перенесшим ОКС, даже при отсутствии повышения содержания в крови холестерина атерогенных липопротеидов низкой плотности. Все более веские подтверждения получает идея применения статинов с первых суток заболевания.
Показатели летальности при ОКС в России в 2–3 раза выше, чем в странах Западной Европы и Северной Америки. Главной причиной этого различия является неполноценное применение в отечественной клинической практике эффективных методов диагностики и лечения ОКС. К сожалению, многие учреждения здравоохранения современной России не располагают возможностями обеспечить выполнение рекомендаций по медицинской помощи больным с ОКС. Однако наряду с объективными трудностями (прежде всего, финансового характера) к причинам этого следует отнести и недостаточную профессиональную осведомленность врачей. Именно недостаточность профессиональных знаний является предпосылкой нерационального использования финансовых средств, выделяемых для оказания медицинской помощи больным с ОКС, значительная часть которых в настоящее время расходуется на обеспечение малоинформативных диагностических методик и приобретение малоэффективных лекарственных препаратов. Принятие врачами основных положений рекомендаций по диагностике и лечению ОКС является важнейшим условием их успешного внедрения в клиническую практику, а реализация согласованных стандартов представляет собой доказанную возможность существенного улучшения результатов медицинской помощи.
Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова
Литература:
1. ACC/AHA guidelines for the management of patients with acute myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on Management of Acute Myocardial Infarction). J Am Coll Cardiol 1996;28:1328–1428.
2. Update: ACC/AHA guidelines for the management of patients with acute myocardial infarction: executive summary and recommendations: a report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on Management of Acute Myocardial Infarction). Circulation 1999;100:1016–1030.
3. ACC/AHA guidelines for the management of patients with unstable angina and non–ST–segment elevation myocardial infarction. A report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on the Management of Patients with Unstable Angina). J Am Coll Cardiol 2000;36:970–1062.
4. Management of acute coronary syndromes: acute coronary syndromes without persistent ST segment elevation. Recommendations of the Task Force of the European Society of Cardiology. Eur Heart J 2000;21:1406–1432.
5. Лечение острого коронарного синдрома без стойких подъемов сегмента ST на ЭКГ. Российские рекомендации. Разработаны Комитетом эксрпертов Всероссийского научного общества кардиологов. М 2001;23.
Профилактика
Профилактика коронарной недостаточности сводится в сущности к предупреждению развития атеросклероза, избеганию хронических стрессов. Значимость профилактических мер сильно возрастает с возрастом. Вот что можно сделать, чтобы значительно снизить риск прогрессирования и развития тяжелых последствий патологии:
- Регулярный анализ крови на липидный спектр, уровень холестерина;
- Снижение потребления количества жирной пищи;
- Регулярные умеренные физические нагрузки — хотя бы 150 минут в неделю;
- Избавление от вредных привычек;
- Своевременное обращение к врачу при появлении соответствующей сердечной симптоматики;
- Минимизация стрессовых ситуаций.
Первая помощь при обострении
При приступе острой формы нужно сразу вызвать скорую помощь. У пациента может остановиться сердце в любую минуту, а возобновить его работу без специализированного оборудования невозможно.
Когда главная задача выполнена – необходимо уделить внимание стабилизации состояния больного. Во время ожидания бригады неотложной помощи, необходимо:
- Обеспечить покой. Больного незамедлительно нужно положить на кровать или диван. Если во время приступа появляется сильная отдышка или кашель, то пациента следует посадить на стул.
- Ликвидировать возможное стеснение грудной клетки. При сердечных приступах на область груди имеют воздействия даже незначительные грузы, в том числе и одежда. Больному необходимо полностью оголить верхнюю часть тала, снять не только вещи, но и украшения (бусы, цепочки, кулоны). По возможности – померить артериальное давление
Обеспечить свежий воздух. При острой коронарной недостаточности в области груди возникает сдавливающее чувство, оно затрудняет дыхание. Открыв все окна, можно увеличить поток и циркуляцию кислорода в помещении. Это облегчит дыхание больного и нагрузку на сердце.- Дать лекарства. Самое распространенное и действенное средство – «Валидол». Он способен уменьшить боль до приезда бригады скорой помощи. Валидол кладут под язык пациенту, и его действие наступает через несколько минут.
«Нитроглицерин» – второй вариант при сердечном приступе. Его тоже необходимо поместить под язык. Действует он быстрее, уже в течение первой минуты. Если боль не уменьшилась или изменения были незначительными, то через 10 минут таблетку необходимо дать повторно. Этот препарат противопоказан при пониженном артериальном давлении.
Причин возникновения коронарной недостаточности много. Ее может спровоцировать как серьезное внутреннее поражение организма, так и внешние факторы. Для поддержания здоровья сердца необходимо заботиться о себе, проводить профилактические мероприятия и отказаться от вредных привычек.
Источники
- Коронарная болезнь сердца — nhlbi.nih.gov.
- Кардиоваскулярная терапия и профилактика, 2016; 15(2): 93–99 https://dx.doi.org/10.15829/1728-8800-2016-2-93-99.
- Курдгелия Т. М., Кислицина О. Н., Базарсадаева Т. С. Внезапная сердечная смерть: эпидемиология, факторы риска и профилактика // БМИК. 2014. №3.
- Руководство по факультетской терапии: учебное пособие / С. А. Болдуева, И. В. Архаров, Е. Л. Беляева, Е. Г. Быкова, Т. В. Ермолова, М. И. Иванова, И. А. Леонова, А. П. Махнов, Н. С. Швец, О. Ю. Чижова; под ред. С. А. Болдуевой. — 3-е изд., доп. и перераб. — СПб.: Изд-во СЗГМУ им. И. И. Мечникова, 2021. — с. 6-32; 64-76.
- Picard F., Sayah N., Spagnoli V., Adjedj J., Varenne O. Vasospastic angina: A literature review of current evidence. //Arch Cardiovasc Dis — 2021 — Vol.112 — №1 — p.44-55
Анализы и диагностика
Важное значение в диагностике острой и хронической сердечной недостаточности играет электрокардиография, которая проводится в покое и в условиях дозированных физических нагрузок. Характерным признаком, указывающим на наличие у пациента патологии с коронарным кровообращением, является регистрация депрессии сегмента ST во время максимальной физической нагрузки либо спустя 2-5 минут после неё. Возникающая во время выполнения нагрузочной пробы аритмия также является косвенным признаком патологии кровообращения сердца.
Оценить состояние венечных сосудов можно посредством проведения коронароангиографии, которая позволяет выявить участки стенотического или окклюзионного поражения сосудов. Суть метода заключается в ведении рентгенконтрастного вещества и последующей оценки проходимости артерий сердца.
Лабораторная диагностика основывается на определении уровня в крови креатининкиназы, глюкозы, электролитов, триглицеридов, АЛТ, АСТ, общего холестерина и лактатдегидрогеназы. Решающее значение отводится определению уровня маркеров поражения миокарда в результате гипоксии и концентрации тропонинов I и T. Выявление высоких концентраций позволяет заподозрить инфаркт миокарда либо иное поражение сердечной мышцы.
Дифференциальная диагностика проводится со следующими заболеваниями:
- эзофагит;
- спазм пищевода;
- язвенное поражение пищеварительного тракта;
- эмболия лёгочной артерии;
- остеохондроз грудного отдела позвоночника;
- остеоартроз плечевого сустава;
- расслоение аорты и др.
Список источников
- Агеев Ф.Т. , Скворцов А.А. , Мареев В.Ю., Беленков Ю.Н. «Сердечная недостаточность на фоне ишемической болезни сердца: некоторые вопросы эпидемиологии, патогенеза и лечения», Регулярные выпуски «РМЖ» №15 от 26.05.2000
- Лупанов В.П. «Алгоритм диагностики и лечения больных с болью в грудной клетке и нормальной коронарной ангиограммой (кардиальным синдромом Х)», статья в журнале «РМЖ»
- Акчурин Р.С., Ширяев А.А., Галяутдинов Д.М. «Показания к операции коронарного шунтирования у больных с различным течением ИБС», Регулярные выпуски «РМЖ» №19 от 03.10.2002