Пролапс клапанов сердца – это заболевание, сопровождающееся нарушением работы клапана, находящегося между желудочком и левым предсердием и являющееся распространённой и относительно неопасной аномалией, во время которой при сокращении сердца проявляется неестественное выпячивание створок клапана.
Клапаном сердца называют состоящие из отдельных элементов подвижные заслонки, перекрывающие отверстия для циркуляции крови из одного отдела сердца в другой. Работа клапанов состоит в том, чтобы управлять кровяными потоками. В сердце размещены четыре клапана – митральный, трёхстворчатый, аортальный и лёгочный, которые пропускают кровь в одном направлении и не дают ей возможность возвращаться обратно. При сокращении сердечной мышцы создаётся давление, и кровь выбрасывается из сердца, а клапаны, регулирующие в этом направлении движение крови в момент сокращения мышцы – раскрываются. После сокращения мышцы давление в сердце падает, клапан закрывается, и кровь не может вернуться в сердце. Среди прочих видов пролапса чаще всего встречается пролапс митрального клапана, причиной которого является врождённая слабость соединительной ткани, из которой состоят сердечные клапаны.
Определение понятия выпадение прямой кишки
Выпадение прямой кишки происходит в результате нарушения фиксации ее со стенками таза при ослаблении мышц тазового дна, что составляет примерно 9 % среди всех заболеваний толстой кишки. Выпадение прямой кишки (ректальный пролапс) — это телескопическое выпячивание прямой кишки через анус; инвагинация — это состояние, при котором телескопическое смещение прямой кишки не выходит за пределы анального канала. Оба этих заболевания приводят к дискомфорту и возникновению незначительной боли (редко) в области промежности. Иногда выпадение прямой кишки сопровождается ишемией и некрозом стенки, при котором требуется экстренная хирургическая ситуация.
Что такое пролапс гениталий
Опущение тазовых органов происходит поэтапно, матка понемногу смещается в сторону выхода из влагалища вместе с прилегающими органами. Влагалище постепенно изменят форму – провисает либо одна стенка (передняя или задняя), либо обе. Если не принимать никаких мер, то через время матка может полностью выпасть наружу, что существенно нарушит качество жизни.
Милые женщины, не доводите себя до такого состояния, когда ничего уже нельзя сделать – только операция и удаление матки! Цена приема врача-гинеколога – ничто по сравнению с ценностью вашего здоровья.
Этиология и патогенез выпадение прямой кишки (ректального пролапса).
Описано много теорий возникновения ректального пролапса. Около 100 лет назад Mosсhcowitz представил выпадение прямой кишки как скользящую грыжу через дефект в тазовой фасции. Позднее Broden and Snellman показали на кинодефекоаграфии, что ректальный пролапс это инвагинация прямой кишки. Выпадение прямой кишки чаще встречается у женщин, чем у мужчин, что вероятно связано с деторождением. Длительные натуживания при потугах, анатомические особенности (широкий таз) являются производящими и предрасполагающими факторами в возникновении этого заболевания. У женщин частота этого нарушения увеличивается с возрастом, тогда как мужчины чаще болеют в молодом возрасте (20-40 лет) и у них почти всегда есть история предварительных болезней прямой кишки, таких как атрезия ануса, либо хирургическое лечение заболеваний прямой кишки и анального канала. У женщин могут быть повреждены срамные нервы во время деторождения, приводящих к нарушению функции тазового дна, таким как недержание мочи и кала или выпадение половых органов или прямой кишки.
Пролапс митрального клапана: клинические варианты, современные представления
Несмотря на более чем полувековую историю изучения пролапса митрального клапана (ПМК), ряд вопросов, касающихся диагностики, определения прогноза, тактики ведения пациентов с этой патологией, продолжают вызывать затруднения у практических врачей. Во многом это связано с морфологической и клинической неоднородностью этого состояния, предполагающей существование разных вариантов митрального пролабирования.
ПМК — синдром, присущий различным нозологическим формам и всякий раз требующий нозологической верификации. Перечень болезней, проявляющихся ПМК, обширен, что объясняется сложностью строения клапанного аппарата сердца и разнообразием механизмов митрального пролабирования. В основе ПМК могут лежать изменения фиброзного кольца, створок митрального клапана и прикрепляющихся к ним хорд, дисфункция папиллярных мышц, нарушения сократимости миокарда левого желудочка.
В клинической практике ПМК может выступать в пяти ипостасях:
- первичный ПМК;
- вторичный ПМК как следствие болезней миокарда;
- вторичный ПМК как проявление наследственных моногенных синдромов;
- митральное пролабирование как вариант нормы или проявление малой аномалии развития сердца;
- ПМК как «эхокардиографическая болезнь».
ПМК как «эхокардиографическая болезнь»
ПМК как «эхокардиографическая болезнь» — ситуация ошибочной диагностики митрального пролабирования. На заре внедрения в клиническую практику двухмерной эхокардиографии ПМК диагностировался у 5–15% и даже 35% людей, подвергнутых обследованию. Столь существенная гипердиагностика была связана с ошибочным представлением о плоской конфигурации митрального клапана. Серия ультразвуковых исследований конца 1980-х гг. доказала трехмерную (седловидную) форму митрального клапанного кольца и сделала обязательной оценку из парастернальной продольной позиции. Современное определение ПМК трактует его как систолическое выбухание одной или обеих створок митрального клапана не менее 2 мм над плоскостью митрального кольца при обязательной регистрации по длинной оси сердца. Как можно заметить, в определении четко оговариваются как анатомические критерии, так и технические аспекты процедуры исследования.
Переход на единые критерии ультразвуковой диагностики и обнародование результатов Фремингемского исследования позволили устранить противоречия во взглядах на распространенность ПМК, которая оказалась существенно ниже, чем представлялось ранее. Из 3491 участника Фремингемского исследования, прошедшего двухмерную эхокардиографию по согласованным диагностическим критериям, у 47 (1,3%) был выявлен классический (с утолщением митральных створок) и у 37 (1,1%) неклассический ПМК с общей частотой 2,4% [1]. Сходные результаты получены и на материале российской популяции.
Вторичный ПМК при болезнях миокарда
В числе прочих причин ПМК может развиваться на фоне коронарной патологии, ревматизма, кардиомиопатии, миокардита, миокардиодистрофии — состояний, вызывающих нарушение сократимости миокарда левого желудочка локального или диффузного характера, дисфункцию или отрыв папиллярных мышц. Подобные варианты митрального пролабирования считаются вторичными, поскольку входят в структуру клинической картины соответствующей болезни. Наличие вторичного ПМК при отсутствии значимой митральной регургитации мало влияет на симптоматику основного заболевания. Исключение составляют случаи острой митральной недостаточности, развившейся в результате отрыва папиллярной мышцы при инфаркте миокарда или тупой травме сердца.
Первичный ПМК
Первичный ПМК — единственный вариант митрального пролабирования, претендующий на нозологическую самостоятельность. Происхождение первичного ПМК связывается с патологией створок митрального клапана, обусловленной конкретной причиной — мезенхимальной неполноценностью в рамках наследственных нарушений (дисплазий) соединительной ткани (ННСТ). ННСТ — группа генетически гетерогенных и клинически полиморфных патологических состояний, объединенных нарушением формирования соединительной ткани в эмбриональном и постнатальном периодах. Генетическая гетерогенность ННСТ подразумевает как моногенную, так и мультифакториальную природу заболевания, а клиническая полиморфность связана с повсеместным распространением в организме соединительной ткани и многообразием проявлений врожденной «слабости» ее отдельных компонентов.
В соответствии с современными представлениями выделяют две категории ННСТ: классифицируемые (имеющие согласованные рекомендации по диагностике) и неклассифицируемые (они же диспластические фенотипы). Согласованные рекомендации по диагностике имеют моногенные синдромы, обусловленные мутацией генов белков внеклеточного матрикса, рецепторов ростовых факторов и матриксных металлопротеиназ. Наиболее известными и клинически значимыми из них являются синдромы Марфана и Элерса–Данло, MASS-фенотип, синдром гипермобильности суставов и другие. К классифицируемым синдромам относится и первичный ПМК. К настоящему времени найдены ответственные за его возникновение три генных локуса, расположенные на 11-й, 13-й и 16-й хромосомах. Поиск генов, причастных к развитию митрального пролапса, продолжается, предполагается, что их идентификация создаст предпосылки для скрининга бессимптомных пациентов, угрожаемых по развитию митральной регургитации. Однако при всей привлекательности молекулярно-генетических методов исследования нельзя не отметить их малодоступность в повседневной практике. Неслучайно существующие рекомендации по ННСТ приоритет в диагностике первичного ПМК оставляют за комбинацией клинических и ультразвуковых данных.
Морфологическим отражением врожденной «слабости» соединительной ткани и маркером первичного ПМК выступает так называемая миксоматозная дегенерация створок митрального клапана. Она характеризуется пролиферацией срединного — спонгиозного слоя створки с избыточным накоплением гликозаминогликанов и дезорганизацией коллагеновых фибрилл (рис. 1). При этом створка утолщается, меняет свои механические свойства, теряет способность противостоять давлению в полости левого желудочка в систолу и пролабирует.
Клиническая картина первичного ПМК разнообразна; он может быть как бессимптомным, так и клинически манифестным. Симптоматика первичного ПМК представлена комбинацией следующих синдромов:
- нарушения внутрисердечной и общей гемодинамики;
- проявления вегетативно-сосудистой дистонии;
- иные (внеклапанные) проявления «слабости» соединительной ткани.
Именно эта триада определяет клиническое своеобразие первичного ПМК, отличающее его от других вариантов митрального пролабирования. Степень выраженности каждого из указанных компонентов может быть разной, что и определяет значительный клинический полиморфизмом, присущий первичному ПМК.
Основным методом и «золотым стандартом» диагностики ПМК является двухмерная эхокардиография. Она позволяет установить факт митрального пролабирования, оценить толщину митральных створок, определить степень митральной регургитации. Указанные характеристики чрезвычайно важны в понимании тяжести состояния пациента, прогноза и тактики ведения. Так, увеличение толщины створки более 5 мм (при норме 2–4 мм) является надежным свидетельством ее миксоматозной дегенерации, представляющей собой морфологический субстрат и основной маркер первичного ПМК. В зависимости от толщины створки выделяют классический (с толщиной створки 5 мм и более) и неклассический (менее 5 мм) ПМК. Поскольку исходы ПМК определяются степенью нарушения внутрисердечной гемодинамики, не менее важным параметром выступает выраженность митральной регургитации, оцененная в ходе допплерографического исследования.
Ведущим механизмом, объясняющим многообразную симптоматику первичного ПМК, признана вегетативная дисфункция, однако наличие бессимптомных пациентов не позволяет однозначно определить ее патогенетическую роль: является ли она причиной ПМК или случайным сочетанием. Тем не менее большинство исследователей считают изменение вегетативного гомеостаза обязательным атрибутом ПМК. Именно вегетативной дисфункцией объясняются такие распространенные проявления «синдрома ПМК», как кардиалгии, большая часть сердечных аритмий, нестабильность артериального давления, липотимии, гипервентиляционный и астенический синдромы. Для объяснения распространенности вегетативной дисфункции при ПМК предложено немало гипотез, в числе которых врожденные изменения перинервия, системный дефект биологических мембран, перинатальное поражение гипоталамических структур, наконец, активно обсуждаемая последнее время версия о патогенетической роли дефицита магния.
Но как бы не были ярки проявления вегетативной дисфункции, в основе гемодинамических нарушений при ПМК лежит все же митральная регургитация. Ее неизбежным следствием становятся объемная перегрузка и дилатация левых отделов сердца, которые приводят к фибрилляции предсердий и прогрессированию сердечной недостаточности. В числе осложнений также можно назвать тромбоэмболии с миксоматозно измененных клапанов и возможность развития вторичного инфекционного эндокардита.
Причиной неблагоприятных последствий и осложнений первичного ПМК выступает не только клапанный механизм. Как было недавно показано, нарушения общей гемодинамики при данной патологии происходят не только посредством митральной недостаточности, но и через дефекты структуры и функции внеклеточного матрикса миокарда, являющиеся следствием врожденной «слабости» соединительной ткани. Указанные дефекты могут служить причиной диастолической дисфункции, снижения сократимости миокарда и развития вторичной кардиомиопатии.
В последнее время представления о тяжести последствий ПМК подверглись переоценке. Ранее ПМК считался патологией с частыми и серьезными осложнениями (включая инсульт, фибрилляцию предсердий, сердечную недостаточность) и высокой потребностью в хирургической коррекции митральной недостаточности. Вопреки прежним сведениям результаты Фремингемского исследования дали основание рассматривать ПМК как доброкачественное состояние с низкой вероятностью неблагоприятных исходов. В частности, частота фибрилляции предсердий, мозгового инсульта, синкопальных состояний у пациентов с ПМК оказалась сопоставимой с аналогичными исходами у лиц с интактными клапанами [1]. Со всей актуальностью встал вопрос о стратификации риска при ПМК. К настоящему времени выделены варианты патологии, ассоциированные с высоким риском и неблагоприятным прогнозом. Вероятность гемодинамических расстройств возрастает при высокой степени митральной регургитации и толщине створки более 5 мм, указывающей на ее миксоматозное перерождение.
Обсуждая возможные осложнения и исходы митрального пролабирования, необходимо подчеркнуть, что первичный ПМК имеет прогредиентное течение. Относясь к врожденной патологии, он тем не менее не встречается у новорожденных, характеризуется низкими показателями заболеваемости среди детей и молодых лиц и затрагивает в основном пациентов зрелого возраста. Временной интервал, предшествующий клинической манифестации ПМК, — период, в течение которого происходит нарастание миксоматозных изменений в клапанной створке вплоть до ее деформации в степени, нарушающей замыкательную функцию и ведущей к митральной регургитации. Появление последней кардинально меняет самочувствие и судьбу больных, что наглядно отражено на рис. 2, соотносящем стадийность течения ПМК с вероятностью осложнений. При этом если тромбоэмболии, инфекционный эндокардит, «функциональные» аритмии регистрируются приблизительно с одинаковой частотой в разные возрастные периоды, то частота застойной сердечной недостаточности и фибрилляции предсердий взмывает вверх после 50 лет.
Роль первичного ПМК в декомпенсации кровообращения и возникновении фибрилляции предсердий в зрелом и пожилом возрасте часто недооценивают. Манифестация клапанной патологии у пожилых больных часто становится причиной диагностических ошибок. Практические врачи слабо осведомлены о ННСТ и по сложившемуся стереотипу относят недостаточность кровообращения и нарушения сердечного ритма у лиц второй половины жизни почти исключительно на счет коронарной патологии. Нередко их не смущает ни отсутствие стенокардии или рубцовых изменений ЭКГ, ни наличие грубого систолического шума, отражающего наличие митральной регургитации.
Отдельной составляющей клинического полиморфизма первичного ПМК выступают внешние и висцеральные маркеры «слабости» соединительной ткани. Поскольку соединительнотканный дефект, лежащий в основе повышенной податливости клапанных створок, является генерализованным, признаки мезенхимальной неполноценности определяются также и со стороны кожных покровов, опорно-двигательного аппарата, внутренних органов. Известные к настоящему времени висцеральные маркеры, а также их важнейшие клинические последствия и исходы приведены в табл.
Поскольку признаки системного вовлечения соединительной ткани являются косвенным подтверждением принадлежности ПМК к ННСТ (т. е. доказательством его «первичности»), их выявление существенно с точки зрения диагностики и оценки прогноза. Так, вероятность клинически и гемодинамически значимого ПМК крайне низка у лиц, не имеющих этих признаков. В целях унификации подходов к оценке системного вовлечения соединительной ткани, в частности, определения порога стигматизации и структурирования признаков с выделением наиболее информативных, предложено использовать принятые мировым сообществом Гентские критерии (Ghent nosology, 2010) синдрома Марфана.
Последнее время характеризуется появлением новых представлений о клеточных и молекулярных механизмах первичного ПМК. Ведущая роль в механизмах возникновения первичного ПМК отводится трансформирующему β-фактору роста (TGF-β) — белку, который активирует рост фибробластов и регулирует формирование и деградацию экстрацеллюлярного матрикса. Выяснено, что целый ряд проявлений ННСТ обусловлен изменением активности TGF-β. В частности, усиленная экспрессия TGF-β обнаружена в миксоматозно измененных створках. Закономерно стремление затормозить повышенную активность TGF-β в целях предотвращения прогрессирования миксоматоза, и такие инструменты уже известны — это нейтрализующие антитела (в эксперименте), блокаторы рецепторов ангиотензина II и β-адреноблокаторы (в эксперименте и клинике). Применение этих средств открывает новые пути коррекции последствий нарушенной мезенхимальной недостаточности и, возможно, будет служить альтернативой хирургическому лечению.
Однако реальные возможности патогенетической терапии первичного ПМК пока остаются скромными. Из относительно широко внедренных в клиническую практику способов лечения следует выделить применение препаратов магния. Патогенетическим обоснованием их применения выступает представление о первичном ПМК как клинической форме генетически обусловленного магниевого дефицита. Известно, что в условиях недостатка ионов магния синтез белков соединительной ткани замедляется, а активность ферментов, участвующих в разрушении коллагена и эластина, напротив, увеличивается. Иными словами, в условиях дефицита магния соединительная ткань разрушается быстрее, чем синтезируется.
В ряде исследований показана принципиальная возможность устранения характерной кардиальной симптоматики и ультразвуковых проявлений ПМК под влиянием препаратов магния. Одно из наиболее известных из них принадлежит коллективу отечественных авторов под руководством академика А. И. Мартынова. 6-месячный курс терапии препаратом Магнерот в дозе 3 г в сутки приводил к уменьшению глубины пролабирования и степени миксоматозной дегенерации клапанных створок. Наряду с этим была достигнута редукция клинической симптоматики, присущей данной категории больных [5]. За прошедшее время было выполнено немало сходных по дизайну исследований, в которых были получены аналогичные результаты.
Наряду с препаратами магния на роль средств патогенетического лечения первичного ПМК также могут претендовать витамины, иные микро- и макроэлементы, анаболики — препараты, имеющие отношение к метаболизму соединительной ткани и способные повлиять на биохимические механизмы, лежащие в основе миксоматозной дегенерации створки и ее пролабирования. Все они в той или иной комбинации находят применение в комплексной терапии первичного ПМК.
Обсуждая лечение ПМК, необходимо четко представлять, что гемодинамически значимое (сопровождающееся признаками сердечной недостаточности) пролабирование — порок сердца, требующий хирургической коррекции. Такие больные должны быть своевременно направлены к кардиохирургу для решения вопроса о протезировании или пластике митрального клапана. Комментируя показания к хирургическому лечению митральной недостаточности, отметим, что современные рекомендации AHA/ACC2014 не подтверждают целесообразность хирургического лечения лишь пациентов с сохраненными фракцией выброса и размером левого желудочка.
Вторичный ПМК при синдромных ННСТ
ПМК может встречаться при моногенных дефектах соединительной ткани, таких как синдромы Марфана, Лоеса–Дитца, Элерса–Данло, несовершенный остеогенез, эластическая псевдоксантома. На его долю приходится 0,25–2% случаев митрального пролабирования. Среди всех моногенных синдромов ПМК наиболее часто наблюдается при синдроме Марфана — 75% случаев (а более тяжелые варианты с миксоматозом клапанов — 28%) [6]. Распространенность ПМК у больных с синдром Элерса–Данло значительно ниже — 6% [7]. ПМК при моногенных ННСТ относится к вторичным, поскольку входит в структуру клинико-морфологических проявлений соответствующей патологии. Однако он характеризуется такими же миксоматозными изменениями клапанов, как и первичный ПМК, и этим схож с ним.
ПМК как вариант нормы или проявление малой аномалии развития сердца
Пограничная степень пролабирования, отсутствие миксоматозного утолщения створок, значимой митральной регургитации и семейного анамнеза позволяют рассматривать ПМК как вариант нормы, преходящий возрастозависимый феномен или малую аномалию сердца. Именно такие случаи митрального пролабирования наиболее часто встречаются в клинической практике, особенно у подростков, субтильных юношей, девушек и молодых женщин, создавая впечатление о чрезвычайной распространенности ПМК в популяции.
В числе причин подобных «невинных» случаев ПМК называют врожденные микроаномалии архитектуры митрального комплекса, асинергию сокращения и расслабления миокарда, нарушение клапанной иннервации и др. Отдельно следует отметить случаи неглубокого, проходящего с возрастом бессимптомного пролабирования, возникающие в пубертатном периоде в связи с неравномерным развитием отдельных элементов клапанного митрального комплекса и их неполным функциональным соответствием друг другу. При этом площадь хордально-створчатого аппарата оказывается избыточной, как бы заготовленной впрок. По окончании периода полового созревания по мере увеличения объема и массы миокарда левого желудочка указанное несоответствие нередко нивелируется (причем у женщин в меньшей степени, чем у мужчин, что, очевидно, объясняет преобладание женщин среди пациентов с ПМК).
Необходимо отдавать отчет в том, что в отсутствие данных молекулярно-генетического исследования достоверно исключить доклиническую стадию первичного ПМК во всех этих случаях не представляется возможным, что оправдывает рекомендации по динамическому наблюдению таких пациентов.
Минуло полвека с момента первого описания ПМК J. В. Barlow, установившему связь позднесистолического шума с митральной регургитацией. К каким итогам мы пришли за это время, какие выводы можем сделать?
- ПМК — синдром, присущий разным нозологическим формам и в каждом случае требующий установления нозологического диагноза.
- Установлены четкие диагностические критерии ПМК, которых следует придерживаться.
- Неоднозначность прогноза при ПМК диктует необходимость стратификации факторов риска.
- Несмотря на возможности молекулярно-генетических методов исследований диагностика ПМК продолжает оставаться синтезом клинических и ультразвуковых проявлений с оценкой признаков системного вовлечения соединительной ткани.
- Достижения в понимании механизмов развития миксоматоза открывают новые перспективы лечения первичного ПМК.
В заключение напомним, что и Всероссийское научное общество терапевтов, и Российское кардиологическое общество выпустили серию рекомендаций, посвященных диагностике и лечению ННСТ и ПМК. Обратившись к этим документам, практический врач может уточнить детали, которые не были в достаточной мере освещены в настоящей статье.
Литература
- Freed L. A., Levy D., Levine R. A. et al. Prevalence and clinical outcome of mitral-valve prolapse // N. Engl. J. Med. 1999; 341 (1): р. 1–7.
- Sainger R., Grau J. B., Branchetti E. et al. Human myxomatous mitral valve prolapse: role of bone protein 4 in valvular interstitial cell activation // J. Cell. Physiol. 2012; 227 (6): р. 2595–2604.
- Boudoulas K. D., Boudoulas H. Floppy mitral valve (FMV)/mitral valve prolapse (MVP) and the FMV/MVP syndrome: pathophysiologic mechanisms and pathogenesis of symptoms // Cardiology. 2013; 126 (2): р. 69–80.
- Delling F. N., Vasan R. S. Epidemiology and pathophysiology of mitral valve prolapse: new insights into diseaseprogression, genetics and molecular basis // Circulation. 2014; 129 (21): р. 2158–2170.
- Мартынов А. И., Акатова Е. В., Николин О. П. Результаты длительной терапии оротатом магния у пациентов с пролапсом митрального клапана // Кардиоваскулярная терапия и профилактика. 2012; 11 (3): с. 30–35.
- Taub C. C., Stoler J. M., Perez-Sanz T. et al. Mitral valve prolapse in Marfan syndrome: an old topic revisited // Echocardiography. 2009; 26 (4): р. 357–364.
- Dolan A. L., Mishra M. B., Chambers J. B., Grahame R. Clinical and echocardiographic survey of the Ehlers-Danlos syndrome // Br. J. Rheumatol. 1997; 36 (4): р. 459–462.
А. В. Клеменов, доктор медицинских наук
ГБУЗ НО ГКБ № 30, Нижний Новгород
Контактная информация
DOI: 10.26295/OS.2019.64.93.014
Пролапс митрального клапана: клинические варианты, современные представления/ А. В. Клеменов Для цитирования: Лечащий врач № 9/2019; Номера страниц в выпуске: 65-69 Теги: сердце, митральное пролабирование, врожденная мезенхимальная неполноценность
Симптомы выпадения прямой кишки
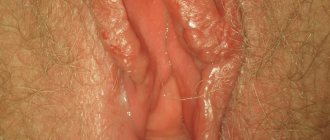
Большинство пациентов с выпадением прямой кишки приходят к хирургу с жалобами именно на само выпадение. Они часто описывают ощущение «чего-то выходящего наружу», особенно во время акта дефекации (Рис.1). Многие жалуются на ощущение того, что они «сидят на мяче», пока самопроизвольное или ручное вправление не уберут выпавшую кишку обратно внутрь. Очень часто это заболевание связано с пачканием нижнего белья и ощущениями выделения слизи из прямой кишки. При пролапсе часто встречается нарушение функции толстой кишки, как запоры и натуживания для акта дефекации, так и недержание кала. При нарушении функции толстой кишки часто встречается повреждения слизистой оболочки (язвы, эрозии и т.д.).
Рис1. Выпадение всех стенок прямой кишки
Классификация
Диагностированные случаи болезни у подростков и взрослых разделяются на два типа:
- ПМК с высоким риском развития регургитации;
- умеренный пролапс с низким риском развития незначительной регургитации.
Также врачи могут разделить недуг на стадии:
- умеренный пролапс 0-1 степени: также известен как первичный (даже при беременности не ощущается никаких негативных симптомов; организм самостоятельно регулирует дополнительную нагрузку на сердце);
- ПМК 2 степени (переходная): признаки — растет внутрисердечное давление, у подростков и при беременности ощущается постоянная одышка, усталость;
- 3-я (декомпенсированная стадия): может быть диагностировано значительное повреждение сердечной мышцы.
Диагностика выпадения прямой кишки (ректального пролапса)
Диагностика спонтанного пролапса очевидна — пролапс всех слоев кишки выглядит как выпадающий цилиндр с концентрическими складками.
У ряда пациентов для его диагностики могут потребоваться натуживания. В этих случаях пролапс лучше всего выявляется в положении сидя на корточках или на стуле. Ряд пациентов приходит на консультацию к хирургу с уже сделанными снимками выпавшей кишки. Очень важно, перед тем как остановить свой выбор на том или ином способе коррекции выпадения прямой кишки необходимо сделать дифференциальную диагностику между пролапсом всех слов стенки прямой кишки и выпадением только слизистой оболочки ее. Пролапс всех слоев выглядит как выпадающий цилиндр с концентрическими складками и канавками в отличие от выпадения только слизистой, где эти складки и борозды имеют строго радиальную ориентацию. Во время исследования врач должен обращать внимание на мацерацию и эрозии перианальной кожи. Тщательное пальцевое исследование прямой кишки является очень важным для выявления сопутствующей патологии анального канала и для оценки адекватности тонуса мышц сфинктеров в состоянии покоя, при сжатии, а также функцию лонно-прямокишечной мышцы.
Далее обязательно следует выполнить колоноскопию, или гибкую сигмоскопию с последующей ирригоскопией с двойным контрастированием для исключения или же выявления любых аномалий слизистой оболочки толстой кишки.
Дефекография
как правило не является обязательной при обследовании пролапса всех стенок прямой кишки, потому что он визуально очевиден, однако, это исследование может быть главной диагностической составляющей при обследовании по поводу внутренней инвагинации прямой кишки (скрытого выпадения) или как часть системы обследования мышц тазового дна.
Анальная манометрия
помогает в оценке функции сфинктеров, потому что хроническое выпадение прямой кишки типично поражает внутренний сфинктер, что приводит к снижению давления в его проекции в состоянии покоя. В манометрических исследованиях больных с выпадением прямой кишки некоторые авторы сообщают об аномалии или полном отсутствии аноректального ингибиторного рефлекса, также отмечается аномально низкое давление в проекции сфинктеров в состоянии покоя, в тоже время давление при сокращении сфинктеров было нормальным.
Анальная электромиография
и исследование скорости проведения возбуждения по волокнам срамного нерва в основном не являются клинически важными исследованиями при этом заболевании, если только нет в истории заболевания необходимости особенно сильных натуживаний для акта дефекации. В таких случаях анальная электромиография может быть применена для исследования наличия неадекватного или же парадоксального (извращенного) сокращения лонно-прямокишечной мышцы — анизм (не расслабляющаяся лонно-прямокишечная мышца или спастическое тазовое дно).
Исследование времени транзита по толстой кишке
должно быть выполнено у больных, с наличием в истории заболевания указаний на запоры, в противном случае может быть выбран неправильный метод операции.
Симптомы пролапса гениталий
На первых этапах болезнь никак не проявляется, а незначительные отклонения могут быть обнаружены только на гинекологическом обследовании. Позднее возникают тянущие боли в нижней части живота, в области поясницы, которые усиливаются и отдают во влагалище при движении. Кроме этого, могут появиться:
- белые выделения, не имеющие запаха, по консистенции похожие на слизь;
- дискомфорт при опорожнении или напряжении брюшных мышц;
- невозможность удержать мочу;
- болезненность и кровянистые выделения после полового акта;
- частые запоры, недержание газов;
- на выходе из влагалища может прощупываться мягкое, подвижное образование (провисшая стенка).
Лечение ректального пролапса (выпадения прямой кишки)
Очевидно, что консервативные мероприятия не способны ликвидировать пролапс тазовых органов, но могут замедлить его прогрессирование, способствовать коррекции отдельных проблем (дисфункции кишки, недержания мочи), а также повысить эффективность оперативного лечения.
Выпадение прямой кишки почти всегда лечится хирургически, при ректоанальной инвагинации должны быть сделаны все усилия терапевтического характера с тем, чтобы избежать хирургии.
Стоит отметить, что при наличии неадекватного или же парадоксального (извращенного) сокращения лонно-прямокишечной мышцы (анизм) может быть применена система тренировки обратной связи или введение Ботулотоксина.
Восстановить структуру и функцию тазового дна, а также существенно улучшить качество жизни пациентов с выпадением прямой кишки может только хирургическое вмешательство.
Хирургическое лечение выпадения прямой кишки (ректального пролапса)
Посмотреть видео операций в исполнении профессора Пучкова К.В. Вы можете на сайте «Видео операций лучших хирургов мира».
Большое количество различных методов было предложено для лечения выпадения прямой кишки. Хирург должен определить, какой метод оперативного вмешательства будет наилучшим для каждого пациента. При этом во внимание принимается большое количество индивидуальных факторов и особенностей методов операции.
Основными индивидуальными факторами являются пол и возраст больного, общемедицинское состояние пациента, функция толстой кишки, а также присутствует или нет недержание кала.
Обязательно следует учитывать протяженность выпадающего участка толстой кишки, влияние операции на функцию толстой кишки и континенцию, риск осложнений при операции, частоту рецидивов при том или ином виде операции, индивидуальный опыт хирурга.
Перед тем как остановить свой выбор на том или ином способе коррекции выпадения прямой кишки необходимо сделать дифференциальную диагностику между пролапсом всех слов стенки прямой кишки и выпадением только слизистой оболочки ее. Пролапс всех слоев выглядит как выпадающий цилиндр с концентрическими складками и канавками в отличие от выпадения только слизистой, где эти складки и борозды имеют строго радиальную ориентацию.
Хирургические доступы в лечении ректального пролапса
Существует два основных подхода при хирургии выпадения прямой кишки – абдоминальные операции и промежностные операции.
Наиболее частой абдоминальной операцией при выпадении прямой кишки является фиксация прямой кишки (ректопексия)
, выполняющаяся изолированно или синхронно с
резекцией сигмовидной кишки.
Типичной промежностной операцией является промежностная ректосигмоидэктомия (операция Алтмайера) или резекция рукава слизистой оболочки выпадающего отдела прямой кишки (операция Делорма).
Специфичность каждой операции должна определяться с учетом состояния и совокупности всех патологических изменений у каждого пациента, но некоторые обобщения могут быть сделаны. Пожилые пациенты с высокой степенью операционно-анестезиологического риска лучше всего лечатся промежностными операциями, которые могут проводиться под региональной анестезией или даже под местной анестезией с внутривенной седацией. Крепкие здоровьем пациенты, с нормальной функцией толстой кишки, могут легко перенести как абдоминальную ректопексию вместе или без синхронной резекции сигмовидной кишки, так и промежностную резекцию прямой и сигмовидной кишки, вместе или без синхронной леваторопластики по поводу недержания кала
.
Функция толстой кишки играет роль в выборе плана операции. Больные с запорами обычно должны подлежать ректопексии и резекции сигмовидной кишки, тогда как пациенты с недержанием кала и выпадением прямой кишки подлежат синхронной абдоминальной ректопексии или промежностной резекции прямой и сигмовидной кишки вместе с леваторопластикой. Рецидивный случай заболевания требует информации о виде первой операции, поскольку эта информация будет определять дальнейшую тактику лечения; первая операция может ограничить выбор операции при рецидиве из-за изменения кровоснабжения оперированной прямой кишки.
К сожалению, существует недостаток высококачественных данных по поводу того, какой именно метод является оптимальным для лечения выпадения прямой кишки. В 2008 году была сделана попытка всеобъемлющего анализа рандомизированных исследований, который выявил недостаточность данных для анализа, хотя некоторые выводы были сделаны. Способ фиксации кишки при ректопексии не влияет на результат. Пересечение боковых связок прямой кишки приводило к высокой частоте запоров, тогда как резекция и ректопексия приводила к меньшим запорам. Наконец, лапароскопические операции приводили к более быстрому восстановлению после операции и меньшим осложнениям.
Лапароскопический доступ в лечении выпадения прямой кишки
В последние годы возрастает популярность лапароскоппического доступа в колоректальной хирургии и во многих случаях использование этого доступа оправдано. Лапароскопической доступ для лечения выпадения всех слоев стенки прямой кишки был использован при множественных техниках абдоминальной коррекции ректального пролапса, таких как ректопексия, резекция с ректопексией и операции с сеткой
. В основном успех и осложнения сравнимы с традиционными операциями с одним преимуществом – более короткая госпитализация и быстрое выздоровление.
Сообщается об итогах 10 летнего опыта применения лапароскопически ассистированной ректопексии с резекцией кишки в рамках одного института у 117 больных с выпадением прямой кишки. Летальность составила 0,8% (1 больной), а осложнения после операции развились у 9% больных (10 человек из 117); 77 из 117 пациентов (66%) были под наблюдением в среднем около 62 месяцев. Рецидив полностенного выпадения прямой кишки был в 2,5% случаев, выпадение слизистой прямой кишки в 18%. Другие авторы обследовали 77 больных, которые перенесли лапароскопическую заднюю ректопексию сеткой (модифицированная операция Wellsа). Они описали только один случай перехода на открытую операцию из-за выраженного спаечного процесса и 2 интраоперационных осложнения, которые были с легкостью скорректированы во время лапароскопической операции. Рецидив заболевания был только у одного больного и 90% пациентов при длительном наблюдении (более 34 месяцев) были удовлетворены результатами операции.
Лечение
Лазерное омоложение
При начальных признаках опущения влагалища и матки назначается неинвазивное лечение – лифтинг стенок влагалища лазером. В клинике Марины Рябцс для лечения и профилактики пролапса гениталий используется лазерная установка Fotona (Словения). Это топовый лазер, широко используемый в гинекологи для решения функциональных и эстетических задач. Качество лечения будет высоким, а результат – длительным и прогнозируемым, если вы пройдете курс процедур. Даже один сеанс позволит вам почувствовать себя лучше, но, чтобы закрепить эффект, нужно прийти на процедуру трижды. Плюсами лазерного метода являются безболезненность, минимальная реабилитация (половую жизнь, например, можно возобновить уже спустя 3 дня после сеанса), отсутствие травматизации стенок влагалища (лазер воздействует на более глубокие слои, не повреждая поверхность слизистой). Лечение пролапса органов малого таза лазером широко используется во всем мире, не противопоказано пациентам с онкологией в анамнезе и отлично сочетается с другими гинекологическими «косметологическими» процедурами: биоревитализацией, контурной пластикой.
Хирургическая коррекция
«Запущенный» пролапс, сопровождаемый грыжами, лечится традиционным хирургическим методом. Реабилитация проводится под общим наркозом, после нее следует реабилитация с рядом ограничений. Так, на протяжении длительного времени вам нельзя будет посещать баню и бассейн, купаться в открытых водоемах, заниматься сексом, принимать ванну.
Рецидив выпадения прямой кишки
Хотя выпадение прямой кишки исторически имеет высоких рецидив заболевания ( до 50%), современные данные свидетельствуют, что повтор выпадения прямой кишки после операции ректопексии с резекцией сигмовидной кишки менее 10%. В основном, при промежностных операциях по поводу выпадения прямой кишки существует более высокий риск рецидива, чем при абдоминальных операциях.
Пациенты с рецидивом выпадения прямой кишки нуждаются в обследовании – манометрии и дефекографии. Очень важно информировать больного о том, что даже если пролапс скорректирован, тем не менее, остаются сопутствующие нарушения функции толстой кишки (запоры или поносы), которые не корректируются ректопексией. Одним из наиболее важных моментов в выборе лучшего хирургического пособия для коррекции рецидива выпадения прямой кишки является оценка ее оставшегося кровотока после первой операции. Первая операция, выполненная по поводу ректального пролапса, играет основную роль в определении типа вмешательства для коррекции рецидива выпадения, так как резекция кишки прерывает кровоснабжение отделов толстой кишки. Любой пациент, который перенес первичную резекцию прямой или сигмовидной кишки с анастомозом требует очень тщательного обследования перед тем, как идти на вторую операцию, включая тщательное изучение протокола первой операции.
Очевидный риск повторной резекции представляет собой ишемия сегмента толстой кишки между двумя анастомозами. Например, если пациент перенес вначале промежностную ректосигмоидэктомию, то потом повторная промежностная ректосигмоидэктомия или трансабдоминальная ректопексия могут быть выполнены. Однако, в таких случаях трансабдоминальная ректопексия с резекцией сигмовидной кишки должна быть исключена из-за риска ишемии остающегося сегмента прямой кишки. Для тех больных, которые первоначально перенесли трансабдоминальную ректопексию, но у них наступил рецидив, повторная трансабдоминальная ректопексия является операцией выбора. Рецидив полностенного выпадения прямой кишки может быть успешно корректирован тем же вариантом операции, который был первоначально.
Сообщения в литературе свидетельствуют об успешном результате коррекции рецидива выпадения прямой кишки в 85-100% случаев. К сожалению, в то время как большинство авторов обосновывают первоначальную хирургическую технику, при повторных вмешательствах они не стремятся адекватно обосновать выбор типа операции. Из этих соображений, видимо, существует недостаточное количество данных, на основании которых можно было бы принять интеллектуально обоснованное лечебное решение по коррекции рецидива выпадения прямой кишки. Не существует специфического алгоритма, доступного для применения в выборе лучшей операции по лечению рецидива выпадения прямой кишки, за исключением того, что большинство сообщений свидетельствуют о том, что лечение молодых пациентов должно быть трансабдоминальным, а пожилых — промежностным доступом.
Было проведено большое ретроспективное исследование 78 больных с рецидивным пролапсом прямой кишки выбранных из группы 685 пациентов, перенесших первичную коррекцию выпадения прямой кишки. При исследовании повторного рецидива после второй и иногда даже 3 операции они показали, что доступ (абдоминальный, против промежностного) определяет частоту повторного рецидива заболевания. Абдоминальные операции были связаны с более низким рецидивом повторного выпадения прямой кишки. Авторы сделали вывод, что если возможно, абдоминальный доступ должен быть использован при коррекции рецидива выпадения прямой кишки.
Как диагностировать?
Наиболее эффективный способ определить наличие заболевания – сделать УЗИ сердца в Ростове-на-Дону. При помощи ультразвукового исследования врач получит понимание о степени пролабирования створок и объеме регургитации.
Для диагностики также выполняют ЭхоКГ, по данным которой выявляют:
- Стадию пролапса;
- Дисплазию соединительной ткани;
- Количество крови, поступающей обратным забросом в предсердие.
По данным исследования врач устанавливает степень регургитации митрального клапана, т.е. на каком уровне она происходит:
- I – створки;
- II –доходит до середины левого предсердия;
- III – доходит в противоположный конец предсердия.
Список опубликованных работ по теме «Ректальный и генитальный пролапс»
«Малоинвазивная хирургия толстой кишки», К. В. Пучков, Д. А. Хубезов
- Пучков К.В., Карпов О.Э., Филимонов В.Б. Лапароскопическая ректопексия // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии.-1997.-Т. 7, №5(прил. 4). -С.248.
- Puchkov K., Filimonov V., Titov G., Chubezov D. Laparoscopic technology in coloproctology // Proktologia. – 2001. — Suppl. №1. – P. 97.
- Пучков К.В., Хубезов Д.А. Лапароскопическая ректопексия // Проблемы колопроктологии. Вып. 18. — М., 2002. — С.194-195.
- Пучков К.В., Хубезов Д.А., Юдина Е.А.. Лапароскопическая одномоментная ректо- и сакровагинопексия // Актуальные вопросы колопроктологии: тез. докл. 1-го съезда колопроктологов России с междунар. участием / под ред. Г.И. Воробьева, Г.П. Котельникова, Б.Н. Жукова.- Самара: ГП < Перспектива >: СамГМУ, 2003. — С. 398-399.
- Пучков К.В., Хубезов Д.А., Политова А.К. Лапароскопическая ректо- и сакровагинопексия у пациенток с сочетанием ректального пролапса и выпадением матки // Актуальные проблемы современной хирургии: тр. конгр., Москва, 22-25 февр. 2003 г. – М., 2003. — С.36.
- Пучков К.В., Хубезов Д.А., Юдина Е.А., Хубезов А.Т., Подъяблонский А.В. Лапароскопическая ректо- и вагиносакропексия одним имплантатом // Актуальные проблемы хирургии органов таза. — М., 2003.- С. 79 –81.
- Пучков К.В., Иванов В.В., Баков В.С., Усачев И.А. Оптимизация техники хирургического лечения тазового пролапса // Малоинвазивные технологии в хирургии: материалы межрегион. науч.-практ. конф. — Махачкала: ИПЦ ДГМА, 2005. — С.159-160.
- Пучков К.В., Хубезов Д.А. Малоинвазивная хирургия толстой кишки: Руководство для врачей.- М.: ОАО «Издательство «Медицина», 2005.- 280 с.
- Пучков К.В., Баков В.С., Иванов В.В. Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии: Монография.- М.: ИД МЕДПРАКТИКА – М.- 2005.- 168 с.
- Пучков К.В., Иванов В.В., Усачев И.А. Применение полипропиленовых имплантатов при одновременном выпадении тазовых органов // 9-й Моск. междунар. конгр. по эндоскопической хирургии, Москва, 6-8 апр. 2005 г.: тез. докл. / под ред. Ю.И. Галингера. – М., 2005. — С.296-297.
- Puchkov K.V., Ivanov V.V., Barsukov V.A., Filimonov V.B. Determining of safety of soldering of vessels in tissue mass of various types while using the technique of dosed ligating electrothermal influence of ligasure // Abstracts of The 10-th World Congress of Endoscopic Surgery, 13-16 September, 2006, Berlin. – P.288.
- Пучков К.В., Черноусова Н.М., Филимонов В.Б., Васин Р.В., Андреева Ю.Е. Коррекция генитального пролапса и недержания мочи при напряжении у женщин с помощью современных синтетических имплантов // Журн. акушерства и женских болезней.-2007.-Т. 57 ( спец. вып.). — С.204-206.
- Puchkov K.V., Filimonov V.B., Vasin R.V. Correction of pelvic floors prolapse and women under tension enuresis // Abstracts book of the 16-th EAES Congress 2008 with the help of up-to-date implants, 11-14 July, 2008, Stockholm, Sweden. – P.208-209.
- Пучков К.В., Филимонов В.Б., Васин Р.В., Васина И.В. Осложнения использования полипропиленовых имплантов при тазовом пролапсе // Журн. акушерства и женских болезней.-2009.-Т. 58 .( выпуск 5). — С.66-67.
- Пучков К.В., Филимонов В.Б., Васин Р.В., Васина И.В. Диагностические возможности и значение ультрасонографии и магнитно-резонансной томографии при тазовом пролапсе // Журн. акушерства и женских болезней.-2009.-Т. 58. (выпуск 5). — С.67-68.
- Puchkov K.V., Filimonov V.B., Vasin R.V., Vasin I.V. Polypropylene implants as the treatment decision for patients with pelvic prolapses, connective tissue displasia and stress incontinence // Abstracts book of the 17-th EAES Congress 2009, 17-20 June, 2009, Prague, Czech Republic. – P.96.
- Puchkov K.V., Podzolkova N.M., Andreeva J.E., Dobychina A.V., Korennaya V.V. Polypropylene implants as the treatment decision for patients with pelvic prolapses // 21st ESGE Annual Congress (Paris, 11-14 September 2012) — Р.88-89.
Профилактика пролапса гениталий
Чтобы не пришлось прибегать к таким радикальным мерам, как операционное удаление матки, следует придерживаться нескольких несложных правил.
- Избегать тяжелого физического труда, ношения тяжестей.
- В течение беременности и после рождения ребенка выполнять все рекомендации лечащего врача.
- Правильно питаться, не допускать ожирения.
- Вести активный образ жизни, заниматься физкультурой, плаванием.
- Ежегодно посещать гинеколога.
- При малейшем отклонении и начальных стадиях опущения гениталий, выполнять специальные комплексы упражнений (гимнастика Кегеля).