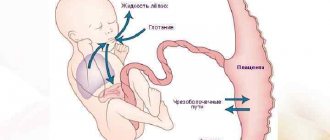
Одной из причин женского бесплодия может оказаться синдром Шерешевского-Тернера. Это генетическое заболевание, обусловленное отсутствием второй Х-хромосомы. Можно сказать, что именно она окончательно делает из женщины женщину.
Естественная беременность при синдроме Шерешевского-Тернера практически невозможна, поскольку у больной женщины не вырабатываются яйцеклетки нужного качества. Раньше подобный диагноз становился приговором, и пациентка теряла всякую надежду на рождение ребенка. Сегодня наука шагнула вперед, и, пройдя определенное лечение, такие женщины могут познать счастье материнства. Клиника «Центр ЭКО» предлагает вам почти беспроигрышный метод, как забеременеть с диагнозом «синдром Шерешевского-Тернера» – ЭКО. Он предпочтительнее, поскольку снижает риск передачи указанного заболевания потомству.
Синдром Шерешевского-Тернера: характеристика заболевания
Эта болезнь была открыта Н. А. Шерешевским почти 90 лет назад. Советский эндокринолог дал подробное описание патологии, предположив, что за ее проявление ответственны гипофиз и половые железы, не в полном объеме выполняющие свои функции. Ученый также обратил внимание на врожденные пороки внутреннего развития больных. Более десяти лет спустя Тернер несколько иначе описал синдром и обозначил его основные внешние признаки.
Хромосомную природу недуга выявил Ч. Форд в конце пятидесятых годов, однако его имя в названии болезни не отражено. Впоследствии было доказано, что решающую роль в развитии ряда аномалий организма, описанных предшественниками Форда, играет именно моносомия. В науке долго велись споры на тему, кто же является первооткрывателем заболевания.
Итак, синдром Шерешевского-Тернера, причины возникновения которого заключаются в отсутствии Х-хромосомы или замещении ее изохромосомой, встречается у одной новорожденной девочки из четырех тысяч. Нередко беременности плодом с данной патологией заканчиваются выкидышами.
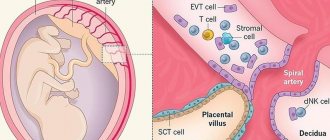
Если в процессе внутриутробного развития у ребенка диагностирован синдром Шерешевского-Тернера, кариотип младенца будет 45Х0. Примечательно, что изначально эмбрион развивается нормально, и лишь к моменту родов половые клетки подвергаются атрезии. У новорожденной яичники будут представлены рудиментами, либо в них не окажется фолликулов.
Лимфедема
На фото лимфедема — вследствие нарушения оттока лимфы и ее скопления в межклеточном пространстве, увеличивается объем конечностей.
Лимфедема – заболевание, при котором появляется отек части тела, который возникает, из-за неправильной работы лимфатической системы (см. фото лимфедемы).
Лимфедема является хронической патологией лимфатической системы, приводящей к другим заболеваниями, таким как: язвы, повышенная пигментация, экземы, уплотнение и т.д.
Синдром Шерешевского-Тернера: мозаичная форма
При мозаичной форме данного заболевания в организме больной сочетаются два типа клеток. Одни обладают нормальным кариотипом, тогда как в других проявляется патология. В целом кариотип будет выглядеть, как 46ХХ/45Х. Состояние здоровья женщины при этом будет зависеть от пропорции клеток с нормальным кариотипом и клеток без одной X-хромосомы.
У многих пациенток развиваются половые признаки, в том числе и гениталии. Шансы на беременность при мозаичном типе синдрома значительно выше, причем зачатие может произойти даже естественным путем. Однако беременной с таким диагнозом понадобится пренатальное кариотипирование, поскольку плод будет находиться в группе риска.
Если у будущей матери синдром Шерешевского-Тернера, профилактика его у ребенка обязательна. Она заключается в выявлении патологий внутриутробного развития и консультациях у генетика.
Диагностика
Синдром Шерешевского-Тернера у новорожденных девочек позволяет заподозрить наличие лимфедемы либо крыловидной складки на шее. Если такие признаки отсутствуют, то подозрение на наличие данной патологии может появиться позже ввиду низкорослости, аменореи, а также при отсутствии пубертата. Исследование кариотипа позволяет подтвердить либо опровергнуть такой диагноз. В целом установить диагноз позволяет наличие клинической картины, характерной для этого заболевания.
С целью выявления врожденных пороков сердца проводится МРТ или эхокардиография. Также проводятся некоторые специфические обследования, в частности, цитогенетическое исследование. Исследование крови при развитии данного забоелвания демонстрирует снижение количества эстрогенов и при этом высокое содержание гормонов гипофиза. При рентгеновском исследовании часто определяется остеопороз, а также патологии развития костного скелета. Кроме того, в процессе диагностики проводится и обследование, направленное на определение сопутствующих заболеваний.
Также в современной медицине практикуются скрининговые проверки, которые дают возможность узнать о риске наличия у плода синдрома Шерешевского–Тернера.
Синдром Шерешевского-Тернера: симптомы патологии
Время начала проявления заболевания у всех пациентов неодинаково. У одних оно диагностируется еще во внутриутробном периоде. Такие дети рождаются с длиной тела не более 48 см и весом 2500-2800 кг. У других патология проявляет себя через несколько лет: девочка заметно отстает в росте, родителям бросаются в глаза вальгусное отклонение в локтевых суставах, низкая линия роста волос на задней части шеи, опущение век. Кроме того, дети с синдромом Шерешевского-Тернера могут страдать задержками умственного развития.
Хотя данная болезнь связана с половым недоразвитием, многие ее симптомы являются внешними:
- маленький рост (135-145 см для взрослой женщины);
- короткая шея;
- неправильное телосложение;
- необычная форма грудной клетки (от щитообразной до бочкообразной);
- укороченные кости запястья;
- избыточное количество кожи на шее (так называемые «крылья);
- низкая посадка ушей, деформация ушных раковин;
- опущенные веки, наличие эпикантуса;
- обилие пигментных пятен.
Так выглядят люди с синдромом Шерешевского-Тернера. Обычно они страдают от сердечных аномалий, пороков кровеносной системы, проблем с почками. Однако нельзя сказать, что при постановке данного диагноза у ребенка будет полный набор всего перечисленного. Проявления у каждого больного – индивидуальные. Синдром Тернера-Шерешевского, признаки которого не могут быть одинаковыми у двух женщин, этим и примечателен. Хотя статистика и приводит примерную картину заболевания, несколько идентичных случаев найти практически невозможно.
Клинические проявления синдрома Шерешевского — Тернера впервые описаны Н. А. Шерешевским в 1925 г. и, независимо, Н. Turner в 1928 г., а хромосомные мутации установлены в 1959 г. Традиционно пациенток консультирует врач-эндокринолог в связи с ма- лорослостью, нарушением развития из-за де-фицита половых гормонов для решения ассоциированных с этими явлениями клинических вопросов. Изучение коморбидности — одно из приоритетных направлений медицинских исследований в последние годы. В связи с про- грессированием комплексной патологии сердечно-сосудистой системы формируется прогноз для жизни пациенток данной группы. Наблюдения за ними выявили целесообразность кардиологического обследования и лечения. Рассмотрим принципы консультирования кардиологом пациенток с синдромом Шерешевского — Тернера, генетическим заболеванием, ассоциированным с коморбидной патологией.
Распространенность указанного синдрома составляет 25—55 случаев на 100 000 женщин. Диагностируется в течение первых 6 нед у трети пациенток, еще у трети — в детском возрасте из-за патологии, выявляемой педиатром, остальные случаи — в пубертатном периоде.
При обследовании пациенток выявляется комплексная патология: низкорослость (100%); черепные уродства; микрогнатия (60%), высокое «арочное» небо (38%); короткая шея (40%); низко посаженные повернутые уши; перепончатая шея (25%), низкий рост волос сзади (42%); множественные пигментные невусы (26%); гипо- пластичные и/или недоразвитые соски; укорочение четвертой метакарпальной кости (37%); искривление в локтевом суставе (47%); лимфатическая обструкция, отек рук и ног (22%); ги-первыпуклые, тонкие и хрупкие ногти (13%); почечные анатомические уродства, подковообразные почки (40%); первичный гипогонадизм (96%); тироидит Хашимото, гипотиреоз (44%); искривление в коленных суставах (35%) [1].
Диагностика аномалий кариотипа (45,Х (45,Х/ 46,ХХ, структурная патология Х-хромосомы) про-водится с помощью генетического тестирования и ПЦР-анализа. Для синдрома Шерешевского— Тернера характерен мозаицизм. При этом клиническом состоянии не все клетки человека содержат одинаковые хромосомы: могут присутствовать две или более генетически различные клеточные популяции. Наиболее часто выявляется вариант 45х/46хх, а 45,Х/ 46,Хг(Х) — один из самых редких. Поиск ано-мальной Y-хромосомы определяет прогноз из- за развития опухоли: гонадобластома или дисгерминома. Последняя ассоциирована с плохим прогнозом из-за метастастатического роста [2].
Факторами риска по кардиологической летальности пациенток с синдромом Шерешев- ского — Тернера являются врожденные сердечно-сосудистые заболевания, диссекция аорты, ишемическая болезнь сердца [3]. Расчетное снижение продолжительности жизни в возрасте 1 года составляет 12,5 года, а для групп в возрасте 20 и 40 лет соответственно 11 и 10 лет [4]. При этом наибольшая смертность установлена среди имеющих кариотипы 45,Х и isoXq [5]. При анализе смертности в разных возрастных группах оказалось, что с увеличением возраста увеличивался вклад сердечно-сосудистой и респираторной патологии, а вклад влияния врожденных аномалий сердца уменьшался [6].
Скрининг сердечно-сосудистой патологии осуществляется следующим образом. Всем пациенткам при диагностике синдрома проводится обследование кардиолога с экспертизой врожденных пороков сердца, комплексное обследование с измерением артериального давления на всех конечностях, а также качественная визуализация сердца, аортального клапана, дуги аорты, легочных вен [7]. Изучение ком-плексной сосудистой патологии при синдроме Шерешевского — Тернера способствовало формулированию рекомендаций по визуализации: в связи с тем, что эхоКГ рекомендовано для диагностики в раннем возрасте, МРТ следует использовать у старших девочек и взрослых, которые способны перенести процедуру без седатации. Визуализация рекомендуется каждые 5—10 лет, при этом модальность повторения тестов неспецифична [8].
Рекомендуется проводить ежегодный скрининг заболеваний сердечно-сосудистой системы у взрослых с целесообразным измерением массы тела, роста, артериального давления, биохимических показателей крови (гликемии и НЬА1с, креатинина, мочевины, электролитов, печеночных трансаминаз, липидного профиля — если он не изменен, то повторно контролировать через более редкие интервалы), общего анализа мочи и показателей гормонов щитовидной железы [9].
Наряду с традиционными факторами риска ишемической болезни сердца (артериальная гипертензия, инсулинорезистентность, сахарный диабет, дислипидемия, ожирение), имеются и специфические (дефицит эстрогенов, дефицит гормона роста, статус гиперкоагуляции и тромбообразования) [6]. Факторами, определяющими летальность от ИБС, являются: аномалии сердца, эндотелиальная дисфункция, ожирение, артериальная гипертензия, гиперли- пидемия, инсулинорезистентность, сахарный диабет и дефицит эстрогенов [3]. Клиническое течение синдрома связано с развитием вторичной артериальной гипертензии из-за коарктации аорты, гипоплазии дуги аорты, мальформации почечных сосудов и при вторичной почечной дисфункции [6]. Ассоциированная патология увеличивает риск прогрессирования сердечнососудистой патологии по сравнению с популя- ционными группами, не имеющими генетической патологии. Это следует учитывать при планировании диспансерных мероприятий.
Скрининговыми критериями для выявления коарктации аорты по анамнезу являются головная боль, носовое кровотечение, слабость в ногах. Объективное обследование выявляет шум над аортой с распространением по току крови. При комплексном обследовании порока у пациентки устанавливают признаки перераспределения крови по крупным сосудам: различие в артериальном давлении (>20/10 мм рт. ст.) между верхними и нижними конечностями или правой и левой рукой, а также изменения формы тени аорты при рентгенографическом исследовании органов грудной клетки с верификацией по данным эхоКГ и других тестов визуализации [10].
Для диагностики артериальной гипертензии следует использовать существующие клинические рекомендации, при этом следует учесть некоторые особенности данной клинической группы. В рамках концепции старения сосудов следует рассматривать результаты популяционных исследований при синдроме Шерешевского — Тернера, которые продемонстрировали увеличение показателей систолического и диастоличес- кого артериального давления с возрастом пациенток. Установлена корреляционная связь между увеличением индекса массы тела и повышением показателей систолического и диас- толического артериального давления [11]. Целевым показателем индекса массы тела считается значение не более 25 кг/м2 [9]. На основании этих фактов немедикаментозные способы коррекции артериального давления столь же актуальны, как и для других групп пациентов с арте-риальной гипертензией. При выявлении офисного артериального давления более 130/80 мм рт. ст. следует выполнить суточное мониториро- вание артериального давления. Целевые показатели среднего дневного артериального давления соответствуют значению 130/80 мм рт. ст. При лечении пациентке дают только советы по изменению образа жизни при значениях артериального давления от 130/80 до 140/90 мм рт. ст. при отсутствии признаков прогрессирования кар- диальной патологии. При наличии коарктации аорты, бикуспидального аортального клапана и дилатации аорты следует начать медикаментозную антигипертензивную терапию, при показателях не менее 140/90 мм рт. ст. медикаментозную терапию следует провести при отсутствии структурных изменений аорты [9]. Эти рекомендации основаны на первичных данных выявления линейной взаимосвязи между систолическим артериальным давлением и диаметром корня аорты (r=0,5; р=0,003) [12]. Артериальная ги- пертензия является фактором риска развития диссекции аорты [3], а структурным фоном для развития этой неотложной ситуации являются дилатация восходящей аорты, элонгация дуги аорты, коарктация аорты, бикуспидальный аортальный клапан [8].
Старение сосудов и прогрессирование сосудистой патологии отмечается при наличии сахарного диабета. Нарушение толерантности к глюкозе встречается у 50% пациенток [9], распространенность диабета 2-го типа определяется встречаемостью генетического варианта: для делеции Хр распространеность диабета составляет 9% относительно общей популяции, при 45,Х — 18%, Хр — 23%, изохромосоме Хр — 43%. При этом развивается сосудистая симпатическая дисфункция из-за формирования диабетической автономной нейропатии, дефицита эстрогенов и дисбаланса в системе ренин-ангиготензин-альдостерона [6]. Лечение пациенток с синдромом Шерешевского — Тернера целесообразно проводить совместно с кардиологом и эндокринологом.
Мониторирование течения кардиологической патологии проводится по показаниям, при арте-риальной гипертензии — ежегодно. Для пациенток с практически нормальным артериальным давлением и сердечно-сосудистой системой повторная визуализация сердца и аорты осуществляется при переводе в клинику для взрослых по возрасту пациентов, перед беременностью, при первичном выявлении артериальной гипер- тензии. Если уже проводилась сонография сердца, то по возрасту показана МРТ и дальнейшая визуализация каждые 5—10 лет. В случае выявления сердечно-сосудистого заболевания показано мониторирование и лечение у кардиолога по программам наблюдения, соответствующим выявленному заболеванию [7].
У пациенток с синдромом Шерешевского — Тернера наблюдается атерогенный характер изменения липидограммы: повышение липопро- теинов низкой плотности и триглицеридов, снижение липопротеинов высокой плотности [13]. При наличии сердечно-сосудистого заболевания, сахарного диабета 1-го и 2-го типа с поражением органов-мишеней, хронической болезни почек со скоростью клубочковой фильтрации менее 30 мл/мин/1,73 м2 и значением по шкале SCORE 10% и более пациентку следует отнести к очень высокому риску. Высокий риск устанавливается при семейной дислипидемии, тяжелой артериальной гипертензии, сахарном диабете без осложнений, умеренно сниженной скорости клубочковой фильтрации 30—59 мл/мин/1,73 м2 и значении по шкале SCORE 5% и более, но менее 10%. Умеренный риск— при значении SCORE 1% и более, но менее 5% за 10 лет, а также при семейном анамнезе кардиальной патологии, абдоминальном ожирении, низкой физической активности, изменениях значений холестерина, триглицеридов, С-реактивного белка, установленных тест-системами высокой чув-ствительности. Низкий риск определяют при значении SCORE менее 1% и отсутствии факторов риска. Целевыми значениями для группы очень высокого риска будет величина липопротеинов низкой плотности менее 1,8 ммоль/л, высокого риска — менее 2,5 ммоль/л, умеренного риска — менее 3 ммоль/л. Целевым значением липопро- теинов высокой плотности для женщин является значение более 1,2 ммоль/л [14].
После лабораторного подтверждения гипер- холестеринемии следует определить процент снижения уровня холестерина у конкретной пациентки до целевого значения в зависимости от подгруппы риска. Далее подбирают препарат и соответствующую условиям дозировку статина. Так, для снижения липопротеинов низкой плотности до 55% следует использовать розувастатин 20 мг или аторвастатин 80 мг в сутки, а для снижения на 63% — только розу- вастатин в дозе 40 мг в сутки [15] (по таблице FDA — Food and Drug Administration, США).
Для достижения целевого уровня липидограм- мы следует назначать статины в наибольшей ре-комендованной дозе или максимальной по переносимости у данной пациентки. При непереносимости статинов рекомендуется использовать сек- вестранты желчных кислот или препараты никотиновой кислоты; в этих условиях возможно применение ингибиторов абсорбции холестерина — одних или в комбинации с секвестрантом желчных кислот, или с препаратом никотиновой кислоты. Если целевой уровень показателей липидо- граммы не достигнут, то может быть рекомендована комбинация статина и ингибитора абсорбции холестерина или секвестранта желчных кислот, или препарата никотиновой кислоты. Целевые значения триглицеридов менее 1,7 ммоль/л достигаются назначением фибратов [16].
При лечении артериальной гипертензии следует использовать современные клинические рекомендации. Предпочтительными к использованию считаются ингибиторы ангиотензин- превращающего фермента, блокаторы рецепторов ангиотензина, блокаторы кальциевых каналов, удобной представляется комбинация бета-адреноблокатора и тиазидного диуретика. Возможны их сочетания, за исключением сочетания первых двух групп из-за установленного повышенного риска сердечно-сосудистых событий. При низком риске возможно использование монотерапии с титрованием дозы, при высоком риске целесообразно начать лечение с комбинированных препаратов. В дальнейшем проводится увеличение их дозировок, в том числе титрованием двух и более препаратов до достижения максимальной дозы каждым из препаратов. При выявлении резистентной артериальной гипертензии может быть использовано 3—4 и более групп препаратов при достижении максимальной дозы каждым из этих препаратов. Оптимально сочетание ингибитора ангиотензинпревращающего фермента или бло- катора рецепторов ангиотензина в сочетании с блокатором кальциевых каналов в максимальных дозах и тиазидным диуретиком. В дальнейшем тестируется уровень ренинемии. При низких показателях ренина дополнительно назначают блокаторы рецепторов альдостерона, при умеренном повышении — блокатор альфа-адренорецепторов, при высоком уровне целесообразно использовать бета-адреноблокатор.
При анализе электрокардиограмм пациенток с синдромом Шерешевского — Тернера установлено, что часто встречается блокада задней ветви левой ножки пучка Гиса, ускоренное атрио- вентрикулярное проведение и патология зубца Т, происходит укорочение интервала PR и удлинение интервала QT, суррогатного маркера гетерогенности реполяризации, приводящего к фатальному исходу. В связи с этим необходимо тестирование ЭКГ при назначении препаратов, удлиняющих интервал QT [17]. Для скрининга вероятного синдрома удлиненного интервала QT следует использовать соответствующие критерии [18]. При проведении генетического типиро- вания пациенток с синдромом Шерешевского — Тернера установлены связь удлиненного QT с кариотипом 45Х; гены SCN5A и KCNH2 (при большом удлинении QT), а также ген KCNE2 (при малом удлинении QT) [19]. Для выявления группы риска среди кровных родственников по внезапной сердечной смерти у пациентов с синдромом удлиненного интервала QT и для их динамического наблюдения можно использовать адреналиновую пробу. При проведении тестирования следует пользоваться современными рекомендациями Европейского общества кардиологов по диагностике желудочковых аритмий [20]. Все рассмотренные методы поиска синдрома удлиненного QT следует широко применять при консультировании пациенток с синдромом Ше-решевского — Тернера.
В соответствии с современными клиническими рекомендациями, синдром удлиненного QT диагностируется при повторной записи 12-канальной ЭКГ с выявлением QTc >480 мс или при значении более 3 баллов по шкале риска синдрома удлиненного QT. Независимо от продолжительности QT синдром удлиненного QT диагностируется по наличию типичных генетических мутаций. Диагноз синдрома удлиненного QT устанавливается по ЭКГ при QTc >460 мс в повторной 12-канальной ЭКГ у пациентов с необъяснимыми синкопальными эпизодами при отсутствии вторичных причин удлинения интервала QT [20].
Для всех пациенток с синдромом удлиненного QT рекомендуются следующие направления модификации образа жизни: 1) избегать препаратов, удлиняющих интервал QT (https:// www.crediblemeds.org); 2) коррекция дизэлектролитемии (гипокалиемии, гипомагниемии, гипокальциемии) вследствие диареи, рвоты, метаболических нарушений; 3) избегать триггеров генотипической аритмии (плавание с нагрузкой, особенно при LQTS1, и громких звуков при LQTS2). При медикаментозном лечении для клинически диагностированного синдрома удлиненного QT пациенткам рекомендованы бета-адреноблокаторы. При случайных мутациях синдрома удлиненного QT последние должны рекомендоваться при нормальном интервале QT. При предшествоваших остановках сердца при использовании бета-адреноблокаторов имплантация кардиовертера-дефибриллятора рекомендована пациентам с синдромом удлиненного QT. В дополнение к бета-адреноблока- торам следует рекомендовать имплантацию кардиовертера-дефибриллятора у пациенток с синдромом удлиненного QT, перенесших синкопе и/или желудочковую тахикардию при приеме адекватных доз бета-адреноблокаторов. Симпатическая денервация левых отделов должна рекомендоваться при симптомном синдроме удлиненного QT: а) бета-адреноблокаторы неэффективны, имеется непереносимость, противопоказаны; б) терапия путем имплантации кардиовертера-дефибриллятора противопоказана или отклонена; в) пациенткам при использовании бета-адреноблокаторов с отмеченны-ми множественными шоками при терапии имплантированным кардиовертером-дефибрилля- тором [20].
Важным направлением консультативной поддержки пациенток с синдромом Шерешевского — Тернера является период наблюдения при беременности и в родах. Уже 20 лет существует технология фертилизации с помощью донорских яйцеклеток, при этом в США в 1997 г. из 258 женщин в программе помощи 52% получали лечение в связи с синдромом Шерешевского — Тернера [21]. Возможно появление пубертата у 10% пациенток при соматических признаках синдрома Шерешевского — Тернера, при этом спонтанная беременность возможна у 2% женщин этой группы [22]. Течение беременности у них сопровождается увеличением риска материнской смертности в 150 раз относительно общей популяции беременных женщин [23].
При планировании беременности пациентке с синдромом Шерешевского — Тернера сообщают о возможности наследования генетических аномалий при спонтанной беременности, что требует участия в консилиуме специалиста по медицинской генетике. Обсуждается возможность влияния на течение беременности сердечно-сосудистых (артериальная гипертен- зия, преэклампсия, разрыв аорты) и метаболических осложнений (сахарный, гестационный диабет), возможных осложнений при использо-вании медицинских технологий поддержки в родах (в 85% случаях выполняется кесарево сечение). Из-за развития акушерских или сердечно-сосудистых осложнений для плода возможны преждевременные роды, задержка внутриутробного развития и появление потребности в интенсивной терапии, относящейся к новорожденному [24].
Скрининг до беременности включает: обследование кардиолога на наличие врожденного порока сердца с оценкой степени гемодинами- ческих нарушений; проведение ЭКГ, эхоКГ, МРТ, контроль артериальной гипертензии, обследование углеводного обмена (гликемия натощак и НЬА1с), УЗИ абдоминальное и исследование функции печени, почек, тест Papanicolaou и ультразвуковое гинекологическое исследование [25]. Беременность противопоказана при наличии данных анамнеза по хирургическому лечению аорты, диссекции аорты, дилатации аорты с максимальным размером более 25 мм/м2 или 35 мм, коарктации аорты, неконтролируемой артериальной гипертензии (несмотря на проводимое лечение), а также при портальной гипертензии с расширением вен пищевода [24].
К осложнениям со стороны сердечно-сосудистой системы при течении беременности следует отнести диссекцию аорты вследствие врожденного порока и артериальной гипертензии. К выделенным факторам прогрессирования, способствующим проявлению осложнения, отнесены индекс размера аорты более 2,0 см/м2, аномалии сердца — 25—50% случаев, артериальная гипертензия — 40—50%, кариотип 45,Х. Артериальная гипертензия, индуцированная беременностью, способствует появлению пре- эклампсии и эклампсии с осложнениями у матери и плода. При первично выявленной артериальной гипертензии на 50% чаще развиваются преэклампсия, эклампсия, HELLP-синдром [25]. Беременность возможна при размере аорты в диаметре менее 25 мм/м2 или 35 мм, если отсутствует связь с коарктацией аорты. В случае верифицированного увеличения дила- тации аорты на 10% и более следует рекомендовать другие техники визуализации (МРТ, КТ или чреспищеводную эхоКГ). Беременность противопоказана при обнаружении документированного расширения аорты [24].
Координированный сердечно-сосудистый мониторинг и эхоКГ показаны в следующие сроки: по окончании I и II триместров; ежемесячно в III триместре, МРТ рекомендовано при увеличении диаметра аорты на 10% и более между двумя исследованиями эхоКГ. В случае развития дилатации аорты потребуется госпитализация в клинику, имеющую кардиохирургичес- кое отделение и роддом с отделением неонатологии и/или неонатологической реанимации при сроке беременности более 32 нед, кардиологическая и хирургическая консультативная помощь специализированного центра; контроль развития легочной системы плода при родах в сроке 25—34 нед; планирование кесарева сечения. При отсутствии дилатации показано кесарево сечение у 85% пациенток после 34 нед вследствие анатомически узкого таза, в зависимости от состояния сердечно-сосудистой системы. Естественные роды протекают с мо- ниторированием артериального давления, при отсутствии диспропорции размеров плода/таза. Рекомендовано использование пособия при родах (вакуум-экстракция или наложение хирургических щипцов). Роды проводятся при участии команды специалистов, включающей кардиолога и кардиохирурга [24].
Следует оценить отношение риск/польза при назначении следующих препаратов во время беременности: амиодарон, клопидогрель, ингибиторы IIb/IIIa-рецепторов, прасугрела гидрохлорид, пропафенона гидрохлорид, тикагрелор, варфарин. Препараты: аденозин, ацетилсалициловая кислота, бета-адреноблокаторы (исключая атенолол), гидралазин, метилдопа, нитраты, нифедипин, соталол, дигоксин, дилтиа- зем, верапамил, флекаинид, фуросемид, не- фракционированный гепарин — оценены как безопасные для применения во время беременности [26]. Низкомолекулярные гепарины ис-пользуются в программе лечения тромбоэмболии легочной артерии при существующей коа- гулопатии (эноксапарин 1 мг/кг каждые 12 ч или делтапарин 100 МЕ/кг каждые 12 ч; максимальный уровень анти-Ха-активности через 4—6 ч от введения препарата составляет 0,6—1,2 МЕ/мл) [27]. При использовании препаратов, удлиняющих интервал QT, следует дополнительно оценить риск и пользу от их применения при синдроме Шерешевского — Тернера.
В постнатальном периоде сохраняется сердечно-сосудистый риск, вследствие этого следует выполнить мониторирование размеров корня аорты по протоколу обследования на 5-е и 8-е сутки после родов в специализированном сонографическом центре. Во внутриутробном периоде возможно обследование плода путем сонографии и кариотипирования клеток ворсин хориона или амниотической жидкости. Тестирование новорожденного на наличие синдрома Шерешевского — Тернера выполняется при спонтанной беременности [24]. В постнаталь- ный период возможно проведение кариотипи- рования клеток, ПЦР-диагностика и поиск Y-мозаицизма [28].
Современная клиническая кардиологическая практика постоянно совершенствуется благодаря разработке и применению клинических рекомендаций по ведению пациентов с артериальной гипертензией, ишемической болезнью сердца, пороками сердца. Представленные материалы, разработанные зарубежными специалистами, по консультативной кардиологической помощи пациенткам с синдромом Шерешевского — Тернера способствуют формированию обоснованного клинического использования диагностических и лечебных технологий для этой генетически детерминированной па-тологии, сложной при клиническом наблюдении.
Контактная информация:
Казаков Сергей Алексеевич — к. м. н., доцент кафедры кардиологии и ревматологии.
Белорусская медицинская академия последипломного образования.
220013, г. Минск, ул. П. Бровки, 3, корп. 3; сл. тел. 375 17 331-92-82.
Конфликт интересов отсутствует.
Ключевые слова:
артериальная гипертензия, диссекция аорты, ишемическая болезнь сердца, синдром удлиненного QT, синдром Шерешевского-Тернера
Автор(ы):
Казаков С. А.
Медучреждение: Белорусская медицинская академия последипломного образования
Синдром Тернера-Шерешевского: причины бесплодия больных
Если патология не была выявлена в младенчестве, то с большой вероятностью диагноз будет поставлен в пубертатный период. Поводом для обращения к врачу будет заметное отставание в половом развитии девочки. Обследование может показать неправильное формирование половых органов:
- воронкообразный вход во влагалище;
- недоразвитость малых половых губ, девственной плевы и клитора;
- высокая промежность;
- внешний вид больших половых губ больше похож на мошонку;
- патологическая атрофия кожи.
Более того, когда есть подозрение на синдром Шерешевского-Тернера, диагностика может показать, что матка девочки неразвита, вместо яичников присутствуют двухсторонние тяжи фиброзной стромы, а яйцеклетки в них не созревают.
Вторичные половые признаки у таких пациенток выражены слабо. Оволосения в подмышечных впадинах и на лобке у них не наблюдается, молочные железы не формируются должным образом. Большинство больных девушек страдает отсутствием менструаций (аменореей).
Очевидно, что при такой патологии будут затруднения с продолжением рода. Лишь пять процентов пациенток оказываются фертильными и рожают детей без медицинского вмешательства. Чаще, если поставлен диагноз «синдром Шерешевского-Тернера» лечение бесплодия неизбежно.
Список источников
- Дедов И.И., Петеркова В.А., Семичева Т. В., Волеводз Н. Н. Синдром Шерешевского—Тернера. — М., 2002;
- Кравец Е.Б. Клинические лекции по детской эндокринологии. — Томск, Экс Либрис, 2007;
- Петеркова ВА, Безлепкина О.Б., Семичева Т.В., Коледо-ва Е.Б. Синдром Шерешевского-Тернера у детей (клиника, диагностика, лечение). Методические рекомендации. М., 1998;
- Дедов И.И., Петеркова В.А. Детская эндокринология. Руководство по детской эндокринологии. — М., Универсум паблишинг, 2006;
- Панкратова, М.С. Синдром Шерешевского-Тернера в практике педиатра-эндокринолога /Панкратова М.С., Петеркова В.А. //Педиатрия. — 2009. — № 4. — С. 115-121.
Паронихия
Паронихия — гнойное воспаление околоногтевого валика и тканей у основания и по бокам ногтя. Заболевание может быть вызвано Синдром Шерешевского-Тёрнера.
Другой причиной паронихии является — попадание инфекции под кожу в результате травмы, продолжительного воздействия химических веществ либо несоблюдение личной гигиены
Основные сведения
Чёткой связи возникновения синдрома Шерешевского — Тёрнера с возрастом и какими-либо заболеваниями родителей не выявлено. Однако беременности обычно осложняются токсикозом, угрозой выкидыша, а роды часто бывают преждевременными и патологическими. Особенности беременностей и родов, заканчивающихся рождением ребёнка с синдромом Шерешевского — Тёрнера, — следствие хромосомной патологии плода. Нарушение формирования половых желёз при синдроме Шерешевского — Тёрнера обусловлено отсутствием или структурными дефектами одной половой хромосомы (X-хромосомы).
У эмбриона первичные половые клетки закладываются почти в нормальном количестве, но во второй половине беременности происходит их быстрая инволюция (обратное развитие), и к моменту рождения ребёнка количество фолликулов в яичнике по сравнению с нормой резко уменьшено или они полностью отсутствуют. Это приводит к выраженной недостаточности женских половых гормонов, половому недоразвитию, у большинства больных — к первичной аменорее (отсутствию менструаций) и бесплодию. Возникшие хромосомные нарушения являются причиной возникновения пороков развития. Возможно также, что сопутствующие аутосомные мутации играют определённую роль в появлении пороков развития, поскольку существуют состояния, сходные с синдромом Шерешевского — Тёрнера, но без видимой хромосомной патологии и полового недоразвития.
Кариотип 45,(X0)=70 % / 46,(XX)=30 % — мозаичная форма синдрома Тёрнера.
При синдроме Шерешевского — Тёрнера половые железы обычно представляют собой недифференцированные соединительнотканные тяжи, не содержащие элементов гонад. Реже встречаются рудименты яичников и элементы яичек, а также рудименты семявыносящего протока. Другие патологические данные соответствуют особенностям клинических проявлений. Наиболее важны изменения костно-суставной системы — укорочение пястных и плюсневых костей, аплазия (отсутствие) фаланг пальцев, деформация лучезапястного сустава, остеопороз позвонков. Рентгенологически при синдроме Шерешевского — Тёрнера турецкое седло и кости свода черепа обычно не изменены. Отмечаются пороки сердца и крупных сосудов (коарктация аорты, незаращение боталлова протока, незаращение межжелудочковой перегородки, сужение устья аорты), пороки развития почек. Проявляются рецессивные гены дальтонизма и других заболеваний.
Синдром Шерешевского — Тёрнера встречается намного реже, чем трисомия X, синдром Клайнфельтера (XXY, XXXY), а также XYY, что указывает на наличие сильного отбора против гамет, не содержащих половых хромосом, или против зигот XО. Это предположение подтверждается достаточно часто наблюдемой моносомией X среди спонтанно абортированных зародышей. В связи с этим допускается, что выжившие зиготы XО являются результатом не мейотического, а митотического нерасхождения, или утраты X-хромосомы на ранних стадиях развития. Моносомии YО у человека не обнаружено. Популяционная частота 1:1500.
Все регионы мира и культуры затрагиваются данной патологией примерно одинаково. По оценкам, она проявляется у 3% всех плодов человека. Однако только 1% этих плодов выживают после родов.
Причины
Вероятность развития синдрома возрастает, если в предыдущих поколениях были генетические заболевания. Существует ряд других неблагоприятных факторов, ведущих к мутациям в генетической информации. Среди них – хронический алкоголизм отца и матери, неблагоприятное состояние окружающей среды в регионе.
Взаимосвязи между возрастом родителей и развитием заболевания не выявлено. Однако замечено, что беременности с такими патологиями плода обычно протекают с токсикозом, существует угроза выкидыша, ребенок появляется на свет раньше времени. Природа этих особенностей – в хромосомной патологии плода.
Лечение
На первом этапе терапия заключается в стимуляции роста тела анаболическими стероидами и другими анаболическими препаратами. Лечение следует проводить минимальными эффективными дозами анаболических стероидов с перерывами при регулярном гинекологическом контроле. Главным видом терапии больных является эстрогенизация (назначение женских половых гормонов), которую следует проводить с 14—16 лет. Лечение приводит к феминизации телосложения, развитию женских вторичных половых признаков, улучшает трофику (питание) половых путей, уменьшает повышенную активность гипоталамо-гипофизарной системы. Лечение следует проводить в течение всего детородного возраста больных.
Если с помощью гормональной терапии удаётся вырастить до нормальных размеров матку, то беременность у таких больных возможна с помощью ЭКО с донорской яйцеклеткой. Случаи, где сохранились свои яйцеклетки, единичны.
В последнее время для увеличения показателей окончательного роста проводится терапия соматотропином.