Хроническая нехватка железа в организме возникает из-за дефицита железа и характеризуется нарушением синтеза гемоглобина, который содержится в эритроцитах. Первые запасы железа организм человека получает от матери через плаценту, после рождения железо восполняется через прием пищи или железосодержащих препаратов. Выводит железо из организма мочевыделительная и пищеварительная системы, потовые железы и во время менструаций у женщин. В сутки выводится около 2 граммов железа, поэтому, чтобы не допустить истощения запасов, его необходимо постоянно восполнять. По данным ВОЗ, каждая 3-я женщина и каждый 6-й мужчина в мире страдают железодефицитной анемией. В группе риска находятся беременные женщины, дети до 3-х лет и девушки-подростки.
Причины железодефицитной анемии (ЖДА)
- недостаточное поступление железа с пищей: голодание, вегетарианство или обедненная железом и белком диета, соблюдаемая длительное время. У детей на грудном вскармливании причиной может быть железодефицитная анемия матери, ранний перевод на искусственное вскармливание, позднее введение прикорма
- нарушение всасывания железа: энтерит (воспаление слизистой тонкой кишки, вызванное инфекцией или глистной инвазией), гастриты и язвенная болезнь желудка и двенадцатиперстной кишки; наследственные заболевания (муковисцидоз и целиакия); аутоиммунное поражение слизистой кишечника и возможно желудка (болезнь Крона); состояние после удаления желудка и/или двенадцатиперстной кишки; рак желудка и кишечника
- хронические кровопотерь. Это самая основная причина. Сюда относятся потери вследствие: язвенной болезни желудка и двенадцатиперстной кишки, неспецифического язвенного колита, болезни Крона, геморроя и анальных трещин, полипоза кишечника, кровотечений из распадающихся опухолей любой локализации и варикознорасширенных вен пищевода; геморрагического васкулита; легочных кровотечений, гемосидероза легких; хронического пиелонефрита, поликистоза и рака почек, мочевого пузыря; потери при гемодиализе; миомs матки, эндометриоза, гиперполименореи, рака шейки матки; носовых кровотечений
- врожденный недостаток железа в организме (недоношенность, рождение от многоплодной беременности, тяжелая железодефицитная анемия у матери, патологические кровотечения во время беременности и родов, фетоплацентарная недостаточность)
- алкоголизм (повреждается слизистая желудка и кишечника, затрудняя всасывание железа)
- применение лекарственных средств: нестероидные противовоспалительные средства (диклофенак, ибупрофен, аспирин) уменьшают вязкость крови и могут способствовать возникновению кровотечений, кроме того эти препараты могут провоцировать возникновение язв желудка и двенадцатиперстной кишки; антациды (альмагель, гастал, ренни) уменьшают продукцию соляной кислоты, которая необходима для эффективного всасывания железа; железосвязывающие препараты (десферал), эти препараты связывают и выводят свободное железо и железо в составе ферритина и трансферрина, и при передозировке могут приводить к железодефицитным состояниям
- донорство (при донациях чаще 4х раз в год развивается железодефицитное состояние)
- нарушение синтеза трансферрина. Трансферрин – это транспортный белок железа, который синтезируется в печени
В норме уровень гемоглобина в крови: у женщин – 120-140 г/л, у мужчин – 130-160 г/л
Введение
Анемия — глобальная мировая проблема: примерно 25–30% людей страдают этим заболеванием, при этом половина всех анемий обусловлена дефицитом железа [1, 2]. Диагностическими критериями анемии, по данным ВОЗ, являются показатели гемоглобина ниже 130 г/л у мужчин всех возрастов и женщин в постменопаузе, для небеременных женщин репродуктивного возраста менее 120 г/л, для беременных — менее 110 г/л. Эти стандарты ВОЗ используются врачами большинства стран в целях профессиональной согласованности [3, 4].
По степени тяжести, в соответствии c уровнем гемоглобина (Hb), выделяют анемию легкой степени (Hb≥90 г/л), средней степени (Hb 90–70 г/л), тяжелой степени (Hb 69–50 г/л) и крайне тяжелую анемию (<50 г/л) [5, 6].
Железодефицитная анемия (ЖДА) — приобретенное заболевание, которое характеризуется сниженным содержанием железа в сыворотке крови, тканевых депо, костном мозге, в результате чего развиваются гипохромия и трофические расстройства в тканях [7–9]. ЖДА — одно из самых распространенных патологических состояний в мире, а у женщин детородного возраста оно стоит на первом месте по встречаемости [7].
Клинические проявления ЖДА
Анемический синдром — происходит из-за снижения уровня эритроцитов и гемоглобина крови, снижая насыщения клеток и тканей кислородом. Признаки анемического синдрома сложно распознаваемые, но помогают заподозрить наличие анемии и в комплексе с данными других обследований поставить диагноз. Это общая слабость, высокая утомляемость и снижение работоспособности, головокружение, шум в ушах и мелькание «мушек» перед глазами, периодическое учащенное сердцебиение, одышка при незначительной физической нагрузке, обморочные состояния. При осмотре выявляются бледность кожного покрова и видимых слизистых, небольшие отеки голеней, стоп, лица (преимущественно области вокруг глаз), тахикардия, различные варианты аритмии, умеренные шумы в сердце, приглушенность сердечных тонов.
Сидеропенический синдром — вызван дефицитом железа в тканях, что вызывает снижение активности многих ферментов (белковые субстанции, регулирующие многие жизненные функции), проявляется многочисленными симптомами:
- изменение вкуса (желание употреблять в пищу необычные продукты: песок, мел, глину, зубной порошок, лед, а также сырой фарш, непропеченное тесто, сухие крупы)
- склонность к употреблению острой, соленой, пряной пищи
- извращение обоняния (привлекают запахи бензина, ацетона, запах лаков, красок, извести)
- снижение мышечной силы и атрофия
- сухость, шелушение кожа; ломкость и выпадение волос; тусклость, поперечная исчерченность, ложкообразная вогнутость ногтей; долго не заживают мелкие травмы, ссадины
- сухость и трещины в углах рта у 10-15% больных
- чувство распирания языка, покраснение и атрофия, частые пародонтозы и кариес
- сухость слизистой пищевода, что вызывает боли при глотании и затруднение при глотании твердой пищи, развитие атрофического гастрита и энтерита
- неотложные позывы к мочеиспусканию, невозможность удержать мочу при кашле, смехе, чихании, эпизоды ночного недержания мочи
- симптом «синих склер» характеризуется голубоватой окраской склер
- длительное повышение температуры тела до субфебрильных цифр (37.0-37.9°С) без видимых причин
- частые ОРВИ
Почему возникает анемия
Причины возникновения малокровия:
- нарушения обмена веществ, участвующих в кроветворении – железа, витаминов В6 и В-12;
- слабость кроветворной системы;
- увеличение потребления железа и витаминов организмом;
- кровопотеря;
- наследственные аномалии эритроцитов;
- болезни ЖКТ, приводящие к нарушению всасывания микроэлементов и витаминов;
- инфекции;
- иммунные патологии;
- распад красных кровяных телец;
- острые и хронические (профессиональные) отравления;
- облучение
Существуют состояния, при которых необходимо проведение периодического лабораторного обследования на анемию:
- хронические патологии кроветворения, ЖКТ сердца, печени, почек;
- период беременности и лактации;
- геморрой, гиперменорея, миома и другие недуги, сопровождающиеся кровотечениями;
- детский возраст;
- период полового созревания;
- недавно перенесенные операции или травмы, сопровождавшиеся значительной кровопотерей;
- профессиональные занятия спортом;
- системные заболевания – волчанка, ревматизм, васкулиты;
- инфекции;
- состояние после переливания крови;
- соблюдение строгих диет;
- перенесённые облучение и химиотерапии;
- работа на вредных производствах.
Диагностика ЖДА
- клинический анализ крови: снижение уровня гемоглобина, эритроцитов, уменьшение содержания гемоглобина в одном эритроците, часто увеличение СОЭ
- биохимический анализ крови: снижение уровня сывороточного железа, увеличение общей железосвязывающей способности сыворотки, снижение содержания ферритина в сыворотке крови
Если в организме пациента с помощью анализов выявлен дефицит железа, то следующим этапом станет поиск причин этого дефицита. Для выявления причины железодефицита проводится комплексное обследование, включающее в себя эзофагогастродуоденоскопию, ректороманоскопию, колоноскопию, бронхоскопию, рентгенографию органов грудной клетки, УЗ-исследование органов брюшной полости, малого таза и почек, осмотр гинекологом, урологом, гематологом, анализ кала на скрытую кровь и яйца гельминтов, а также исследование красного костного мозга из грудины или подвздошной кости (стернальная пункция, трепанобиопсия).
Изменения в анализе крови при анемии
Для диагностики анемии и установления ее разновидности сдаётся кровь из пальца и вены. При некоторых видах анемий проводится анализ мочи на желчные пигменты, образующиеся в результате распада эритроцитов и сопутствующего поражения печени.
В крови определяют:
- Содержание эритроцитов и гематокрита;
- Концентрацию ретикулоцитов;
- Наличие эритроцитов неправильной формы, состава и размера;
- Цветовой показатель (ЦП), по этому признаку анемии делятся на три типа: гипохромные – ЦП понижен; нормохромные — ЦП не изменен; гиперхромные – ЦП увеличен.
- Концентрацию сывороточного железа. По этому признаку анемии делят на три типа: нормосидеремические — показатель в норме; гипосидеремические –концентрация железа меньше нормы; гиперсидеремические – содержание железа увеличено.
- Насыщение кровяной сыворотки трансферином – белком, транспортирующим железо, для образования эритроцитов;
- Содержание лейкоцитов. При анемии может изменяться как общий показатель, так и содержание лейкоцитов какого-либо типа (лимфоцитов, моноцитов, эозинофилов, базофилов);
- Концентрацию билирубина и гаптоглобина;
- Средний диаметр эритроцитов (СДЭ). Анемии бывают: нормоцитарными, красные тельца нормальны; микроцитарными – размер эритроцитов уменьшен; макроцитарными и мегалобластными – обнаруживаются неестественно большие красные кровяные клетки.
Осложнения ЖДА
Осложнения возникают при длительном течении анемии без лечения и снижают качество жизни пациента: снижение иммунитета, учащение сердцебиения, которое ведет к сердечной недостаточности; у беременных — повышается риск преждевременных родов и задержки роста плода; у детей- недостаток железа обуславливает задержку роста и развития; редким и тяжелым осложнением является гипоксическая кома; гипоксия из-за недостатка железа осложняет течение уже имеющихся сердечно-легочных заболеваний (ИБС, бронхиальная астма, хроническая ишемия головного мозга и др.) до развития неотложных состояний, таких как острый или повторный инфаркт миокарда и острое нарушение мозгового кровообращения (инсульт).
Геморрагическая анемия
Этот вид малокровия бывает острым, возникшим из-за массивной кровопотери вследствие операции, выкидыша, внематочной беременности, тяжелых родов. Анемия может быть хронической, вызванной незначительными, но частыми кровотечениями.
Содержание эритроцитов падает менее 3,5·1012л, сразу после потери большого количества крови показатель может быть существенно снижен вплоть до 2,1 1012л. Уменьшается содержание гемоглобина – чем ниже этот показатель, тем тяжелее анемия.
Средний объем эритроцита, снижается. В крови увеличивается содержание недоразвитых или деформированных красных телец, которые не могут правильно функционировать. Количество незрелых эритроцитов – ретикулоцитов увеличивается, поскольку красные кровяные тельца не успевают созревать.
Количество лейкоцитов в крови падает, ведь при кровопотере теряются не только эритроциты, но и белые тельца.
Лечение ЖДА
К основным принципам терапии железодефицитной анемии относятся устранение причины, вызвавшей железодефицит, коррекция рациона питания, восполнение железодефицита в организме.
- Диета при железодефицитной анемии представляет собой употребление продуктов, богатых железом. Пациентам показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Из растительных продуктов богаты железом фасоль, бобы, чечевица, горох, шпинат, цветная капуста, картофель, морковь, свекла, бананы, абрикосы, персики, яблоки, черника, малина, клубника, миндаль и грецкие орехи. Следует помнить, что усилению всасывания железа в ЖКТ способствует аскорбиновая кислота, которая содержится в болгарском перце, капусте, шиповнике, смородине, цитрусовых, щавеле, а ухудшают всасывание железа — оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и другие вещества. Однако сколько бы мы ни ели мяса, в кровь из него за сутки попадет всего 2,5 мг железа — именно столько способен усвоить организм. А из железосодержащих комплексов всасывается в 15—20 раз больше — вот почему с помощью одной только диеты проблему анемии не всегда получается решить, в связи с чем назначаются железосодержащие препараты
- Пероральные препараты железа отличаются от других лекарственных средств особыми правилами приема: — железосодержащие препараты короткого действия не употребляют непосредственно перед едой и во время ее. Лекарство принимают спустя 15- 20 минут после приема пищи или в паузе между приемами, пролонгированные лекарственные средства (сорбифер дурулес, тардиферрон-ретард и др.) можно принимать и перед едой, и на ночь (1-2 раза в сутки); — препараты железа не запиваются молоком и напитками на основе молока (кефир, ряженка, простокваша) – они содержат кальций, который будет тормозить всасывание железа — таблетки (за исключением жевательных), драже и капсулы не разжевываются, проглатываются целиком и запиваются большим количеством воды, отваром шиповника или осветленным соком без мякоти Пероральные препараты железа (в таблетках, каплях, сиропе, растворе) являются стартовым лечением при анемии легкой и средней тяжести, при наличии беременности прием согласуется с акушером-гинекологом. Длительность лечения составляет 4–8 недель до нормализации уровня гемоглобина, затем препарат принимают в течение 4–6 недель в половинной дозе. Наиболее часто назначаются: — сорбифер дурулес/фенюльс 100 мг по 1-2 таблетки 1-2 раза в сутки до восстановления уровня гемоглобина (у беременных для профилактики 1 таблетка 1 раз в сутки, для лечения 1 таблетка 2 раза в сутки) — ферретаб комп. 1 капсула в сутки, максимально до 2-3 капсул в сутки в 2 приема, минимальный срок приема 4 недели — мальтофер/актиферрин бывает в трех лекарственных формах (капли, сироп, таблетки), прием по 40-120 капель/10-30 мл сиропа/1-3 таблетки в сутки в 1-2 приема — тардиферрон 80 мг по 1-2 таблетки в сутки, беременным женщинам по 1 таблетке в сутки II-III триместр — тотема (комбинированный препарат железа, меди и марганца) по 2-4 ампулы в сутки, раствор разводят в 1 стакане воды, прием в течение 3-6 месяцев — ферлатум 15 мл 1-2 флакона в день в 2 приема
- Инъекционные препараты железа (венофер, ликфер, космофер, ферринжект) используются исключительно в стационаре (необходимо иметь возможность оказания противошоковой помощи), противопоказаны при беременности и лактации
- Гемотрансфузия (переливание эритроцитсодержащих компонентов крови) производится при тяжелой анемии, по строгим показаниям и в условиях стационара.
Метаболизм железа
Известно, что железо является важным микроэлементом, который используется главным образом в качестве компонента гема в эритроцитах для транспорта кислорода, в меньшем количестве присутствует в мышцах в виде гем-миоглобина и в печени в виде ферритина [10]. Достаточный его уровень необходим для поддержания физиологического гомеостаза [11]. Вместе с тем избыточный уровень железа может привести к гибели клеток через образование свободных радикалов и перекисное окисление липидов биологических мембран, токсическое повреждение белков и нуклеиновых кислот. Важно, что и дефицит, и перегрузка железом могут иметь катастрофические последствия для организма, поэтому содержание данного микроэлемента жестко регулируется [7, 9, 12–14].
В организме здорового человека содержится около 3–5 г железа, из которого большая часть, 2100 мг, входит в состав клеток крови и костного мозга. Примерно 2,5 г этого железа присутствует в гемоглобине для транспорта кислорода, а еще 2 г хранится в виде ферритина, в основном в костном мозге, печени и селезенке [9]. В костном мозге железо используется для образования гемоглобина, железо печени — главный резерв микроэлемента, ретикулоэндотелиальные клетки селезенки удаляют старые эритроциты. Наконец, относительно небольшое количество железа (примерно 400 мг) присутствует в клеточных белках, таких как миоглобин и цитохромы, и примерно 3–4 мг связано с трансферрином, находясь в циркуляторном русле [10, 15]. Практически все метаболически активное железо находится в связанном с белками состоянии, а свободные ионы железа могут присутствовать в крайне низких концентрациях.
В естественных условиях ежедневно теряется не более 0,05% (<2,5 мг) от общего количества железа за счет слущивающегося эпителия кожи и желудочно-кишечного тракта (ЖКТ), в результате потоотделения [12, 13, 16, 17]. Процессы всасывания, рециркуляции и хранения запасов железа регулируются специальным гормоном — гепсидином, который продуцируется клетками печени. В физиологических условиях продукция гепсидина контролируется сложным взаимодействием сигналов, прежде всего уровнем железа в крови и степенью оксигенации ткани печени. При патологических условиях его продукция регулируется провоспалительными цитокинами, из которых главную роль играет интерлейкин-6 [7, 12, 13, 18].
Дефицит железа выявляется у людей всех возрастных и социальных групп, но чаще у женщин репродуктивного возраста, детей раннего возраста и пожилых людей [5, 6]. К основным причинам развития дефицита железа следует отнести снижение потребления пищи, уменьшение всасывания и кровопотерю. В развитых, богатых ресурсами странах рацион питания взрослых людей почти всегда адекватен, и наиболее распространенной причиной железодефицита является кровопотеря [2, 6].
Прогноз и профилактика железодефицитной анемии
В большинстве случаев железодефицитная анемия поддается успешной коррекции. Однако при неустраненной причине железодефицит может повторяться или прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития.
В целях профилактики железодефицитной анемии необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов.
Железорефрактерная анемия
Железорефрактерная (sideroblastnaya, sideroahristicheskaya) анемия возникает из-нарушений впитывается железа, возникающего при наследственных патологиях, системных болезнях, нарушениях обмена веществ, хронических отравлениях, злокачественных опухолях.
При этом заболевании содержание сывороточного железа в крови достигает 225—260 мкмоль/л. Избыток откладывается в сидеробластах и сидероцитах – клетках спинного мозга, количество которых может доходить до 70%. В органах формируются образования – гемосидерозы, состоящие из железистых соединений.
Неправильный обмен железа мешает выработке эритроцитов, концентрация которых падает до 1,0 •1012 /л., а гемоглобин может составлять менее 30 г/л. Снижается и цветовой показатель
Количество ретикулоцитов увеличивается. В крови обнаруживаются макроциты – крупные незрелые эритроциты, неполноценные и уродливые кровяные тельца.
Гипопластическая анемия
Это тип анемии вызывают инфекции, наследственные патологии, отравления промышленными ядами, истощение костного мозга, болезни иммунной и эндокринной систем, облучение.
Такая форма малокровия вызвана слабостью кроветворения. Элементы крови имеют нормальную форму и размер, но их количество меньше нормы. Возникает панцитопения – состояние, вызванное гибелью клеток, из которых должны формироваться эритроциты. Плохой прогностический признак – снижение количества нейтрофилов ниже 0,5 • 109/л.
Количество тромбоцитов тоже уменьшено, поэтому кровь плохо сворачивается. В анализах обнаруживается ускорение СОЭ, увеличение концентрации сывороточного железа, билирубина.
В клеточном содержимом костного мозга наблюдается опустошение, вызванное угнетением кровяных клеток.
Железодефицитные состояния при гинекологических заболеваниях и способы их коррекции
Железодефицитная анемия (ЖДА) — гематологический синдром, характеризующийся нарушением синтеза гемоглобина вследствие дефицита железа. В основе анемии лежит тканевая гипоксия, развивающаяся в результате снижения количества гемоглобина вследствие кровопотери, нарушения образования эритроцитов, их деструкции или сочетания этих причин [1, 2].
Дефицит железа встречается почти у 1/3 жителей Земли, а железодефицитная анемия составляет 80–90% среди всех анемий. Распространенность анемий различается от пола, возраста, климато-географических и эколого-производственных причин [1, 3, 4].
Соответствующий дефицит развивается, когда потери железа превышают его поступление 2 мг/сут, и наблюдается при различных физиологических состояниях и заболеваниях [5, 6].
Железодефицитная (гипохромная, микроцитарная) анемия обычно возникает вследствие снижения ресурсов железа в организме при хронической кровопотере или недостаточном внешнем поступлении железа.
Наиболее уязвимы по развитию железодефицитных состояний женщины репродуктивного возраста вследствие ежемесячной физиологической кровопотери во время менструации, беременные по причине высокой потребности в микроэлементах, дети и подростки — из-за высоких потребностей растущего организма, пожилые люди, страдающие хроническими заболеваниями и имеющие плохое питание.
Железо является незаменимым микроэлементом, играющим важную роль в функционировании клеток многих систем организма, основная из которых — участие железа в процессах тканевого дыхания. Общее количество железа в организме женщины достигает 2–3 г, а его концентрация — 40–50 мг на кг массы тела.
Различают два вида железа: гемовое и негемовое. Гемовое железо входит в состав гемоглобина, содержится лишь в мясных продуктах, легко всасывается, и на его всасывание практически не влияет состав пищи.
Негемовое железо находится в свободной ионной форме — двухвалентного или трехвалентного железа. Абсорбция негемового железа (содержится преимущественно в овощах), на которое приходится до 90% железа всего рациона, находится в зависимости от целого ряда факторов. Основная часть железа входит в состав гемоглобина и миоглобина — 70%; депо железа — 18% (внутриклеточное накопление в форме ферритина и гемосидерина); функционирующее железо — 12% (миоглобин и содержащие железо энзимы); транспортируемое железо — 0,1% (железо, связанное с трансферрином) [7–9].
К наиболее важным железосодержащим соединениям относятся: гемопротеины, структурным компонентом которых является гем (гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза), негемовые ферменты (сукцинатдегидрогеназа, ацетил-КоА-дегидрогеназа, ксантиноксидаза), ферритин, гемосидерин, трансферрин.
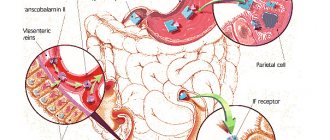
В слизистой оболочке тонкого кишечника из продуктов питания усваивается только двухвалентное негемовое железо. Чтобы железо могло связаться с белками и поступить в клетку, трехвалентное железо восстанавливается в двухвалентное в присутствии кислой среды, основную роль в этом процессе в большинстве случаев играет аскорбиновая кислота [10–13]. Затем для поступления в плазму крови и связывания с трансферрином железо вновь окисляется до трехвалентного. В связанном с трансферрином состоянии железо доставляется тканям посредством эндоцитоза, где оно либо утилизируется клеткой, либо откладывается в составе ферритина. В составе ферритина железо хранится в легкодоступной и нетоксичной форме. Уровень ферритина является «золотым» стандартным показателем количества депонированного железа в организме. Каждый микрограмм ферритина соответствует 8 мг депонированного железа и для женщин в норме составляет 15–150 мг/мл [2, 14–16]. Концентрация же сывороточного железа подвержена значительным суточным колебаниям и составляет в среднем у женщин 6,6–26 мкмоль/л. Поэтому ее определение не имеет первостепенного значения [2].
Гемоглобин является транспортным белком для кислорода, содержащим гемовое железо. Гемы объединены в протопорфириновый каркас, в центре которого находится один двухвалентный атом железа. Одна молекула гемоглобина может перенести максимум 4 молекулы кислорода. Таким образом, количество эритроцитов и гемоглобина играет важную роль в транспортировке кислорода [2].
В течении железодефицита выделяют последовательные стадии: латентный дефицит железа, при котором потери железа превышают его поступление без изменений концентрации гемоглобина, и собственно железодефицитную анемию, которую в зависимости от степени выраженности подразделяют на компенсированную, субкомпенсированную и декомпенсированную формы [3].
Концентрация гемоглобина выражается в граммах на литр. Нормальным уровнем гемоглобина у женщин считается 115–145 г/л (MCHC, Mean Corpuscular Hemoglobin Concentration — средняя концентрация гемоглобина в клетке 320–360 г/л), об анемии говорят при снижении гемоглобина ниже 110 г/л. О тяжести течения анемии судят по уровню гемоглобина. По степени выраженности анемии выделяют легкую степень — 90–109 г/л, среднюю степень — 70–89 г/л и тяжелую степень — менее 70 г/л [3, 14, 15].
Кроме того, для железодефицитной анемии характерны снижение гематокрита, гипохромия (MCH, Mean Corpuscular Hemoglobin — среднее абсолютное содержание гемоглобина в одном эритроците), микроцитоз (MCV, Mean Corpuscular Volume — средний обьем эритроцита), гипосидероз (снижение количества сывороточного железа, увеличение общей железосвязывающей способности сыворотки крови, снижение уровня ферритина в сыворотке крови и в гемолизате) [3, 5]. Количество эритроцитов, гематокрита и гемоглобина составляют измеряемые величины, а MCV, MCH, MCHC являются производными этих величин [2].
Клиническая картина анемии обусловлена кислородным голоданием тканей, прогрессирующей гемической гипоксией с последующим развитием вторичных метаболических расстройств. Клинические симптомы появляются по мере возрастания тяжести заболевания: общая слабость, головокружение, головная боль, сердцебиение, одышка, обмороки, снижение работоспособности, бессонница. Симптомы, характерные ЖДА, заключаются в изменении кожи, ногтей, волос, мышечной слабости, извращении вкусовых ощущений. Кожа становится сухой, на ней появляются трещины. Вследствие нарушения обмена каротина при дефиците железа возникает желтизна кожи. Изменяется форма ногтей, они уплощаются, становятся вогнутыми и ломкими. Волосы истончаются, ломаются и обильно выпадают, появляется седина. При ЖДА также возможны симптомы поражения сердечно-сосудистой системы: сердцебиение, одышка, боли в груди и иногда отеки на ногах [6, 14].
Основными компенсаторными механизмами являются циркуляторная и вентиляционная адаптация, включающие увеличение сердечного выброса, вазодилатацию, снижение сосудистого сопротивления, увеличение перфузии тканей, перераспределение крови, увеличение минутного объема дыхания, усиление активности эритропоэтина. Острая, тяжелая и некомпенсированная анемия может привести к циркуляторному коллапсу и шоку [2].
Основной причиной развития железодефицитных анемий у женщин являются кровопотери различной этиологии. Дефицит железа у женщин встречается в 6 раз чаще, чем у мужчин. Значительное количество крови теряется во время менструации, беременности, в родах. При обильных менструациях возможна потеря железа в количестве 50–250 мг железа [2]. Чаще всего гиперполименорея связана с наличием миомы матки, аденомиозом, гиперпластическими процессами эндометрия, дисфункциональными маточными кровотечениями. Метроррагии при миоме матки чаще всего связаны с субмукозной локализацией узлов, при которой увеличивается менструирующая поверхность, повышается проницаемость кровоснабжающих миому сосудов, снижается сократительная способность матки. При миоме замедляется регенерация кровоточащей поверхности матки после десквамации эндометрия. При аденомиозе поражается миометрий матки, что приводит к длительным обильным менструациям и к вторичной железодефицитной анемии.
Нарушения менструального цикла возникают у женщин в различные возрастные периоды. К развитию гиперменструального синдрома могут привести разнообразные причины — сильные эмоциональные потрясения, нарушение питания, авитаминозы, ожирение, профессиональные вредности, инфекционные и септические заболевания, незрелость гипоталамических структур в пубертатном возрасте и инволютивная перестройка в пременопаузе. В значительной части случаев менометроррагии у женщин сопровождаются анемией различной степени тяжести, что способствует развитию трофических нарушений в различных органах и тканях. Профилактика и лечение анемий у женщин с нарушением менструального цикла и органическими гинекологическими заболеваниями являются важнейшими факторами восстановления их здоровья [1, 4, 17].
Независимо от причины менометроррагий (миома, эндометриоз, дисфункция яичников) и необходимости воздействия на соответствующий фактор, требуется длительная терапия препаратами железа для приема внутрь. Доза, режим дозирования и конкретный препарат подбираются индивидуально с учетом содержания железа в препарате, его переносимости и т. д.
При выборе конкретного препарата и оптимального режима дозирования необходимо иметь в виду, что адекватный прирост показателей гемоглобина при наличии ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг двухвалентного железа [18]. Одними диетическими мероприятиями нельзя возместить дефицит железа и достичь лечебного эффекта.
Антианемическая терапия должна проводиться препаратами для приема внутрь и не должна прекращаться после нормализации гемоглобина. Показания для парентерального введения достаточно ограничены: патология кишечника с нарушением всасывания, непереносимость препаратов для приема внутрь, социальные причины (использование у пациентов с изменениями личности, душевнобольных). По данным многих исследований парентеральные формы не имеют преимущества перед пероральными, при этом отмечается большое количество серьезных побочных эффектов [4, 10, 19]. Гемотрансфузии при ЖДА должны проводиться только по жизненным показаниям.
Современные пероральные ферропрепараты представляют собой соли двухвалентного железа (в пищеварительном тракте ионы трехвалентного железа не всасываются) или соединения, состоящие из гидроксид-полимальтозного комплекса трехвалентного железа (механизм всасывания отличается от такового ионных препаратов) [20].
Наивысшей биодоступностью обладает сернокислая соль железа, поэтому в основном в ферропрепаратах содержится сульфат железа [19, 21]. Сульфат железа это наиболее изученная, проверенная форма, хорошо зарекомендовавшая себя при длительном применении, поэтому чаще других входит в состав препаратов для приема внутрь. Обладает наибольшей степенью всасывания из всех препаратов железа.
В процессе всасывания двухвалентного железа в кишечнике большое значение имеет аскорбиновая кислота, которая способствует поддержанию железа в двухвалентной форме, поэтому очень важно ее наличие в препарате [22]. В гемопоэзе существенная роль принадлежит фолиевой кислоте, усиливающей нуклеиновый обмен. Для нормального обмена фолиевой кислоты необходим цианокобаламин, который способствует образованию из нее активной формы. Дефицит этих веществ, часто возникающий при анемиях, связанных с кровопотерями, приводит к нарушению синтеза ДНК в кроветворных клетках, тогда как включение этих компонентов в препарат увеличивает активную абсорбцию железа в кишечнике и его дальнейшую утилизацию. Наличие в лекарственном препарате аскорбиновой и фолиевой кислот, а также цианокобаламина значительно увеличивает скорость синтеза гемоглобина и повышает эффективность терапии железодефицитных состояний и железодефицитной анемии [14, 23, 24].
Перечисленные компоненты, повышающие биодоступность железа, входят в состав комплексного антианемического препарата Ферро-Фольгамма® [24], который был разработан и производится в соответствии с рекомендациями Всемирной организации здравоохранения (1998).
В 1 капсуле содержится 112,6 мг сульфата железа (элементарного железа 37 мг), что является оптимальной дозой для терапии и сокращает частоту побочных эффектов.
Абсорбция железа из препаратов солей (Fe2+) происходит в виде пассивной диффузии согласно градиенту концентрации, не зависит от рН и двигательной активности желудочно-кишечного тракта (ЖКТ), что обеспечивает быстрое насыщение.
Аскорбиновая кислота улучшает всасывание железа в кишечнике, предотвращает его переход из двухвалентной формы в трехвалентную, ускоряет транспортировку железа и его включения в гем, а также участвует в процессе высвобождения железа из депо.
Аскорбиновая кислота необходима для образования и сохранения восстановленной формы фолиевой кислоты — тетрагидрофолиевой кислоты.
В свою очередь фолиевая кислота является важнейшим фактором для синтеза ДНК и РНК, метаболизма белков и образования красных кровяных клеток, а также выступает дополнительным стимулятором эритропоэза и гемопоэза [21, 23, 25].
Цианокоболамин необходим для образования гемоглобина, эритроцитов, метаболизма белков, жиров, углеводов, производства энергии.
Ферро-Фольгамма® обладает высокой эффективностью, обеспечивая прирост гемоглобина в среднем 2,5 г/л/сут (наибольшая скорость прироста гемоглобина среди препаратов сульфата железа). При использовании препарата Ферро-Фольгамма® ослабление клинической симптоматики постгеморрагической анемии отмечается в течение первых 10 дней приема [6].
Ферро-Фольгамма® назначается по 1 капсуле 3 раза в день после еды в течение 3–4 недель при легкой форме анемии, при средней форме — по 1 капсуле 3 раза в день 8–12 недель, а при тяжелых формах анемии — по 2 капсулы 3 раза в день в течение 16 недель и более. Во время беременности назначается для профилактики недостаточности фолиевой кислоты и железа по 1 капсуле 3 раза в день во II и III триместрах, в послеродовом периоде во время кормления грудью.
После прекращения лечения препаратом Ферро-Фольгамма® положительный эффект и стабилизация показателей сыворотки крови (уровень гемоглобина, эритроцитов, сывороточного железа, общая железосвязывающая способность сыворотки крови) гарантированно сохраняются минимум на протяжении одного месяца [4].
Активные компоненты препарата Ферро-Фольгамма® находятся в специальной нейтральной оболочке, которая обеспечивает их всасывание в верхнем отделе тонкой кишки, что исключает раздражающее действие на желудок. Компоненты растворены в рапсовом масле, которое позволяет улучшить всасывание железа и одновременно снизить раздражающее влияние железа на слизистую оболочку желудка, способствуя хорошей переносимости препарата со стороны пищеварительного тракта [1, 13]. Благодаря отсутствию агрессивного действия на слизистую оболочку ЖКТ Ферро-Фольгамма® может с успехом применяться для коррекции анемического синдрома, при дефиците витамина В12 и фолиевой кислоты на фоне нарушения всасывания в ЖКТ (атрофия слизистой желудка и двенадцатиперстной кишки).
Кроме того, Ферро-Фольгамма® эффективно применяется при сочетанных железо-фолиево-В12-дефицитных анемиях, вызванных хроническими кровопотерями, хроническим алкоголизмом, инфекциями, приемом противосудорожных и пероральных контрацептивных препаратов, анемии во время беременности и кормления грудью.
Эффективность препарата Ферро-Фольгамма® для лечения и профилактики железодефицитной анемии при хорошей переносимости и благоприятных фармакоэкономических характеристиках (стоимость/доза железа/эффективность) была доказана в нескольких российских исследованиях, которые включали широкий круг пациентов, в т. ч. беременных и женщин с гинекологическими заболеваниями [4, 18, 19]. Показаниями к назначению препарата Ферро-Фольгамма® являются анемии, вызванные сочетанным дефицитом железа, фолиевой кислоты и витамина B12, возникающие на фоне хронических кровопотерь (мено- и метроррагий и др.), а также при хроническом алкоголизме, инфекционных заболеваниях, приеме противосудорожных средств и пероральных контрацептивов. Препарат разрешен для профилактики и лечения дефицита железа и фолиевой кислоты во II и III триместрах беременности, в послеродовом периоде и во время лактации.
Таким образом, антианемическая терапия с применением препарата Ферро-Фольгамма® с оптимальным содержанием железа является высокоэффективной с быстрой скоростью прироста гемоглобина (полная клиническая и гематологическая ремиссия у 93% пациенток после 3 недель терапии). Отмечается хорошая переносимость — отсутствие побочных эффектов у 95% пациентов, аллергических реакций и отрицательного влияния на организм женщин, а также стабильность достигнутых результатов и сохранение положительного эффекта в течение месяца после лечения, что позволяет рекомендовать препарат Ферро-Фольгамма® широкому кругу пациентов.
Литература
- Стенограмма научного симпозиума «Железодефицитные состояния в акушерстве и гинекологии». III Российский форум «Мать и дитя». М., 2001, 29.
- Хук Р., Брейман К. Анемия во время беременности и в послеродовом периоде. М., 2007, 74.
- Городецкий В. В., Годулян О. В. Железодефицитные состояния и железодефицитная анемия: диагностика и лечение. Методические рекомендации. М.: Медпрактика-М, 2005; 28.
- Коноводова Е. Н., Докуева Р. С.-Э., Якунина Н. А. Железодефицитные состояния в акушерско-гинекологической практике // РМЖ. 2011; 20: 1228–1231.
- Долгов В. В., Луговская С. А., Морозова В. Т., Почтарь М. Е. Лабораторная диагностика анемий. М., 2001. С. 84.
- Козловская Л. В. Гипохромные анемии: дифференциальный диагноз и лечение // Новый мед. журн. 1996; 56: 8–12.
- Шехтман М. М. Руководство по экстрагенитальной патологии у беременных. М., 2005, 816, 373–399.
- Johnson-Wimbley T. D., Graham D. Y. Diagnosis and management of iron deficiency anemia in the 21 st century // Therap. Adv. Gastroenterol. 2011; 4 (3): 177–184.
- UNICEF/UNU/WHO. Iron Deficiency Anemia: Assessment, Prevention, and Control. A Guide for Programme Managers. Geneva: WHO/NHD, 2001.
- Аркадьева Г. В. Диагностика и лечение железодефицитных состояний. Учебно-методическое пособие. М.: 1999: 22–25.
- Бурлев В. А., Гаспаров А. С. и др. Эпокрин в лечении железодефицитной анемии у больных миомой матки после гистерэктомии // Проблемы репродукции. 2003; 6: 59–64.
- Касабулатов Н. М. Железодефицитная анемия беременных // РМЖ. 2003; 11, 1: 18–20.
- Лебедев В. А., Пашков В. М. Принципы терапии железодефицитной анемии у гинекологических больных // Трудный пациент. 2013, 11, 11: 3–7.
- Дворецкий Л. И., Заспа Е. А. Железодефицитные анемии в практике акушера-гинеколога // РМЖ. 2008; 29.
- Казюкова Т. В., Самсыгина Г. А., Калашникова Г. В. и др. Новые возможности ферротерапии железодефицитной анемии // Клин. фармакология и терапия. 2000; № 9 (2): 88–91.
- Pasricha S. R., Flecknoe-Brown S. C., Allen K. J. et al. Diagnosis and management of iron deficiency anaemia: a clinical update // Med. J. Aust. 2010; 193 (9): 525–532.
- Fernаndez-Gaxiola A. C., De-Regil L. M. Intermittent iron supplementation for reducing anaemia and its associated impairments in menstruating women // Cochrane Database Syst. Rev. 2011. 12. CD009218.
- Бурлев В. А., Коноводова Е. Н., Орджоникидзе Н. В., Серов В. Н., Елохина Т. Б., Ильясова Н. А. Лечение латентного дефицита железа и железодефицитной анемии у беременных // Российский вестник акушера-гинеколога. 2006. № 1. C. 64–68.
- Верткин А. Л., Годулян О. В., Городецкий В. В., Скотников А. С. Железодефицитная анемия и выбор препарата для ее коррекции // Русский медицинский журнал. 2010. № 5.
- Грацианская А. Н. Железодефицитная анемия: Ферро-Фольгамма // РМЖ. 2013; № 29.
- Arvas A., Gur E. Are ferric compounds useful in treatment of iron deficiency anemia? // Turk J Pediatr. 2000. Vоl. 42 (4). Р. 352–354.
- Teucher B., Olivares M., Cori H. Enhancers of iron absorption: ascorbic acid and other organic acids // Int J Vitam Nutr Res. 2004. Vоl. 74 (6). Р. 403–419.
- Коноводова Е. Н., Бурлев В. А. Ферро-Фольгамма + Эритропоэтин — новые возможности лечения анемии у больных с миомой матки // Фарматека. 2004. № 15 (92). C. 70–73.
- Ферро-Фольгамма. Терапия железом, фолиевой кислотой, витамином В12 и аскорбиновой кислотой. Научный обзор. Wеrwag Pharma. М., 2001.
- Ghinea M. M. Treatment of iron deficiency anemia with Ferro-Folgamma // Rom J Intern Med. 2004. Vоl. 42 (1). Р. 225–230.
А. З. Хашукоева1, доктор медицинских наук, профессор С. А. Хлынова, кандидат медицинских наук М. В. Бурденко, кандидат медицинских наук М. Р. Нариманова О. В. Козлова, кандидат медицинских наук, доцент
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация
Abstract. The role of Ferrum in human organism has been analyzed, mechanisms of its digestion from food, clinical presentations of hypoferric conditions and women’s hypoferric anemia, as well as approaches to therapy and prophylaxis of hypoferric anemia with modern peroral preparations.