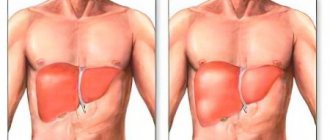
Склеродермия является хроническим аутоиммунным заболеванием, при котором происходит выработка антител к собственным клеткам организма. До конца не изучены точные причины развития заболевания. Существуют предрасполагающие факторы возникновения склеродермии, наличие которых повышает возможность образования очагов склероза. Аутоиммунная болезнь классифицируется в зависимости от степени активности заболевания, а также локализации патологического очага. Склеродермия может поражать кожу и распространяться на внутренние органы. Клинические симптомы заболевания разнообразны. Часто аутоиммунная патология принимается за другие болезни в связи с схожестью признаков.
Диагностика склеродермии не представляет затруднений. Для этого используются метода лабораторного и инструментального исследования. На основании диагностических данных производится подбор индивидуальной терапии. В настоящий момент склеродермия считается неизлечимым заболеванием. Однако, регулярный прием лекарственных средств позволяет минимизировать возможность обострения болезни. Для того, чтобы контролировать течение заболевания, разработаны профилактические меры, включающие рекомендации по образу жизни, трудовому режиму и другим показателям. Прогноз при склеродермии зависит от активности процесса. Чем раньше удалось диагностировать патологию, тем благоприятнее прогноз для жизни. В международной классификации болезней МКБ-10 склеродермия имеет код М34.
Юсуповская больница занимается всеми видами диагностики и лечения склеродермии. Высококвалифицированный персонал с помощью современного оборудования в кротчайшие сроки выявляет аутоиммунное заболевание и назначает необходимый объем терапии.
Причины
До сих пор не определены точные причины возникновения склеродермии. Специалисты выделяют предрасполагающие факторы, наличие которых повышает риск возникновения аутоиммунного заболевания. К ним относятся:
- Генетическая предрасположенность. Наличие склеродермии у родственников значительно увеличивает возможность развития заболевания у следующих поколений. Существует теория, согласно которой за формирование аутоиммунного заболевания ответственен дефект гена HLA-9QA1. Мутации генома могут быть врожденными и приобретенными. Развитию генетического дефекта способствуют следующие факторы:
- Радиационное облучение.
- Длительное воздействие ультрафиолетовых лучей.
- Прием некоторых лекарственных средств. Например, цитостатиков.
- Вирусная или бактериальная инфекция.
- Воздействие высоких и низких температур.
- Воспалительный процесс. Биологически активные вещества, вырабатываемые в процессе воспалительной реакции, способны провоцировать тканевые и сосудистые изменения. Проницаемость сосудов увеличивается, усиливается воспалительный процесс. В результате создаются предпосылки для формирования хронического воспаления. Риск возникновения склеродермии увеличивается при присоединении других провоцирующих факторов.
- Иммунные нарушения. Склеродермия является аутоиммунным заболеванием, при котором собственные клетки организма воспринимаются, как чужеродные. Иммунные реакции запускают фактор роста соединительной ткани.
- Инфекционные заболевания. Не существует единого мнения, касаемо участия инфекционных агентов в развитии склеродермии. Специалисты не выделяют конкретного возбудителя, провоцирующего аутоиммунные процессы. Замечено, что у некоторых пациентов с диагностированной склеродермией, определялись фрагменты цитомегаловируса.
- Факторы окружающей среды. Специалисты выделяют теорию, согласно которой существует взаимосвязь между воздействием факторов окружающей среды и возникновением склеродермии. При наличии генетической предрасположенности, воздействие факторов окружающей среды повышает риск развития аутоиммунного заболевания. К основным провоцирующим факторам относятся:
- Химические соединения. Например, кремний, ртуть, бензол, толуол, эпоксидная смола.
- Пищевые добавки. Среди них выделяют L-триптофан, мазиндол, фенфлурамин.
Механизм возникновения склеродермии связан с развитием иммунного ответа против собственных клеток организма. В результате этого формируется воспалительный процесс, истончающий кожные покровы и кровеносные сосуды. Циркулирующие комплексы оседают на внутренних органах, вызывая их поражение. Склеродермия сопровождается образованием склеротических изменений с формированием рубцовой ткани.
Причины системной склеродермии
Заболевание системной склеродермией начинается в результате появления избытка коллагена в коже и других тканях человеческого организма. Коллаген относится к разновидности протеина, он составляет основу кожи и соединительной ткани.
Причины данного явления до конца не установлены, однако многие ученые полагают, что в этом «виновата» наша иммунная система. Она в результате непонятного сбоя запускает механизм, стимулирующий чрезмерную выработку коллагена (белка соединительной ткани).
Факторами риска появления системной склеродермии могут являться:
- пол человека (женщины заболевают этой патологией в 4 раза чаще, чем мужчины);
- расовая принадлежность (люди с темной кожей страдают этой болезнью намного чаще, чем белокожие);
- внешние факторы, провоцирующие возникновение болезни (переохлаждение, воздействие химических веществ, некоторых видов лекарственных препаратов, длительный стресс и др.).
Симптомы
Склеродермия характеризуется поражением различных органов и систем. В связи с этим сопровождается разнообразной клинической симптоматикой. Выраженность признаков заболевания зависит от степени активности болезни и ее формы. Общими для всех видов склеродермии являются следующие симптомы:
- Болевой синдром в мышцах и суставах.
- Слабость, резкий упадок сил.
- Головная боль, головокружение.
- Возможно появление одышки и изжоги.
По степени распространенности склеротического процесса выделяют 2 формы заболевания:
- Системная. Склеродермия сопровождается распространением роста очагов склероза в толще кожи, а также внутренних органах. В связи с этим происходит их повреждение и функциональные расстройства.
- Ограниченная. Склеротические очаги располагаются в коже, редко в мышцах и костях. Процесс затрагивает кровеносные сосуды. Ограниченная склеродермия классифицируется в зависимости от формы очага. В соответствии с этим выделяют:
- Бляшечная склеродермия. Самая распространенный вид заболевания. Очаги склероза имеют небольшой размер. По мере прогрессирования заболевания происходит их разрастание. Кожа в области патологического очага становится плотной.
- Линейная склеродермия. Данная форма аутоиммунной болезни локализуется в волосистой части головы. Наиболее часто линейная склеродермия встречается у детей. Единственный очаг склероза постепенно разрастается. Внешне он напоминает рубец.
- Буллезная склеродермия. Протекает в комбинации с другой формой заболевания. Клиническая картина характеризуется образованием пузырьков на кожной поверхности.
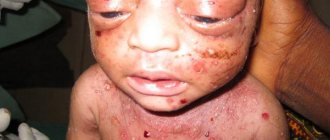
- Ограниченная склеродермия с односторонней прогрессирующей атрофией лица. Тяжелая форма заболевания. Может протекать в виде самостоятельной патологии или в совокупности с другим видом болезни. Очаги склероза поражают половину лица. При этом происходит атрофия кожи, выпадение волос, ресниц, бровей, поражение нервных волокон. В результате этого лицо приобретает ассиметричный вид. Наиболее часто ограниченная склеродермия с односторонней прогрессирующей атрофией лица встречается в молодом возрасте.
- Болезнь белых пятен. Характеризуется образованием пятен белого цвет небольшого размера. Чаще всего данная форма склеродермии локализуется в области шеи, туловища, слизистых оболочках. Отличительной особенностью белых пятен является розовая окантовка.
В зависимости от локализации очага склероза выделяют поражение следующих органов и тканей:
- Кожа. Развитие склеродермии данной локализации происходит в три стадии:
- Отек. Биологически активные вещества провоцируют расширение кровеносных сосудов. В результате этого происходит увеличение пальцев, кистей, стоп в объеме из-за пастозности. Возможно появление зуда кожи и синюшного оттенка. Продолжительность стадии отека зависит от степени активности процесса. В среднем она составляет несколько недель.
- Уплотнение. В результате разрастания соединительной ткани происходит замещение нормальных клеток патологическими. Очаги склероза определяются в виде плотной, холодной, жесткой поверхности.
- Атрофия. Завершающая стадия склеродермии кожи. При этом происходит полное замещение нормальных клеток патологическими, в результате чего пораженный участок меняет окрас. Кожные покровы в данной области становятся сухими, образуются трещины при воздействии любого травмирующего фактора. Склеродермия кожи наиболее часто локализуется в области рук, предплечий, груди, живота, голеней, стоп.
- Сосуды. Поражение кровеносных сосудов при склеродермии выражается в форме синдрома Рейно. При этом происходит спазм артерий, вызывающий характерную симптоматику. Развитие синдрома проходит в три фазы:
- Бледность пальцев. Провоцирующий фактор (например, холод) вызывает спазм кровеносных сосудов. Это приводит к микроциркуляторным нарушениям. В результате кожа приобретет бледный цвет, что становится заметно по четкой границе с здоровой областью.
- Посинение. Синюшный цвет пальцы приобретают в результате скопления гемоглобина. При этом в пораженную область не поступают достаточное количество питательных веществ и кислорода.
- Гиперемия. После того, как спазм кровеносных сосудов устраняется, происходит резкий выброс крови к пораженной области. Это приводит к покраснению пальцев. Помимо изменений цвета пальцев, синдром Рейно сопровождается их онемением, ощущение покалывания.
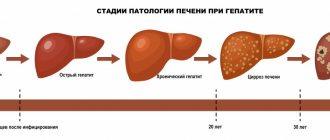
- Печень. Распространение соединительной ткани с формированием очагов склероза провоцирует развитие цирроза печени. Основным симптомом заболевания является желтуха. Она возникает в связи с скопление большого количества билирубина. Со временем появляется зуд кожных покровов, ахоличный кал.
- Легкие. Наиболее опасной локализацией склеродермии являются легкие. В результате образования патологических очагов происходит склерозирование капилляров и альвеол. Это провоцирует нарушения газообмена в легких. Помимо этого, возможно повышение давления в легочной артерии. Подобные изменения характерны для легочной гипертензии. Клинически это выражается появлением следующих признаков:
- Одышка
- Чувство нехватки воздуха
- Боли в грудной области и в правом подреберье.
- Болевого синдрома. Боль локализуется за грудиной.
- Одышки. Признак появляется во время выполнения физической нагрузки.
- Ощущения учащенного сердцебиения.
- Головной боли, головокружения.
- Нарушением ритма сердца. Появляется аритмия.
- Артериальная гипертензия.
- Головная боль, головокружение.
- Тяжесть в голове.
- Неустойчивость походки.
- Отечность нижних конечностей.
- Кратковременная потеря сознания.
- Асцит. Образуется в результате скопления жидкости в области брюшной полости.
- Плеврит. Скопление жидкости в области легких происходит в результате интоксикации продуктами распада.
- Эндокардит. Жидкость в сердце возникает в связи с почечной недостаточностью.
- Анемия, тромбоцитопения.
- Болевой синдром. Локализация боли может быть различной. При этом она усиливается при движении, а также появляется в покое.
- Скованность движений. Симптом возникает в связи с сильным болевым синдромом.
- Атрофия мышц.
- Сгибательная контрактура. Формируется по мере прогрессирования патологического процесса.
- Эректильная дисфункция.
- Частые позывы к мочеиспусканию. Симптом возникает в связи с уменьшением объема мочевого пузыря в результате склероза его тканей.
- Болевой синдром. Очаги склероза вызывают снижение функции вагинальных желез, что выражается в сухости влагалища. При этом возникает боль при половом акте.
- Снижение либидо.
- Раннее наступление климактерического периода.
- Повышенное газообразование, вздутие живота.
- Неустойчивый стул. Понос чередуется с запорами.
- Болевой синдром в области живота.
- Тошнота, рвота. При этом возможно появление примесей крови в рвотных массах.
- Недержание стула.
- Нарушение проходимости пищи. Глотание затруднено в связи с сужением пищевода.
- Рефлюкс. Происходит обратный заброс пищи. Появляется изжога.
Вышеперечисленные симптомы не являются специфичными для склеродермии. Подобные проявления встречаются при других заболеваниях желудочно-кишечного тракта. Поэтому важно обращаться за медицинской помощью при наличии первых признаков патологии для своевременной диагностики.
Для обозначения наиболее часто встречающихся поражений при склеродермии существует CREST-синдром. Он включает в себя:
- C – Calcinosis – Кальциноз. Кальциноз – это плотные подкожные образования, которые представляют собой отложения солей кальция. В некоторых случаях они формируют язвочки, в которые попадают бактериальные агенты способные вызывать инфекционное поражение мягких тканей и костей (остеомиелит).
- R – Raynauld’s phenomen – феномен Рейно. Феномен Рейно возникает из-за спазма периферических сосудов и проявляется нарушением циркуляции крови в пальцах рук и ног. Характеризуется изменением цвета пальцев при воздействии низких температур.
- E – Esophageal dysmotility – нарушение подвижности пищевода. Из-за поражения гладкой мускулатуры пищевода нарушается процесс глотания, у больных возникает непроизвольное срыгивание, появляется изжога.
- S – Sclerodactyly – склеродактилия. Склеродактилия – это патологическое состояние, при котором кожа пальцев утолщена, подкожная клетчатка атрофирована, концевые фаланги увеличены в размерах. На фоне всех этих изменений нарушается подвижность пальцев, сжатие кисти значительно затрудняется.
- T – Telangiecasia – сосудистые звездочки. Из-за поражения капилляров и других мелких кровеносных сосудов кожи на лице, верхней половине тела и на слизистых оболочках рта, глаз и половых органов появляются небольшие красно-синие точки, по своей форме схожие со звездочками.
| Пораженный орган | Механизм действия | Основные симптомы |
| Печень | Распространение соединительной ткани с формированием очагов склероза провоцирует развитие цирроза печени. Желтуха возникает в связи с скоплением большого количества билирубина. | 1.Желтуха. 2.Кожный зуд. 3.Ахоличный кал. |
| Легкие | В результате образования патологических очагов происходит склерозирование капилляров и альвеол. Это провоцирует нарушения газообмена в легких. Помимо этого, возможно повышение давления в легочной артерии. Подобные изменения характерны для легочной гипертензии. | 1.Одышка 2.Чувство нехватки воздуха 3.Боли в грудной области и в правом подреберье. |
| Почки | Склеродермия наиболее часто поражает кровеносные сосуды, в том числе почечные. Подобные изменения приводят к нарушению функции почек и развитию почечной недостаточности. Фильтрация крови ухудшается, что сопровождается скоплением продуктов распада с развитием интоксикационного синдрома. Склеротическое поражение почек вызывает повышение артериального давления. Данный признак считается благоприятным, так как он указывает на нормальную работу сердечной системы. | 1.Артериальная гипертензия. 2.Головная боль, головокружение. 3.Тяжесть в голове. 4.Неустойчивость походки. 5.Отечность нижних конечностей. 6.Кратковременная потеря сознания. 7.Асцит. Образуется в результате скопления жидкости в области брюшной полости. 8.Плеврит. Скопление жидкости в области легких происходит в результате интоксикации продуктами распада. 9.Эндокардит. Жидкость в сердце возникает в связи с почечной недостаточностью. 10.Анемия, тромбоцитопения. |
| Сердце | Соединительная ткань замещает функциональную. В результате этого нарушается функция сердца, отвечающая за перекачку крови. Это приводит к недостаточности кровоснабжения сосудов, тканей и сердца. Возникает венозный застой крови. | 1.Болевой синдром. Боль локализуется за грудиной. 2.Одышка. Признак появляется во время выполнения физической нагрузки. 3.Ощущение учащенного сердцебиения. 4.Головная боль, головокружение. 5.Нарушение ритма сердца. Появляется аритмия. |
| Кости и мышцы | Поражение опорно-двигательного аппарата считается одним из самых частых проявлений склеродермии внутренних органов. | 1.Болевой синдром. Локализация боли может быть различной. При этом она усиливается при движении, а также появляется в покое. 2.Скованность движений. Симптом возникает в связи с сильным болевым синдромом. 3.Атрофия мышц. 4.Сгибательная контрактура. Формируется по мере прогрессирования патологического процесса. |
| Мочевыделительная система | Распространение склеротического процесса редко затрагивает мочеполовую систему. В результате поражения кровеносных сосудов, нарушается микроциркуляция в паховой области. | 1.Эректильная дисфункция. 2.Частые позывы к мочеиспусканию. Симптом возникает в связи с уменьшением объема мочевого пузыря в результате склероза его тканей. 3.Болевой синдром. Очаги склероза вызывают снижение функции вагинальных желез, что выражается в сухости влагалища. При этом возникает боль при половом акте. 4.Снижение либидо. 5.Раннее наступление климактерического периода. |
| Желудочно-кишечный тракт | В результате разрастания соединительной ткани происходит нарушение перистальтики. Очаги склероза приводят к нарушению всасывания питательных веществ. Это приводит к резкой потере массы тела, развитием авитаминоза. | 1.Повышенное газообразование, вздутие живота. 2.Неустойчивый стул. Понос чередуется с запорами. 3.Болевой синдром в области живота. 4.Тошнота, рвота. При этом возможно появление примесей крови в рвотных массах. 5.Недержание стула. 6.Нарушение проходимости пищи. Глотание затруднено в связи с сужением пищевода. 7.Рефлюкс. Происходит обратный заброс пищи. Появляется изжога. |
| Форма | Характеристика | Фото |
| Бляшечная склеродермия | Самая распространенный вид заболевания. Очаги склероза имеют небольшой размер. По мере прогрессирования заболевания происходит их разрастание. Кожа в области патологического очага становится плотной. | |
| Линейная склеродермия | Данная форма аутоиммунной болезни локализуется в волосистой части головы. Наиболее часто линейная склеродермия встречается у детей. Единственный очаг склероза постепенно разрастается. Внешне он напоминает рубец. | |
| Буллезная склеродермия | Протекает в комбинации с другой формой заболевания. Клиническая картина характеризуется образованием пузырьков на кожной поверхности. | |
| Ограниченная склеродермия с односторонней прогрессирующей атрофией лица | Тяжелая форма заболевания. Может протекать в виде самостоятельной патологии или в совокупности с другим видом болезни. Очаги склероза поражают половину лица. При этом происходит атрофия кожи, выпадение волос, ресниц, бровей, поражение нервных волокон. В результате этого лицо приобретает ассиметричный вид. Наиболее часто ограниченная склеродермия с односторонней прогрессирующей атрофией лица встречается в молодом возрасте. | |
| Болезнь белых пятен | Характеризуется образованием пятен белого цвет небольшого размера. Чаще всего данная форма склеродермии локализуется в области шеи, туловища, слизистых оболочках. Отличительной особенностью белых пятен является розовая окантовка. |
Очаговая склеродермия
За последнее десятилетие существенно расширились представления о системных заболеваниях соединительной ткани, среди которых второе место по частоте занимает склеродермия. Заболевание характеризуется системным прогрессирующим поражением соединительной ткани с преобладанием фиброзно-склеротических и сосудистых изменений по типу облитерирующего эндартериита с распространенными вазоспастическими расстройствами [7, 12].
Несмотря на отсутствие официальных статистических данных, можно утверждать, что больных с таким аутоиммунным заболеванием, как очаговая склеродермия, становится все больше и протекает это заболевание агрессивнее [15]. Возможно, это связано с несоблюдением норм диспансеризации и сроков лечения [11].
Дискуссии о взаимосвязи системной (ССД) и ограниченной (ОСД) склеродермии продолжаются. По мнению некоторых авторов ОСД и ССД представляет собой разновидности одного патологического процесса, что подтверждается наличием висцеропатий при ОСД, однонаправленностью метаболических сдвигов, общностью патогистологических изменений кожи при обеих формах болезни, а также случаями трансформации локализованного процесса в прогрессирующий системный склероз [3, 12, 14, 18]. Другие исследователи относят к группе «диффузных болезней соединительной ткани» лишь ССД, считая, что ОСД и ССД — два резко различающихся по клинической картине, течению и прогнозу заболевания. Однако не всегда можно провести четкую границу между очаговым и системным процессом. Клинические наблюдения показали, что поражение кожи как один из первых признаков диффузной склеродермии наблюдается в 61% случаев, а описания трансформации ограниченного процесса, в частности, склероатрофического лихена, в системную склеродермию дают основание предполагать единство этих двух форм. Как свидетельствуют результаты обследования больных ограниченной склеродермией, неблагоприятному течению заболевания с переходом в системный процесс способствуют в основном 4 фактора:
- дебют заболевания в возрасте до 20 или после 50 лет;
- множественная бляшечная или линейная формы заболевания;
- локализация очагов поражения с вовлечением кожи лица или областей над суставами конечностей;
- выраженность дефицита клеточного звена иммунитета, дисиммуноглобулинемии, повышение крупнодисперсных циркулирующих иммунных комплексов и антилимфоцитарных антител [2, 3, 12, 16].
ОСД, так же как и ССД, чаще болеют лица женского пола, например, девочки болеют чаще мальчиков более чем в 3 раза, а женщины в возрасте 40–55 лет составляют 75% больных склеродермией [21]. Заболевание может возникать в любом возрасте, даже у новорожденных, начинаясь обычно без каких-либо субъективных ощущений и нарушения общего состояния. В связи с тенденцией растущего организма к распространению патологии, к выраженным сосудистым реакциям у детей это заболевание часто имеет склонность к обширному поражению, хотя в ранние сроки может проявляться единичными очагами.
Патогенез склеродермии связывают главным образом с гипотезами обменных, сосудистых и иммунных нарушений. На возникновение ОСД влияют также нарушения вегетативной нервной системы и нейроэндокринные расстройства. Принято рассматривать ограниченную склеродермию как своеобразное аутоиммунное заболевание, в основе которого лежат аутоиммунные и воспалительные реакции на различные антигены. В. А. Владимирцев и соавт. (1982) считают, что повышенный уровень коллагеновых белков, являясь источником активной антигенной стимуляции, создает фон, на котором при генетической предрасположенности реализуются аутоиммунные реакции. Возникающий порочный круг взаимовлияния лимфоидных и коллагенсинтезирующих клеток ведет к прогрессированию фиброзного процесса [6]. Установленные нарушения гуморального и клеточного иммунитета у больных склеродермией чаще регистрировались у женщин. Клеточный иммунитет у женщин, в отличие от его гуморального звена, менее активен по сравнению с мужским. Снижение клеточного иммунитета, особенно его супрессорного звена, при повышении активности гуморального иммунитета приводит к тому, что у женщин гораздо чаще, чем у мужчин, развивается аутоиммунный процесс. Прослеживается связь склеродермии с беременностью и менопаузой [21]. В последние годы появились исследования об участии эстрогенов и прогестерона, а также некоторых других гормонов в реакциях синтеза коллагена и других компонентов соединительной ткани. Особое патогенетическое значение при склеродермии придают изменениям микроциркуляции, которые наиболее выражены в период менопаузы. В их основе лежат поражения преимущественно стенок мелких артерий, артериол и капилляров, пролиферация и деструкция эндотелия, гиперплазия интимы [3, 5, 12, 16, 20]. До сих пор обсуждается вопрос о роли наследственности в развитии ОСД. По данным Furst A. (2004) коренные индейцы штата Оклахома в 8 раз чаще болеют склеродермией, чем другие жители Соединенных Штатов. Также более подвержены данной болезни чернокожие люди, они чаще заболевают в детском возрасте и имеют более распространенный процесс по сравнению с белокожими. Однако исследования, проведенные тем же автором, установили, что всего 6% близнецов одновременно болеют склеродермией, и это недостаточно высокий процент заболеваемости среди близнецов, чтобы утверждать чисто генетическую этиологию болезни.
Противоречия данных литературы, вероятно, обусловлены тем, что характер и выраженность иммунологических, эндокринных и обменных сдвигов в значительной степени зависят от течения заболевания в целом и от степени поражения индивидуально [8].
До настоящего времени многие исследователи продолжают поддерживать инфекционную теорию возникновения склеродермии. Развитие склеродермии может быть связано с перенесением таких заболеваний, как грипп, ангина, скарлатина, пневмония. Отдельные авторы рассматривают распространенную склеродермию как позднее проявление боррелиоза (син.: иксодовый клещевой боррелиоз, Лайма болезнь), что подтверждается определением у некоторых больных (особенно бляшечной и склероатрофическими формами) высокого титра иммуноглобулиновых антител к боррелиям Бургдорфера и поразительно быстрым улучшением после лечения заболевания пенициллином. S. Вucher, основываясь на результатах иммунологических исследований и обнаруженных в замороженных биоптатах спирохетоподобных структур, посчитал это подтверждением спирохетной теории возникновения склеродермии [9, 18]. Проведенные наблюдения установили различные кожные проявления Лайм-боррелиоза: бляшечная форма склеродермии (98%), атрофодермия Пазини–Пьерини (80%), анетодермия и хронический атрофический акродерматит (100%) и редко — склероатрофический лихен [4, 9, 16, 18].
В противовес приведенным данным многие исследователи склонны расценивать случаи ограниченной склеродермии с большим титром антител к боррелиям и выявление спирохет — как боррелиоз, протекающий под маской ограниченной склеродермии, а склерозирование кожи — как псевдосклеротические изменения, но ни в коем случае не как проявления истинной склеродермии. По мнению Н. С. Потекаева и соавт. (2006), патогенетическая связь ОСД с болезнью Лайма, также как и атрофодермии Пазини–Перини, синдрома Перри–Ромберга лишь предполагается [17]. Для подтверждения наличия болезни Лайма у больного со склеродермическими очагами целесообразно определение специфических антител в сыворотках больных методами непрямой реакции иммунофлюоресценции (НРИФ), полимеразной цепной реакции (ПЦР), а также выявление боррелий в биоптатах кожи из очагов поражения методом серебрения [9, 18].
Несмотря на разнообразие теорий возникновения ОСД, ни одна из них не раскрывает инициальную причину и взаимодействие факторов патогенеза склеродермического процесса. Наиболее интересными представляются исследования некоторых показателей кальциевого обмена, проведенных Болотной Л. А. и соавт. (2004). Авторы на основании полученных результатов сделали вывод, что изменения кальция и магния, выявленные на всех этапах ОСД, имеют патогенетическое значение. Степень этих расстройств находится в прямой зависимости от активности, формы и длительности дерматоза. Дефект функций клеточных мембран может обуславливать накопление кальция в разных клетках больных ОСД и усиливать синтетическую активность фибробластов, сужение сосудов микроциркуляторного русла, стимуляцию лимфоцитов. Гипомагниемия, выявленная у данных больных, способствует дестабилизации клеточных мембран и может быть одной из причин накопления кальция в эритроцитах, а также обуславливать нарушение функции ряда ферментов [4].
Единой общепринятой классификации ОСД не существует, на наш взгляд, более приемлема классификация С. И. Довжанского (1979), в которой наиболее полно представлены все клинические формы ОСД:
- Бляшечная (дискоидная): а) индуративно-атрофическая; б) поверхностная «сиреневая»; в) узловатая, глубокая; г) буллезная; д) генерализованная.
- Линейная: а) по типу «удара саблей»; б) лентообразная, полосовидная; в) зостериформная.
- 3. Болезнь белых пятен.
- 4. Идиопатическая атрофодермия Пазини–Пьерини.
Избыточное фиброзообразование и нарушение микроциркуляции формируют клиническую картину заболевания, особенности его проявлений. Среди всех клинических разновидностей ОСД наиболее часто встречаемой формой является бляшечная. Для бляшечной склеродермии характерно образование небольшого числа округлых очагов поражения. Очаги в своем развитии проходят три стадии: пятна, бляшки и атрофии. Начинается заболевание незаметно с появления одного или нескольких сиренево-розовых округлых пятен различных размеров. Постепенно центр пятен бледнеет и начинает уплотняться, очаг поражения со временем превращается в очень плотную бляшку характерного желтовато-белого цвета («слоновая кость») с гладкой, блестящей поверхностью. По периферии бляшек некоторое время сохраняется сиреневый венчик, за счет которого происходит их рост и по которому можно судить об активности процесса. Волосы на бляшках выпадают, кожный рисунок сглаживается, пото- и салоотделение прекращается; кожу на пораженном участке нельзя собрать в складку. В таком состоянии очаги могут оставаться на неопределенный срок, а затем постепенно подвергаются атрофии [2, 10, 19].
Более редкой разновидностью ограниченной склеродермии является полосовидная (линейная), наблюдаемая обычно у детей. Отличие от бляшечной склеродермии заключается только в очертаниях очагов — они имеют вид полос и располагаются обычно на конечностях и по саггитальной линии на лбу (напоминают рубец от удара саблей).
Другая разновидность склеродермии — лихен склероатрофический (склеродермия каплевидная, болезнь белых пятен, лишай белый Цумбуша). Предполагают, что он может являться атрофической формой красного плоского лишая, или крауроза; не исключается самостоятельность дерматоза. Однако часто наблюдается сочетание бляшечной склеродермии и склероатрофического лихена, что говорит о единстве этих клинических форм. Высыпания при склероатрофическом лихене представлены мелкими рассеянными или сгруппированными белесоватыми пятнами, иногда с ливидным оттенком, размерами 0,5–1,5 см, чаще локализующиеся на коже туловища и шее, а также на любом участке кожного покрова. Нередко заболевание развивается у девочек и молодых женщин в области половых органов. Встречаются распространенные формы склероатрофического лихена и атипичные варианты; буллезная и телеангиоэктатическая [2, 10, 19]. Для буллезной формы характерно образование пузырей с плотной покрышкой и серозным содержимом. Пузыри могут вскрываться, обнажая эрозии, или ссыхаться в плотную серозную корку. Пузыри свидетельствуют о прогрессировании атрофического процесса, и если на их месте впоследствии образуются эрозии и язвы, процесс трудно поддается терапии. При телеангиоэктатической форме на участках белесоватой атрофии кожи образуются телеангиоэктазии [12].
Склероатрофический лихен вульвы (САЛВ) считается редким заболеванием, однако у детей заболевание встречается не столь редко, как это следует из данных зарубежной литературы. Большинство детей (70%) заболевает в возрасте до 10–11 лет, т. е. до начала пубертатного периода. САЛВ считается заболеванием с неизвестной этиологией и патогенезом, некоторые авторы отмечают участие гормонального фактора в его патогенезе. В частности, Е. А. Бурова (1989) указывает на ведущую роль дисгормональных нарушений в системе гипофиз — надпочечники — яичники. Клиническая картина САЛВ представлена образованием небольших склероатрофических очагов беловато-сероватого цвета, иногда с перламутровым оттенком, блеском, точечными углублениями, фолликулярным кератозом, сиреневым краем. Атрофические изменения наиболее выражены при локализации в области вульвы. Для девочек с САЛВ в связи с низким уровнем эстрогенов характерны более поздние сроки полового созревания, менструальная дисфункция [2, 5, 10, 19].
Атрофодермия Пазини–Пьерини характеризуется немногочисленными пятнами, которые располагаются преимущественно на спине и имеют, как правило, большие размеры (до 10 см и более) и часто неправильные очертания. Заболевание является как бы переходной формой между бляшечной склеродермией и атрофией кожи. Эта разновидность обычно наблюдается у молодых женщин. Высыпания — в виде синевато-фиолетовых пятен с гладким, слегка западающим центром, но без феномена проваливания пальца или грыжевидного выпячивания. Иногда вокруг пятна видно сиреневое кольцо. Характерным признаком этой формы ОСД является длительное отсутствие уплотнения в начале заболевания. В ряде случаев отчетливо выражена пигментация. Одновременно с клиническими проявлениями атрофодермии Пазини–Пьерини могут наблюдаться типичные проявления ОСД [2, 10, 19]. Хотя высказывается мнение, что атрофодермия является самостоятельным заболеванием, все же, по-видимому, правильнее рассматривать ее как клиническую разновидность ОСД, тем более что в ряде случаев атрофия и гиперпигментация предшествуют развитию склероза, который все же появляется на бляшках атрофодермии лишь через несколько лет. Отличие идиопатической атрофодермии от бляшечной склеродермии состоит в том, что при атрофодермии поражается главным образом кожа туловища, а не лица и конечностей, а сам процесс развивается длительно (в течение нескольких лет), очаги поражения представляют собой бляшки почти без уплотнения, синевато-коричневого цвета без лилового кольца по периферии. Полного регресса атрофодермии не наблюдается, в то время как очаг бляшечной склеродермии может исчезнуть полностью (при вовремя начатом лечении) или после него остается легкая атрофия или стойкая пигментация [2, 10, 19].
Одним из редких проявлений склеродермии является гемиатрофия лица Парри–Ромберга — заболевание, характеризующееся прогрессирующей атрофией только одной половины лица, проявляющееся дистрофическими изменениями кожи и подкожной клетчатки, в меньшей степени — мышц и лицевого скелета. Общее состояние больных, как правило, остается удовлетворительным, главной жалобой является косметический дефект в области лица. По данным литературы, среди больных преобладают женщины. В большинстве наблюдений заболевание развивается в возрасте от 3 до 17 лет. Одинаково часто отмечается левосторонняя и правосторонняя локализация процесса. Как правило, заболевание имеет длительное, хроническое течение. Активная стадия длится в основном до 20 лет, в некоторых наблюдениях — до 40 лет. Первыми признаками заболевания являются локальные изменения кожи лица, которая вскоре приобретает желтоватый или синюшный оттенок. Постепенно развивается уплотнение кожи в очагах. В дальнейшем в местах уплотнения кожа атрофируется; с течением времени атрофические изменения прогрессируют с вовлечением в процесс подкожной жировой клетчатки и мышц лица. Наиболее выраженными и частыми признаками поражения кожи являются резкое ее истончение, морщинистость, гиперпигментация диффузного или очагового характера. В атрофированных участках кожи отсутствует рост волос. У больных страдает не только кожа, но и подлежащие мягкие ткани, что, как правило, приводит к грубейшей деформации лица в виде значительной асимметрии его правой и левой половины, наиболее выраженной при дебюте заболевания в раннем детском возрасте. Костные структуры тоже поражаются, если гемиатрофия возникает до окончания их роста. У части больных наблюдается атрофия половины языка. Имеются клинические наблюдения развития прогрессирующей гемиатрофии лица как проявление терминальной стадии у больных с агрессивным течением полосовидной склеродермии на лице. В литературе приводятся данные о результатах обследования больных склеродермией, у 16,7% из которых в последующем развилась лицевая гемиатрофия. Такие случаи дают основание предполагать, что гемиатрофия Ромберга является неблагоприятным вариантом течения ОСД [1].
Диагностика ограниченной склеродермии может представлять определенные трудности, особенно в начальной стадии заболевания. Дифференциальный диагноз ОСД проводят с витилиго, краурозом, недифференцированной формой лепры, синдромом Шульмана.
В начале развития бляшечной склеродермии, когда уплотнение еще не выражено и имеется только обесцвеченное пятно, процесс может напоминать витилиго или депигментированное пятно при недифференцированной лепре. При витилиго пятна имеют более четкую границу, которая хорошо видна при наличии гиперпигментированной зоны. Поверхность пятен гладкая, без признаков атрофии и шелушения. Пятна витилиго сохраняются довольно длительно без уплотнения.
При недифференцированной лепре изменения на коже характеризуются пятнистыми высыпаниями. Последние могут быть эритематозными, различных оттенков (от розового до синюшного) и гипопигментированными. В области пятен болевая, тактильная и температурная чувствительность снижена.
Труднее дифференцировать линейную склеродермию от линейно расположенного келлоидоподобного невуса. Отличительным признаком может служить обнаружение келлоидоподобного невуса в первые месяцы жизни и его длительное существование без выраженных изменений на протяжении многих лет.
Крауроз вульвы может в известной мере напоминать склеродермию, в частности склероатрофический лихен, поскольку при этом заболевании поверхность пораженных участков сухая, блестящая, плотная. Однако при краурозе вульвы имеются интенсивный зуд и телеангиоэктазии. В дальнейшем развиваются атрофия малых и больших половых губ, лейкоплакия и, нередко, рак. Крауроз полового члена проявляется в виде хронической атрофии и сморщивания головки полового члена и внутреннего листка крайней плоти, тогда как склеротические изменения крайней плоти и головки полового члена вызывают фимоз и сужение отверстия мочеиспускательного канала. В противоположность краурозу вульвы, при поражениях полового члена зуд отсутствует и болезнь не осложняется раком.
Синдром Шульмана (син.: эозинофильный фасциит, диффузный фасциит с гипергаммаглобулинемией и эозинофилией). Под этим заболеванием понимают диффузное склеродермоподобное уплотнение кожи, утолщение мышечной фасции, инфильтрацию ее эозинофилами, лимфоцитами и плазматическими клетками. Очаги локализуются чаще на конечностях и приводят к сгибательным контрактурам. Дифференциальными признаками, характерными для синдрома Шульмана, служат отсутствие фиолетового венчика вокруг очага уплотнения и атрофии кожи, а также наличие болевого синдрома и эозинофилия в периферической крови [2, 10, 19].
При локализации очага склеродермии на лице нужно помнить о такой редкой разновидности опухоли, как склеродермоподобная форма базалиомы, при которой патогномоничный для базалиомы узелок медленно увеличивается в размерах, трансформируется в плотную, слегка возвышающуюся над поверхностью кожи бляшку цвета слоновой кости с восковидным блеском, в центральной части которой видны телеангиоэктазии. Границы очага резкие, очертания округлые или неправильные, размеры от 1 до 3 см и более. Эта форма представляет трудность для диагностики, если игнорировать имеющиеся по периферии очага узелки, патогномоничные для базалиомы.
Лечение. Терапия ОСД должна быть многокурсовой и многокомпонентной. При активном процессе количество курсов должно быть не менее 6, с интервалом 1–2 месяца; если процесс стабилизировался, интервал между курсовым лечением увеличивается до 4 месяцев; при остаточных клинических проявлениях и в целях профилактики проводится терапия 2–3 раза в год препаратами, улучшающими микроциркуляцию.
При активном процессе в лечение ОСД следует включать следующие группы препаратов:
- Антибиотики пенициллинового ряда — рекомендуемый курс 15–20 млн ЕД. При непереносимости пенициллина, его можно заменить фузидовой кислотой, оксациллином, ампициллином, амоксициллином, которые необходимо назначать под прикрытием антигистаминных препаратов. Первые 3 курса лечения обязательно должны включать антибиотики.
- Важным препаратом в терапии заболевания является Лидаза, содержащая гиалуронидазу, которая расщепляет гиалуроновую кислоту, являющуюся цементом соединительной ткани. Кроме того, Лидаза увеличивает проницаемость тканей и облегчает движение жидкости в межтканевых пространствах. Лидазу можно заменить алоэ или экстрактом плаценты, Коллализином, Актиногиалом, Лонгидазой.
- Сосудистые средства. В первую очередь — это препараты никотиновой кислоты, обладающие сосудорасширяющим действием, улучшающие углеводный обмен, обладающие гипохолестеринэмической активностью (снижают триглицериды и липопротеинемиды). Ксантинол никотинат (Теоникол, Компламин) — является сочетанием теофиллина и никотиновой кислоты, расширяет периферические сосуды, улучшает мозговое кровообращение, уменьшает агрегацию тромбоцитов. Важно знать, что ксантинол никотинат не рекомендуется назначать в первом триместре беременности, при язве желудка; его также нельзя сочетать с гипотензивными средствами. Также препаратами выбора являются Трентал, Милдронат. При выборе лечебного препарата не следует забывать о фитопрепаратах, улучшающих микроциркуляцию. Получен определенный терапевтический эффект от инъекций Мадекассола (препарат из цинтеллы азиатской) в течение 2–4 недель применения, Мадекассол оказывает менее выраженное антифиброзное, но положительное сосудистое действие. Экспериментальными исследованиями установлено подавление биосинтеза коллагена и компонентов основного вещества соединительной ткани, замедление фиброзообразования под влиянием препарата. Наиболее эффективен Мадекассол у больных с распространенной ОСД, при которой показано одновременное назначение препарата в таблетках и в виде мази. Также из фитопрепаратов рекомендуется Пиаскледин, Эскузан, Берберин по 1 таб. 3 раза в день в течение 1–2 мес.
- Антагонисты ионов кальция. Препараты этой группы обладают специфической способностью тормозить проникновение ионов кальция в миофибриллы и понижать этим активность миофибриллярной АТФазы. Они вызывают расслабление мышечных волокон и уменьшают сопротивление в коронарных и периферических сосудах. Антагонисты ионов кальция улучшают коронарный кровоток и снабжение сердца кислородом, расширяют периферические сосуды и вызывают некоторое понижение системного артериального давления. К препаратам этой группы относятся нифедипин (Коринфар, Фенигидин, Кальцигард ретард), верапамил. Болотная Л. А. (2004) доказала на примере циннаризина (Стугерон) клиническую эффективность антогонистов кальция в лечении ОСД. К «естественным физиологическим блокаторам кальция» также относятся препараты, содержащие магний (Магне В6) [3].
При склероатрофическом лихене к лечению рекомендуется присоединять Ретинол пальмитат 100 000 ЕД в сутки, а местно мази «Солкосерил», «Актовегин», кремы с витамином Е, F.
При единичных очагах поражения можно ограничиться назначением витамина В12 в свечах и фонофореза с Лидазой, Ронидазой, трипсином, хемотрипсином (№ 7–10). Местное лечение ОСД должно состоять из аппликаций наружных средств и физиотерапии. В топической терапии ОСД обычно используются следующие мази: Гепариновая, Гепароид, Троксовазиновая, Бутадионовая, Теониколовая. Препаратами выбора топической терапии являются Димексид, Унитиол, Ронидаза, трипсин, химотрипсин, Лидаза, которые могут применяться в виде аппликаций или вводиться в очаги поражения с помощью электро- и фонофореза. Ронидазу применяют наружно, нанося ее порошок (0,5–1,0 г) на смоченную физиологическим раствором салфетку. Накладывают салфетку на очаг поражения, фиксируя бинтом в течение полусуток. Курс аппликаций продолжают 2–3 нед. Рекомендуется назначать ультрафонофорез Купренила и Гидрокортизона на очаги поражения. При ОСД применяют также магнитотерапию, вакуум-декомпрессию, низкоинтенсивную лазеротерапию. В конце курса терапии можно присоединить массаж очагов поражения. При спаде активности процесса — сероводородные и родоновые ванны [10, 19, 20].
Современные тенденции к уменьшению объема лекарственной терапии способствуют внедрению препаратов, сочетающих в себе несколько терапевтических эффектов. Таким многофакторным действием на организм обладают системные полиэнзимы, представляющие собой стабильную смесь энзимов растительного и животного происхождения, рутина. Обоснованием использования в лечении ОСД «Вобэнзима» (в таблетках и в виде мази) явилось его действие на метаболизм коллагена, способность подавлять образование и расщеплять патологические иммунные комплексы, повышать цитотоксическую активность макрофагов, улучшать микроциркуляцию за счет влияния на тромбоциты и реологические свойства крови, поддерживать нормальное функционирование эндогенных энзимов. Стартовая доза 5 таб. 3 раза в день на фоне основной терапии, далее по показаниям: 3–4 таб. 3 раза в день.
В последние годы широкое применение при лечении различной патологии получила гипербарическая оксигенация (ГБО), способствующая более интенсивному обогащению тканей кислородом, который при повышенном давлении может оказывать также противомикробное действие, особенно в отношении анаэробных микроорганизмов. ГБО увеличивает метаболическую активность митохондрий и их способность к регенерации, нормализует окисление липидов, повышает уровень утилизации кислорода тканями в связи с активацией аэробных процессов в очагах поражения, улучшает микроциркуляцию. На целесообразность использования ГБО при склеродермии указывают ряд авторов [3, 13].
Многие авторы рекомендуют плазмозамещающие препараты декстрана (Декстран, Реомакродекс) [3, 10, 16]. Однако, на наш взгляд, к такой терапии следует прибегать при распространенных, быстропрогрессирующих формах ОСД.
Нами не отмечено значительного эффекта от лечения гормонами, анаболиками и препаратами хинолинового ряда.
В заключение хочется подчеркнуть, что к лечению больных ОСД нужно подходить индивидуально в зависимости от стадии процесса, распространенности, наличия сопутствующих заболеваний. Необходимо объяснить больному целесообразность длительной терапии, тщательного обследования и профилактического лечения.
Литература
- Белоусова Т. А., Колмогорова И. В., Мокина Е. В. Гемиатрофия лица Ромберга: современный взгляд на проблему // Российский журнал кожных и венерических болезней. 1999, № 5. С. 20–23.
- Беренбейн Б. А., Студницин А. А. Дифференциальная диагностика кожных болезней. М.: Медицина, 1989. 672 с.
- Болотная Л. А., Сербина И. М. Современная патогенетическая терапия склеродермии // «Международный медицинский журнал». 1999, № 3. С. 56–58.
- Болотная Л. А., Шахова Ф. Б., Сербина И. М. Новое в патогенезе и терапии ограниченной склеродермии // Вестник дерматогии и венерологии. 2004, № 2. С. 31–34.
- Бурова Е. А. Склероатрофический лихен вульвы у детей, особенности клиники, патогенеза, лечения // Дис. … канд. мед. Наук. М., 1989. 110 с.
- Владимирцев В. А., Авдеева Ж. И., Гусева Н. Г. и др. Изучение клеточного иммунного ответа на коллаген 1 типа у больных системной склеродермией // Вопр. ревмат. 1982, № 1. С. 33–38.
- Гусева Н. Г. Системная склеродермия: клиника, диагностика, лечение // Рос. журн. кож. и вен. болезней. 2002, № 4. С. 5–15.
- Довжанский С. И. Клинико-иммунологические параллели при ограниченной и системной склеродермии // Рос. журн. кожн. и вен. бол. 2002, № 4. С. 26–29.
- Домасева Т. В., Бабкин А. В. Спектр атрофии кожи при Лайм-боррелиозе // Восьмой всероссийский съезд дерматовенерологов. Тезисы научных работ, часть 1. Дерматология. Москва, 2001. С. 176.
- Иванов О. Л. Кожные и венерические болезни // Справочник. М.: Медицина, 1997. 352 с.
- Коробейникова Э. А., Мартынова Л. М., Анисимова А. В. Клинические аспекты ограниченной склеродермии // Рос. журн. кожн. и вен. бол. 2004, № 3. С. 27–29.
- Кряжева С. С., Болдырева М. В. Телеангиоэктатическая форма склероатрофического лихена // Российский журнал кожных и венерических болезней. 1996, № 6. С. 27–29.
- Кряжева С. С., Сапронова Т. И., Булохова Л. М. Гипербарическая оксигинация в комплексной терапии бляшечной склеродермии // Российский журнал кожных и венерических болезней. 1998, № 4. С. 39–41.
- Кряжева С. С., Сапронова Т. И., Булохова Л. М. К проблеме трансформации ограниченных кожных форм склеродермии в системную // Российский журнал кожных и венерических болезней. 1998, № 6. С. 10–13.
- Кубанова А. А., Тихонова Л. И. Дерматовенерология в России. Реальность и перспективы // Вестник дерматологии и венерологии. 2004, № 2. С. 4–11.
- Пономарев А. А., Куликов Е. П., Караваев Н. С., Федосеев А. В. Редкие кожно-висцеральные синдромы. Рязань, 1998. 648 с.
- Потекаев Н. С., Потекаев Н. Н. Болезнь Лайма и обусловленные ею поражения кожи // Вестник дерматологии и венерологии. 2006, № 6. С. 3–9.
- Самсонов В. А., Олисова М. О., Милонова Т. И. О взаимосвязи болезни Лайма и очаговой склеродермии // Вестник дерматологии и венерологии. 1996, № 1. С. 8–9.
- Скрипкин Ю. К. Кожные и венерические болезни. Руководство для врачей в 4-х т. Т. 2 / Под редакцией Ю. К. Скрипкина. М.: Медицина, 1995. 544 с.
- Смирнов А. В., Главинская Т. А. Современные представления о патогенезе и возможностях терапии ограниченной склеродермии // Нижегородский медицинский журнал. 1997, № 3. С. 73–82.
- Furst A. Scleroderma: a fascinating, troubling disease // Advanced Practice Nursing journal. 2004. 4 (2).
Ю. А. Галлямова, доктор медицинских наук, доцент РМАПО, Москва
Диагностика
Склеродермия характеризуется хроническим течением и постоянным прогрессированием процесса. В связи с этим необходимо проведение динамического наблюдения для своевременной корректировки лечения. Комплексная диагностика заболевания включается в себя:
- Общий анализ крови. Позволяет определить наличие воспалительного процесса. При этом в крови увеличивается концентрация лейкоцитов и СОЭ. Склеродермия может сопровождаться снижением количества эритроцитов с развитием анемии.
- Биохимический анализ крови. Определение уровня креатина, мочевины, билирубина, аланинаминотрансферазы и аспартатаминотрансферазы необходимо для оценки функции внутренних органов. Повышение концентрации С-реактивного белка свидетельствует о наличии воспалительной реакции в организме. Для определения степени активности заболевания используют именно этот показатель.
- Общий анализ мочи. Воспалительный процесс в организме отражается на качестве мочи. В ходе исследования определяется повышение концентрации белка и лейкоцитов. Характерным является осадок из эритроцитов.
- Определение уровня CXCL4. Повышение концентрации данного биологически активного вещества происходит при поражении легочной ткани с формированием пневмофиброза или легочной гипертензии.
- Определения уровня NT-proBNP. Мозговой натрийуретический пептид вырабатывается при чрезмерной физической нагрузке. Определение данного фактора необходимо для оценки степени легочной гипертензии.
- ЭКГ. Проводится с целью диагностики изменений в сердечной мышце. При выявлении патологических состояний рекомендуется дополнительное назначение ЭхоКГ.
- Ультразвуковое исследование. Безболезненный и доступный метод инструментального исследования. Назначается для оценки состояния внутренних органов. УЗИ почек, органов брюшной полости и сердца позволяет определить начальные изменения, связанные со склеродермией.
- ФВД. Измерение жизненного объема легких необходимо для определения степени поражения легочной ткани. Данное исследование рекомендуется проводить каждые 6 месяцев для своевременной диагностики склеротических изменений.
- Биопсия. На гистологическое исследование отправляют фрагмент кожи или легких. Это необходимо для дифференцировки склеродермии с другими системными заболеваниями. В биоптате обнаруживаются признаки хронического воспаления, фиброза тканей с отложением коллагена.
Диагностика склеродермии невозможна без определения концентрации аутоантител. Их повышение в крови возможно до появления клинической симптоматики заболевания. Аутоантитела используют для первичной диагностики склеродермии, а также для контроля течения заболевания.
- ANA. Антинуклеарные тела диагностируются почти во всех случаях склеродермии. Они представляют собой иммуноглобулины, атакующие ядра клеток.
- Аnti-Scl-70ю. Выявление высокого уровня антител к топоизомеразе I повышает риск поражения легочной ткани с развитием пневмофиброза. Данные аутоантитела диагностируются в 30% случаев заболевания.
- Анти-РНК полимераза I и III. Отвечают за прогрессирование кожной симптоматики заболевания. Антитела к РНК полимеразе I и III выявляются при повышении риска возникновения почечной недостаточности.
- Anti-RNP. Аутоантитела данной группы выявляются при наличии нескольких аутоиммунных заболевания. Антитела к рибонуклеопротеинам значительно повышаются при поражении мышц и легких.
- Антицентромерные антитела. Определение необходимо для оценки степени тяжести поражения сосудов.
Более 30 лет назад были разработаны критерии склеродермии, основывающиеся на клинической картине заболевания. В зависимости от частоты встречаемости их разделили на большие и малые. Диагноз склеродермия устанавливается при наличии одного большого и, хотя бы, двух малых критериев заболевания.
| Большие критерии | Малые критерии |
| Единственным критерием данной группы является склероз кожных покровов. Распространение процесса происходит по всему телу. | Кожные покровы пальцев рук утолщаются, что провоцирует ограничение подвижности и скованность движений. Данный процесс называется склеродактилией. |
| Склеродермия вызывает язвенное или рубцовое поражение ладонной поверхности ногтевых фаланг. | |
| Разрастание соединительной ткани приводит к поражению легких с формированием фиброза. |
Юсуповская больница располагает новейшим оборудованием для точной диагностики склеродермии. Персонал больницы имеет многолетний опыт исследования и лечения данного заболевания. Высококвалифицированные врачи-ревматологи клиники назначают индивидуальный курс диагностики, позволяющий подобрать необходимый объем лечения.
Диагностика системной склеродермии
Для подтверждения диагноза врач-ревматолог может назначить следующие обследования:
- общий анализ крови;
- общий анализ мочи;
- биохимический анализ крови;
- ревмапробы (может показать увеличенное количество определенных антител);
- биопсия скелетной мышцы;
- электромиографию.
Кроме того, могут потребоваться и другие анализы для определения состояния работы сердца, легких, желудочно-кишечного тракта.
1 Общий анализ крови
2 Биохимический анализ крови
3 Диагностика системной склеродермии в МедикСити
Лечение склеродермии
В настоящее время склеродермия является неизлечимым заболеванием. Однако, современная терапия позволяется ему находиться в длительной ремиссии. Объем лечения зависит от степени активности склеродермии, поражения внутренних органов, а также клинических проявлений. Для терапии аутоиммунного заболевания используют следующие группы препаратов:
- Ферменты. Механизм действия ферментных лекарственных средств связан с их способностью блокировать рост соединительной ткани, тем самым снижая склеротические процессы. Помимо этого, ферменты улучшают эластичность кожных покровов. Введение данной группы препаратов возможно в виде инъекций или трансдермально при помощи электрофореза. Курс лечения определяется лечащим врачом в зависимости от выраженности клинической симптоматики и активности патологического процесса.
- Иммуносупрессоры. В связи с тем, что склеродермия является аутоиммунным заболеванием, необходимо назначение препаратов, блокирующих активность иммунитета. С этой целью используют иммуносупрессоры. К их числу относятся:
- Ритуксимаб. Склеродермия сопровождается образованием антител к собственным клеткам. Ритуксимаб блокирует В-лимфоциты, которые участвуют в их образовании.
- Метотрексат. Действие препарата основано на угнетении деления иммунных клеток.
- Циклофосфамид. Является самым распространенным препаратом группы. Его активно используют в терапии многих аутоиммунных заболеваний. Механизм действия циклофосфамида связан с замедлением скорости разрастания соединительной ткани.
- Циклоспорин. Используется в качестве супрессора Т-лимфоцитов, участвующих в развитии диффузной склеродермии.
- Блокаторы кальциевых каналов. Препараты данной группы блокируют поступление кальция, участвующего в процессах мышечного сокращения. Благодаря этому уменьшается спазм гладкой мускулатуры сосудов.
- Ингибиторы фосфодиэстеразы. Действие препаратов связано с блокировкой фермента, участвующего в сокращении кровеносных сосудов. Лекарственные средства данной группы применяются при легочной гипертензии.
- Ингибиторы АПФ. Механизм действия препарата связан с блокировкой ренина. Лекарственные средства оказывают антигипертензивный эффект, а также защищают ткани почек от патологического воздействия.
Выбор курса терапии осуществляется лечащим врачом на основании диагностических исследований. Московская Юсуповская больница много лет занимается лечением склеродермии. Высококвалифицированные врачи-ревматологи подбирают индивидуальную терапию в соответствии с степенью активности заболевания. Лечение осуществляется в соответствии с последними международными рекомендациями по терапии хронических аутоиммунных заболеваний.
Лечение
Эта аутоиммунная патология пока не устраняется – такого лекарства на данный момент не существует. Все действия сводятся к тому, чтобы стабилизировать состояние больного и продлить ему жизнь. Лечение склеродермии с такой целью включает:
- прием разных медикаментов: антифиброзные, противовоспалительные средства, ферменты и т.д.;
- хирургическое вмешательство. Оно необходимо для восстановления подвижности конечностей, для устранения синдрома Рейно, а также для коррекции косметических недостатков (в основном на лице);
- физиотерапию. Сюда относят лазерное облучение крови (низкоинтенсивное), а также сеансы ПУВА-терапии;
- коррекцию питания. Диета при склеродермии предполагает выбор в пользу здоровой пищи, максимально богатой витаминами, микроэлементами.
Пациентам, страдающим такой патологией, рекомендуется и отказ от вредных привычек, движение в сторону здорового образа жизни.
Прогноз
Продолжительность жизни и прогноз при склеродермии определяется характером ее течения. В соответствии с этим выделяют следующие виды заболевания:
- Острое. Склеродермия характеризуется быстрым развитием, ранним появлением тяжелой клинической симптоматики. В данном случае прогноз для выздоровления и жизни считается неблагоприятным. Как правило, острое течение патологии приводит к полиорганному поражению спустя год от начала заболевания. Острая склеродермия считается наиболее опасной и тяжелой формой болезни.
- Подострое. Аутоиммунное заболевание развивается быстро, однако, склерозирование тканей происходит медленнее, чем при остром течении. Это обеспечивает более благоприятный прогноз. Успешность терапии зависит от степени активности склеродермии.
- Хроническое. Развитие заболевания происходит медленно. В связи с этим прогноз становится благоприятным.
Склеродермия является неизлечимым заболеванием. Соблюдение рекомендаций по лечению и образу жизни позволяют поддерживать длительную ремиссию. К профилактическим мерам относятся:
- Регулярное прохождение медицинского осмотра. Это необходимо при появлении признаков обострения, а также в случае стабильного состояния для контроля заболевания в динамике.
- Прием лекарственных средств. Не разрешается самостоятельная корректировка дозы назначенных препаратов без консультации с лечащим врачом.
- Исключение переохлаждения и переутомления. Длительная стрессовая ситуация может провоцировать обострение склеродермии. Поэтому необходимо соблюдать режим труда с перерывами на отдых.
- Соблюдение рационального и сбалансированного питания. При склеродермии не выделяют специфической диеты. Однако, рекомендуется включать в ежедневный рацион продукты, богатые витаминами, минералами, микроэлементами. В меню ограничивают количество соли и воды, а также витамина С в связи с его стимулирующим воздействием на рост соединительной ткани.
Соблюдение вышеперечисленных рекомендаций поможет свести к минимуму число обострений склеродермии. При появлении первых признаков заболевания необходимо обратиться за медицинской помощью для проведения диагностических мероприятий. Подобным образом можно предотвратить развитие осложнений и тяжелого течения склеродермии.
Обсуждение
Представленные пациентки демонстрируют сложности диагностического поиска в связи с нетипичной для склеродермии клинической картиной. У пациентки Г. кожные высыпания отличались необычной для бляшечной склеродермии кольцевидной формой и имели сходство с атрофической формой красного плоского лишая или кольцевидной гранулемой. Кроме того, эти высыпания оказались резистентны к назначенной стандартной терапии.
Другие клинические случаи глубокой склеродермии демонстрируют нам особенности протекания склеродермического процесса на нижних конечностях, которые в своем дебюте симулировали клинические проявления васкулита, красной волчанки или токсикодермии, что привело к отсроченной постановке правильного диагноза. Назначенное пациенткам лечение без учета данных ранее выполненных патогистологических исследований привело к выраженному распространению патологического процесса в более глубокие слои дермы и подкожно-жировую клетчатку.
Лечение склеродермии в Москве
Аутоиммунные заболевания требуют своевременной диагностики и корректного лечения. Пройти обследование в Москве можно в Юсуповской больнице. Клиника много лет занимается выявлением и терапией любых ревматологических заболеваний. Больница обладает новейшей аппаратурой, позволяющей провести диагностические мероприятия, необходимые для уточнения наличия склеродермии. На основании полученных данных высококвалифицированный персонал проводит курс индивидуального лечения, подобранного в соответствии со стадией заболевания. Записаться на консультацию к специалисту, а также задать любой интересующий вопрос можно по телефону или на официальном сайте Юсуповской больницы.
Клинические наблюдения
Для иллюстрации сложностей диагностики некоторых форм локализованной склеродермии приводим три собственных клинических наблюдения.
Пациентка Г.
Пациентка Г.,
58 лет, обратилась в консультативно-диагностическое отделение ГБУЗ ККВД МЗ КК в июле 2021 г. с жалобами на высыпания на коже груди, спины.
Из анамнеза:
считает себя больной около полугода, когда после продолжительной инсоляции появились округлые гиперемированные пятна с периферическим краем белого цвета. Отмечала слабый центробежный рост элементов. К врачу не обращалась, лечение не получала.
Объективно:
на коже туловища в области груди и спины визуализируются очаги цвета слоновой кости, размером 1,5–2,0 см, кольцевидной формы, с гладкой поверхностью и восковидным блеском (рис. 1 А–Г). По периферии очагов наблюдается слабовыраженный бледно-лиловый венчик. Пальпаторно отмечаются возвышение и плотность края элементов. Субъективных ощущений нет.
При обследовании:
общий анализ крови: эритроциты — 4,7×1012/л, гемоглобин — 121 г/л, цветовой показатель — 0,8, лейкоциты — 6,9×109/л, скорость оседания эритроцитов (СОЭ) — 4 мм/ч.
Общий анализ мочи — в пределах нормы.
Биохимический анализ крови: общий билирубин — 14,0 мкмоль/л, глюкоза — 5,5 ммоль/л, холестерин — 5,0 ммоль/л, общий белок — 69 г/л, аспартатаминотрансфераза (АСТ) — 22 Ед/л, аланинаминотрансфераза (АЛТ) — 18 Ед/л.
Со стороны внутренних органов: патологии не выявлено.
На основании анамнеза и клинической картины был выставлен предварительный диагноз: Склероатрофический лихен? Красный плоский лишай?
Для уточнения диагноза была проведена биопсия
из патологического очага, располагающегося на коже спины (рис. 1 Д, Е). Результаты биопсии: гиперкератоз. Эпидермис с тенденцией к атрофии, сосочки сглажены на большом протяжении. Участки вакуольной дистрофии клеток мальпигиева слоя. Под эпидермисом участки гомогенизации и базофилии коллагеновых волокон. В верхних отделах дермы капилляры спазмированы, умеренные периваскулярные и диффузные гистиолимфоцитарные инфильтраты с плазмоцитами, примесью нейтрофилов и тучных клеток. В сетчатом слое отечный, гомогенизированный, местами фрагментированный коллаген. Потовые железы располагаются внутри дермы. Заключение: морфологическая картина с учетом клинических данных в большей степени соответствует склеродермии.
Было проведено иммунологическое обследование, пациентка консультирована ревматологом, системная склеродермия была исключена.
На основании клинической картины и данных патогистологического исследования (ПГИ) пациентке был выставлен окончательный диагноз:
Бляшечная склеродермия.
Рекомендовано лечение
: стимуляторы регенерации тканей, сосудистые препараты (пентоксифиллин), поливитамины с микроэлементами, наружная терапия (топические глюкокортикостероиды, топические противовоспалительные препараты).
В ходе лечения отмечалась слабовыраженная положительная динамика.
Пациентка Н.
Пациентка Н.,
65 лет, обратилась в консультативно-диагностическое отделение ГБУЗ ККВД МЗ КК в июне 2021 г. с жалобами на уплотнение в области правой голени и болезненность при ходьбе.
Из анамнеза:
больна с 2008 г., когда появилась отечность и боли в области правой голени. Обратилась к дерматологу по месту жительства, который поставил предварительный диагноз: Склеродермия? Васкулит? и рекомендовал сделать биопсию кожи. Заключение ПГИ: гистологические признаки склеродермии, начальная стадия. Далее пациентка обратилась на консультацию к ангиохирургу. Был поставлен диагноз «тромбофлебит», по поводу которого периодически получала лечение (диосмин, ацетилсалициловая кислота, диклофенак, варфарин, гепаринсодержащая мазь) с незначительным эффектом. Лечение по поводу склеродермии не получала.
Объективно:
на коже нижней трети передне-медиальной поверхности правой голени наблюдается слабовыраженная гиперпигментация, деформация подлежащих тканей (рис. 2 А, Б). Кожа с трудом собирается в складку. При пальпации определяются выраженная плотность и болезненность тканей. Субъективно — чувство жжения и боли при ходьбе.
При обследовании:
общий анализ крови: эритроциты — 4,7×1012/л, гемоглобин — 128 г/л, лейкоциты — 7,1×109/л, СОЭ — 14 мм/ч.
Общий анализ мочи — в пределах нормы.
Биохимический анализ крови: общий билирубин — 14,0 мкмоль/л, глюкоза — 5,8 ммоль/л, холестерин — 5,6 ммоль/л, общий белок — 74 г/л, АСТ — 22 Ед/л, АЛТ — 18 Ед/л.
Флюорография грудной клетки — без патологии.
Консультация терапевта: ожирение 1 ст. ИМТ=31,9 кг/м2. Остеохондроз поясничного отдела позвоночника. Со стороны внутренних органов: патологии не выявлено. На основании анамнеза и клинической картины был выставлен предварительный диагноз
: Очаговая склеродермия? Васкулит?
Для уточнения диагноза была проведена глубокая биопсия
из патологического очага, располагающегося на коже медиальной поверхности правой голени (рис. 2 В, Г). Результаты биопсии: эпидермис нормальной толщины. Вакуольная дистрофия клеток мальпигиева слоя. Местами повышено содержание меланина в базальном слое эпидермиса. Дерма утолщена. Поверхностные сосуды спазмированы, стенки их утолщены. Во всех отделах дермы и подкожно-жировой клетчатке отечный, утолщенный, местами гомогенизированный коллаген. Стенки сосудов резко утолщены за счет мукоидного набухания, некоторые сдавлены склерозированными тканями. Слабовыраженные периваскулярные гистиолимфоцитарные инфильтраты с примесью нейтрофилов и фибробластов. Потовые железы и островки жировой ткани располагаются внутри дермы. Заключение: морфологическая картина с учетом клинических данных в большей степени соответствует склеродермии.
Было проведено иммунологическое обследование, пациентка консультирована ревматологом, системная склеродермия была исключена.
На основании клинической картины и данных ПГИ пациентке был выставлен окончательный диагноз
: Очаговая склеродермия, подкожная форма.
Рекомендовано лечение
: стимуляторы регенерации тканей, сосудистые препараты (пентоксифиллин), поливитамины с микроэлементами, наружная терапия (топические глюкокортикостероиды, топические противовоспалительные препараты).
В процессе лечения и по его окончании у пациентки отмечали положительную динамику патологического процесса — уменьшение инфильтрации и атрофии.
Пациентка К.
Пациентка К.,
49 лет, обратилась в консультативно-диагностическое отделение ГБУЗ ККВД МЗ КК в июне 2021 г. с жалобами на высыпания и уплотнение кожи в области голеней, незначительный периодический зуд.
Из анамнеза:
больна более 5 лет, когда после повышения температуры до 38 °С появились несколько гиперемированных плотных высыпаний на коже голеней. Отмечала боли в мышцах. Также беспокоила отечность в области правого верхнего века. Больной был выставлен диагноз: Васкулит? Красная волчанка? После проведенного лечения «сосудистыми» препаратами наступила ремиссия. В мае 2021 г. появились аналогичные высыпания. Обратилась к дерматологу по месту жительства, который порекомендовал сделать биопсию кожи с предварительными диагнозами: Многоформная экссудативная эритема? Токсикодермия? Заключение ПГИ: атрофодермия идиопатическая Пазини — Пьерини. Больная лечилась самостоятельно метилурациловой мазью, кожный патологический процесс прогрессировал.
Объективно
: на коже средней трети передней поверхности левой голени и верхней трети латеральной поверхности правой голени располагаются 2 узла 3×4 см, покрытые кожей розово-коричневого цвета с явлениями атрофии (рис. 3А). При пальпации определялась выраженная плотность тканей. Субъективно — периодический зуд при обострении.
При обследовании:
общий анализ крови: эритроциты — 5,12×1012/л, гемоглобин — 142 г/л, гематокрит — 45,70%, лейкоциты — 9,60×109/л, нейтрофилы — 85,80%, лимфоциты — 7,80%, моноциты — 5,00%, эозинофилы — 0,60%, базофилы — 0,10%, СОЭ — 37 мм/ч.
Общий анализ мочи — в пределах нормы.
Биохимический анализ крови: общий билирубин — 13,30 мкмоль/л, глюкоза — 5,8 ммоль/л, холестерин — 10,31 ммоль/л, общий белок — 71,43 г/л, АСТ — 10,00 Ед/л, АЛТ — 13,00 Ед/л, мочевина — 4,30 ммоль/л, креатинин — 81,00 мкмоль/л, антистрептолизин-О — 27,70 Ед/мл (норма — 0,00–200,0 Ед/мл), С-реактивный белок — 19,36 мг/л (норма — 0,00–8,00 мг/л), ревматоидный фактор — не обнаружен, С4 компонент комплемента — 0,22 г/л (норма — 0,12–0,52 г/л).
Иммунологическое обследование: ANA антиядерные антитела — 1>1:160 (отрицательно), тип свечения — крапчатое, криоглобулины — 0,050 (0,00–0,02), антитела к нативной ДНК — сомнительно (отрицательно), циркулирующие иммунные комплексы — общая фракция — 0,080 ед. опт. пл. (0,040–0,100). Антинуклеарные антитела IgG к антигену SS-А60 ++.
Флюорография грудной клетки — без патологии.
Консультация ревматолога: убедительных данных за системный процесс не выявлено.
Со стороны внутренних органов: патологии не выявлено.
На основании анамнеза и клинической картины был выставлен предварительный диагноз
: Очаговая склеродермия? Вторичный кальциноз?
Для уточнения диагноза была проведена глубокая биопсия
из патологического очага, располагающегося на коже латеральной поверхности правой голени (рис. 3Б). Результаты биопсии: эпидермис нормальной толщины. Участки вакуольной дистрофии клеток мальпигиева слоя. Местами повышено содержание меланина в базальном слое эпидермиса. Дерма утолщена. В верхних отделах дермы стенки сосудов утолщены. Периваскулярные слабовыраженные лимфогистиоцитарные инфильтраты. В сетчатом слое отечный, местами фрагментированный коллаген. Количество фибробластов увеличено. Потовые железы и островки жировой ткани располагаются внутри дермы. В нижних отделах дермы с переходом на подкожно-жировую клетчатку выявляются склеротические изменения в виде выраженного утолщения, гомогенизации и гиалиноза коллагеновых волокон. Стенки сосудов утолщены, некоторые гиалинизированы, периваскулярные умеренные лимфогистиоцитарные инфильтраты с примесью нейтрофилов. Заключение: морфологическая картина с учетом клинических данных в большей степени соответствует глубокой склеродермии.
На основании клинической картины и данных ПГИ пациентке был выставлен окончательный диагноз
: Очаговая склеродермия, подкожная форма.
Рекомендовано лечение:
стимуляторы регенерации тканей, сосудистые препараты (пентоксифиллин), поливитамины с микроэлементами, рассасывающая (бовгиалуронидазы азоксимер) и наружная терапия (топические глюкокортикостероиды, топические противовоспалительные препараты).
В процессе лечения и по его окончании у пациентки отмечали положительную динамику патологического процесса — уменьшение инфильтрации и атрофии.