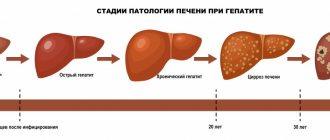
Порфирии — это группа наследственных заболеваний, которые возникают из-за нарушения образования гема, в результате чего в организме накапливаются порфирины или их токсичные предшественники. Гем — железосодержащая часть гемоглобина, сложный белок, «ответственный» за связывание кислорода, транспорт его в ткани и выведение углекислого газа.
В процессе биосинтеза гема образуются соединения под названием порфирины. Строго говоря, гем — это порфирин, в центре которого находится молекула железа Fe2+. Все порфирины имеют красный цвет.
Из-за дефекта ферментных систем при порфириях в организме накапливаются те или иные патологические продукты обмена веществ. Клинические проявления патологии разнятся в зависимости от конкретного дефектного гена.
Различного рода порфирии встречаются с частотой 7–12 случаев на 100 тысяч населения. Бессимптомное носительство различных генов, способных привести к этой патологии, составляет примерно 50–100 человек на 100 тысяч1.
Классификация
Биосинтез гема происходит в костном мозге и в печени. В процессе образования порфиринов участвует восемь ферментов, каждый из которых кодируется своим геном. Семь из них могут пострадать из-за того или иного генетического дефекта.
Соответственно, существует семь вариантов клинических проявлений порфирий, которые делятся на две большие группы — эритропоэтические и печеночные — в зависимости от того, в какой части организма отмечается преимущественное нарушение синтеза порфиринов.
Печеночные порфирии:
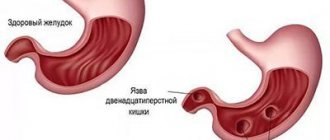
Причина порфириновой болезни — генетический дефект
- поздняя кожная порфирия
- острая перемежающаяся порфирия
- вариегатная порфирия
- наследственная копропорфирия
Эритропоэтические порфирии:
- врожденная эритропоэтическая порфирия (болезнь Гюнтера)
- эритропоэтическая протопорфирия
- эритропоэтическая копропорфирия
Последствия и осложнения
Поскольку порфирии за исключением поздней кожной порфирии являются наследственно обусловленными их излечение полностью невозможно. При наличии у пациента 2-3 и более приступов в год может длительно сохраниться неврологический дефицит в виде вялых периферических парезов. В случаях тяжелого течения возможны осложнения в виде бульбарного синдрома, гипонатриемии, паралича дыхательной мускулатуры с высокой угрозой летального исхода. При порфириях с поражением кожных покровов — риск развития склеродермоидных процессов.
Причины порфирии
Как уже упоминалось, снижение активности ферментов, которое приводит к нарушению обмена порфиринов, вызвано мутацией в одном из семи генов, кодирующих белки-ферменты. При этом даже значительное (до 50%) уменьшение ферментативной активности может какое-то время не вызывать клинических проявлений. Спровоцировать манифестацию болезни могут:
- чрезмерное употребление алкоголя;
- некоторые лекарственные препараты (нестероидные противовоспалительные, сульфаниламиды, барбитураты и др.);
- беременность;
- чрезмерная инсоляция (пребывание на солнце);
- голодание;
- бактериальные и вирусные инфекции;
- воздействие гепатотоксичных химикатов.
Список источников
- Кузнецова Н.П., Панков Б.С., Чубарова А.С. и др. Порфирии. М., 1981. с. 66–14.
- Пустовойт Я.С., Пивник А.В., Карпова И.В. Клиника, диагностика и лечение порфирий // Пособие для врачей. Москва, 2003 г.
- Воробьёв А, Кравченко С, Кременецкая А, Карпова И, Пустовойт Я. Острая перемежающаяся порфирия: проблемы диагностики и лечения // Врач. 2003 г. №2, стр. 8-13.
- Диагностика и лечение острых порфирий: Клинические рекомендации национального гематологического сообществ/ под ред. Пустовойт Я.С., Кравченко С.К., Шмакова Р.Г., Савченко В.Г. — 2021.
- Руководство по гематологии в 3 томах/ под ред. Воробьева А.И. – 2005 – Т.3.
Симптомы порфирии
Клинические проявления порфирий разнообразны и зависят от конкретного типа заболевания.
Врожденная эритропоэтическая порфирия. Заболевание дебютирует в возрасте 1–5 лет. Основные симптомы:
- повышенная чувствительность к свету вплоть до появления пузырей на открытых участках кожи;
- красный цвет мочи;
- розовато-коричневый цвет зубов (из-за отложения порфиринов);
- чрезмерное оволосение;
- увеличение селезенки и гемолитическая анемия (усиленное разрушение эритроцитов).
Под солнцем на коже больного образуются пузыри, которые вскрываются, образуя эрозии, и заживают с рубцами. Постепенно кожа стягивается. Нарушается подвижность суставов, могут деформироваться конечности, мутилировать («отсохнуть») фаланги пальцев. Это довольно редкая форма порфирий: с 1911 года, когда заболевание было описано впервые, известно лишь 100 случаев2.
Эритропоэтическая протопорфирия. Манифестирует в 3–8 лет. У этой болезни клиническая картина довольно размыта: фотосенсибилизация проявляется по типу крапивницы или световой оспы (высыпания в виде мелких пузырьков, которые заживают с образованием рубцов). Солнечные лучи вызывают зуд, жжение, отек, покраснение кожи. Симптомы обостряются весной и летом и затихают зимой.
Эритропоэтическая копропорфирия. Симптомы аналогичны предыдущей форме, но эту разновидность порфирий выделяют, потому что в эритроцитах накапливается другой вид порфирина.
Поздняя кожная порфирия. Чаще страдают мужчины 30–50 лет, жители крупных городов с развитой химической промышленностью, водители, трактористы, автомеханики, дорожные рабочие. Манифестацию заболевания провоцирует контакт с бензином, тяжелыми металлами и другими гепатотоксичными соединениями, а также солнечное облучение и перенесенный вирусный гепатит. Все эти факторы нарушают функционирование ферментных систем печени, что и провоцирует проявление скрытого генетического дефекта.
Кожные симптомы:
При порфириях инсоляция вызывает появление пузырей и эрозий
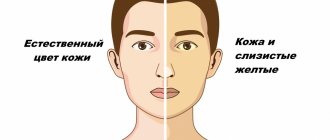
- пигментация: цвет открытых участков кожи меняется от землисто-серого до красновато-синюшного;
- буллезные проявления: реакция на солнце аналогична другим типам порфирий, инсоляция вызывает появление пузырей и эрозий;
- гипертрихоз — повышенная волосатость.
Поражение нервной системы вызывает следующие синдромы:
- астеновегетативный: слабость, нарушение сна, повышенное потоотделение, нарушение температурной регуляции;
- полиневротический: атрофия мышц кистей лица, плечевого пояса из-за нарушения иннервации;
- нарушения сердечного ритма: тахикардии (увеличение частоты сердечных сокращений), брадикардии (урежение ЧСС), аритмии;
- боли в животе, запоры, поносы.
Печеночные проявления:
- гепатомегалия;
- болезненность при пальпации печени;
- бессимптомный вялотекущий гепатит.
Также отмечаются поражения глаз (конъюнктивит, дегенерация сетчатки), ЛОР-органов (вазомоторный ринит) и других систем.
Острая перемежающаяся порфирия также отличается разнообразием клинических проявлений:
- Со стороны ЖКТ отмечаются боли в животе (часто имитирующие острые хирургические патологии), тошнота, рвота, запоры, поносы
- Со стороны нервной системы: параличи, нарушения кожной чувствительности, полиневриты, потеря голоса из-за нарушения иннервации гортани, двоение в глазах (из-за поражения глазодвигательного нерва), недержание мочи и кала, эпилептиформные припадки
- Со стороны психики: эмоциональная лабильность, бессонница, депрессия, спутанность сознания, галлюцинации
- Со стороны сердечно-сосудистой системы: гипертония, тахикардия
Смешанная (вариегатная) порфирия. В Европе встречается редко, характерна для африканских стран. Симптомы аналогичны поздней кожной или острой перемежающейся порфирии, отличия только биохимические.
Наследственная копропорфирия. Протекает в виде приступов, во время которых отмечаются боли в животе, запоры, рвота, депрессивные и истероидные проявления. У некоторых больных отмечается фотосенсибилизация. Возможно бессимптомное течение.
Клинический случай
Пациент Т
., 20 лет, 23.12.17 во время тренировки по спортивным единоборствам получил удар в живот, после чего отмечал эпизод тошноты. Через 4 дня появились выраженная боль в эпигастральной области, тошнота, рвота желчью. Лечение не получал, в течение 2 дней симптоматика регрессировала. 05.01.18 вновь почувствовал боль в эпигастральной области, сопровождавшуюся рвотой и жидким стулом, температура тела при этом не повышалась. Через 2 сут госпитализирован в районную больницу по месту жительства с диагнозом «острый панкреатит». Перенесенные ранее заболевания и обращения за медицинской помощью отрицал. Назначена антисекреторная терапия, рекомендован голод. За 2 нед потерял массу тела на 13 кг, появились слабость и боли в конечностях. 16.01.18 г. пациент переведен в отделение реанимации и интенсивной терапии (ОРИТ) областной больницы. При обследовании обнаружены электролитные нарушения (уровень натрия — 128 ммоль/л, калия — 2,8 ммоль/л), амилаземия (уровень амилазы — 223 МЕ/л), стеноз устья чревного ствола (80% по данным компьютерной томографической ангиографии). Консервативная терапия к улучшению состояния пациента не привела, в связи с чем 28.01.18 он госпитализирован в Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий с диагнозом «Стеноз чревного ствола. Синдром хронической абдоминальной ишемии. Кахексия. Электролитные нарушения» для решения вопроса об оперативном лечении. При поступлении: состояние пациента тяжелое. Кожные покровы обычной окраски, нормальной влажности. Температура тела 37,7 °С. Дыхание самостоятельное, везикулярное, с частотой 18 в 1 минуту, насыщение гемоглобина крови кислородом 98%. Артериальное давление — 155/110 мм рт.ст., частота сердечных сокращений — 115 уд/мин. По данным электрокардиографии — синусовая тахикардия. Живот не вздут, при пальпации мягкий, безболезненный, симптомов раздражения брюшины не было. Энтеральное питание усваивал, отмечались снижение аппетита, запоры в течение 1 нед. Мочеиспускание не контролировал, цвет мочи соломенно-желтый. По поводу стеноза чревного ствола больной консультирован сосудистым хирургом, от хирургической тактики решено воздержаться, рекомендовано консервативное лечение. При осмотре неврологом: сознание ясное, по шкале комы Глазго (ШКГ) — 15 баллов. Ориентация в месте, времени, собственной личности полная. Менингеальные симптомы отрицательные. Зрачки OD = OS, реакция на свет в норме. Движения глазных яблок в полном объеме. Лицо симметричное, язык по средней линии. Дизартрии, дисфонии, дисфагии не было. Мышечный тонус снижен. Тетрапарез по шкале оценки мышечной силы: в руках до 2 баллов в проксимальных и до 4 баллов в дистальных отделах, в ногах — до 3 баллов в проксимальных и дистальных отделах. Сухожильные рефлексы не вызывались. Нарушений чувствительности не было. Имелись нарушения тазовых функций по типу недержания мочи, запоров. Неврологом рекомендовано дообследование (электронейромиография (ЭНМГ), магнитно-резонансная томография (МРТ) головного мозга, шейного и грудного отделов позвоночника, исследование ликвора) для дифференциальной диагностики и уточнения генеза полинейропатии. При лабораторном обследовании обнаружены лейкоцитоз, анемия легкой степени и тромбоцитопения (лейкоциты 13,3·109/л, гемоглобин 12,3 г/дл, тромбоциты 114·109/л соответственно), повышение уровня панкреатической амилазы (77 Ед/л), гипоальбуминемия (30 г/л), электролитные нарушения (натрий 124 ммоль/л, калий 3,5 ммоль/л), повышение уровней воспалительных маркеров (С-реактивный белок 47,6 мг/л, прокальцитонин 7,4 нг/мл), удлинение активированного частичного тромбопластинового времени (40 с), снижение сывороточной концентрации железа (2,2 мкмоль/л) и фолиевой кислоты (1,9 нг/мл). При компьютерной томографии (КТ) органов грудной полости выявлены единичные очаги в нижних долях легких.
Начаты коррекция водно-электролитных нарушений (инфузии растворов натрия хлорида 0,9% и калия хлорида 4%) и анемии (фолиевая кислота, сульфат железа), эмпирическая антимикробная терапия (левофлоксацин), смешанное питание, профилактика стресс-язв (омепразол), профилактика тромботических осложнений (эноксапарин натрия), мероприятия по реабилитации в ОРИТ, включая механотерапию в прикроватных тренажерах, лечебную физкультуру (ЛФК), высаживание в прикроватное кресло.
В рамках дообследования при ЭНМГ обнаружена аксонально-демиелинизирующая (первично аксональная) моторно-сенсорная полинейропатия. При МРТ данных за стенозирование шейного и грудного отделов позвоночного канала, наличие объемных образований, очаговое поражение головного мозга не получено. Анализ ликвора от 30.01.18: бесцветный, прозрачный, цитоз 2 кл/мкл, глюкоза 3,9 ммоль/л, белок 0,2 г/л; вирусологические данные (вирус Эпштейна—Барр, цитомегаловирус, вирус простого герпеса 1-го и 2-го типов) — отрицательные. При бактериологическом исследовании крови, дистального конца удаленного венозного катетера и мокроты обнаружен рост золотистого стафилококка, в связи с чем с 30.01.18 левофлоксацин заменен на линезолид.
Учитывая результаты дообследования, состояние пациента расценили как проявление синдрома Гийена—Барре и кахексии с алиментарной недостаточностью вследствие перенесенного панкреатита, осложнившихся развитием нозокомиальной пневмонии, а также катетерассоциированной инфекции кровотока и тромбоза яремной и подключичной вен. 31.01.18 начат 5-дневный курс специфической терапии синдрома Гийена—Барре иммуноглобулином G — препаратом Октагам («Octapharma Pharmaceutica Production GmbH», Австрия) в дозе 0,4 мг на 1 кг массы тела в сутки.
Несмотря на проведенное лечение и ежедневные реабилитационные мероприятия, неврологическая симптоматика сохранялась на прежнем уровне. 05.02.18 усилились боли в конечностях. Учитывая длительный анамнез иммобилизации в ОРИТ, симптоматику расценили как проявления ПИТС, и к терапии добавлены флувоксамин и карбамазепин. Кроме того, сохранялись электролитные нарушения, и с целью исключения надпочечниковой недостаточности пациент дополнительно обследован: суточная экскреция натрия с мочой составила 87 ммоль/л, сывороточный уровень кортизола 19,7 мкг/дл. Учитывая полученные данные, к терапии добавили гидрокортизон. В связи с неэффективностью монотерапии линезолидом (повторный рост золотистого стафилококка в крови 05.02.18, сохраняющаяся высокая температура тела), антимикробная терапия усилена цефазолином. При повторном дуплексном сканировании отмечены сохраняющиеся тромбозы подключичной и внутренней яремной вен, что, вероятно, и служило причиной стойкой бактериемии, несмотря на проводимую антимикробную терапию.
Для исключения инфекционного эндокардита выполнена чреспищеводная эхокардиография, при которой данных за наличие вегетаций на клапанном аппарате и в полостях сердца не получено. Во время эзофагогастродуоденоскопии обнаружен грибковый эзофагит, позже подтвержденный результатами микроскопии.
После начала терапии карбамазепином и флуконазолом 08.02.18 состояние пациента с отрицательной динамикой в виде снижения уровня сознания до оглушения (14 баллов по ШКГ), появления спонтанного нистагма, тошноты. При повторной МРТ головного мозга с целью исключения понтинного миелинолиза изменений не выявлено. На следующие сутки восстановилось ясное сознание, однако пациент стал эмоционально лабилен, начал жаловаться на нарастающие ноющие боли в конечностях и сердце, при этом изменений на электрокардиограмме не было.
По совокупности всех клинико-лабораторных и инструментальных данных у пациента заподозрена острая порфирия, что потребовало специального лабораторного подтверждения. 09.02.18 в анализе мочи обнаружен порфобилиноген (ПБГ) 200,6 мг/л, δ-аминолевулиновая кислота (АЛК) 145,6 мг/л. Пациент переведен в отделение реанимации Национального медицинского исследовательского центра гематологии, где находился в течение 25 сут. В рамках патогенетической терапии острой порфирии проводилась постоянная инфузия 20% раствора глюкозы в объеме 1000 мл/сут, проведен курс аргинатом гема (препарат Нормосанг, «Orphan Europe S.a.r.L.», Франция) 125 мг/сут. В динамике в результате проводимой терапии отмечено снижение концентрации ПБГ с 200 до 31 мг/л, АЛК с 146 до 23 мг/л. Пациенту продолжена антибактериальная терапия стафилококковой инфекции (очаговая двусторонняя пневмония, инфекция кровотока). Диагностирован пиелонефрит, вызванный Pseudomonas aeruginosa.
Проводилась терапия тромбозов вен нижних конечностей и яремной вены справа. В связи с сохраняющейся алиментарной недостаточностью пациент получал смешанное питание. Течение заболевания в отделении реанимации осложнилось развитием симптоматического психоза, в связи с чем проводилась терапия галоперидолом с положительным эффектом. По данным лабораторных исследований выявлены признаки фолиеводефицитной и железодефицитной анемии, проводилась заместительная терапия фолиевой кислотой. На фоне коррекции гипонатриемии удалось стабилизировать уровень натрия в пределах 132 ммоль/л (минимальный уровень достигал 120 ммоль/л). Ежедневно проводились занятия кинезиотерапией и ЛФК. 04.04.18 пациент был выписан. Его состояние расценивалось как средней степени тяжести и обусловлено течением основного заболевания, сохраняющимся вялым парезом конечностей, алиментарной недостаточностью, анемией сочетанного генеза, тромботическими осложнениями.
Диагностика порфирии
Относительная редкость патологии и разнообразие клинических проявлений становятся причиной регулярных диагностических ошибок. Особенно это касается диагностики печеночных порфирий. Часто такие пациенты безрезультатно лечатся у дерматолога и других узких специалистов.
Для диагностики заболевания необходимо провести анализ на определение уровня различных фракций порфиринов в крови, моче и кале. В зависимости от того, уровень каких фракций порфиринов повышен и каково соотношение между разными фракциями, диагностируется та или иная форма порфирии.
Болезнь вампиров
О связи двух этих явлений: болезни и древних верований о людях-кровососах впервые заявил доктор Ли Иллис из Великобритании. В 1963 году он представил в Королевское медицинское общество монографию «О порфирии и этиологии оборотней». Труд ученого содержал подробный сравнительный анализ сохранившихся исторических свидетельств, в которых описывались вампиры, и симптомов порфирии. Оказалось, что клиническая картина редкой болезни в точности копирует портрет самого колоритного вурдалака.
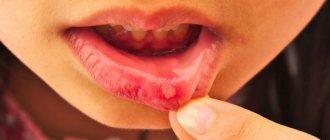
При запущенной форме порфирии кожа вокруг губ и десен у больных высыхает, отчего резцы обнажаются до десен, создавая впечатление оскала. К тому же на самих зубах откладывается особое вещество порфирин, которое окрашивает улыбку (а вернее, оскал) человека в красновато-бурый цвет. Кожа на лице и теле таких людей истончается и от воздействия солнечного света лопается, покрываясь шрамами и язвами. Болезнь повреждает еще и хрящи, а также те органы, из которых они состоят (прежде всего, это нос и уши). Пальцы становятся скрюченными. Солнечный свет доставляет бедолагам наиболее тяжкие мучения, ведь именно под воздействием ультрафиолета начинается распад гемоглобина. Поэтому днем люди, страдающие порфирией, стараются на улице не появляться, а активность проявляют только в сумерки, ближе к ночи. То ли от испытываемых мучений, то ли от вынужденного затворничества, то ли от каких-то внутренних процессов, происходящих в организме, эти люди страдают еще и нервно-психическими расстройствами и неадекватным, в том числе, агрессивным поведением.
Можно себе представить ужас тех, кто однажды вечером или ночью при свете луны встретил на узкой дорожке одного из таких «симпатяг». Тут не только в вампиров и оборотней поверишь, а во что угодно!
Лечение порфирии
Лечением порфирий занимается гематолог. Так заболевание носит генетический характер, терапия сводится лишь к снижению симптомов.
Причины и симптомы порфирии
При эритропоэтических порфириях на первый план выходит защита от солнца: максимально закрытая одежда, шляпы с широкими полями, солнцезащитные кремы. Для повышения фотозащиты могут быть рекомендованы препараты бета-каротина, никотиновой кислоты.
Чтобы отсрочить развитие цирроза при печеночных порфириях, пациентам назначают гепатопротекторы — например, препараты урсодезоксихолевой кислоты (Урсосан), которые повышают устойчивость гепатоцитов (клеток печени) к внешним токсическим воздействиям и таким образом снижают активность апоптоза (гибели клеток).
Для уменьшения уровня порфиринов в организме могут быть рекомендованы кровопускания и прием противомалярийных препаратов. В качестве поддерживающей терапии назначают витамины, АТФ и кокарбоксилазу.
Про кровь голубую и простую
Современные ученые считают, что в охоте на вурдалаков пострадали, как это часто бывает, люди невиновные. Хотя повод у преследователей все-таки был. Нет, те, кого обвиняли в вампиризме, не пили чужую кровь и не оборачивались по ночам дикими зверями, но при этом выглядели они – не приведи бог, да и образ жизни вели, мягко говоря, подозрительный. Но обо всем по порядку.
| А вот и не сказки! | |
| Миф о нелюбви вампиров к чесноку возник неслучайно. Страдающие порфирией на самом деле не выносят этот пряный овощ, поскольку сульфоновая кислота, выделяемая чесноком, усиливает в организме повреждения, вызванные заболеванием. А вот главное обвинение в кровопийстве – это поклеп. Восполнить собственный дефицит красных кровяных телец благодаря чужой крови невозможно. К тому же главная проблема больного – не нехватка красных кровяных телец в крови, а переизбыток порфиринов в организме. | |
Медики полагают, что люди, несправедливо обвиненные в вампиризме, на самом деле страдали редким генетическим заболеванием крови, называемым «порфирия» (от греческого «porphyros» – «пурпурный»). Считается, что распространению этой болезни способствовали браки между близкими родственниками. Порфирия была наиболее распространена в маленьких деревнях Трансильвании (родине графа Дракулы) примерно 1000 лет назад. Но ходят слухи, будто бы недуг не обошел стороной и королевские фамилии. Например, историк Эндрю Уилсон в своей книге «Викторианцы» упоминает о наследственной порфирии, свирепствовавшей в британской королевской семье, и утверждает, что именно эта болезнь лишила разума деда королевы Виктории короля Георга III. Однако с восшествием на престол Виктории венценосная семья избавилась от этого проклятия. Уилсон полагает, что тут дело не обошлось без адюльтера, в результате которого и появилась на свет будущая английская королева.
Так что же это за болезнь такая? Сегодня ученые знают точно, что именно делает людей похожими на вампиров. При порфирии нарушается воспроизводство гема – небелковой части гемоглобина, что в свою очередь приводит к избыточному накоплению в организме токсических веществ – порфиринов и их предшественников, обладающих способностью связывать в организме металлы, прежде всего железо и магний. Избыток порфиринов оказывает токсическое воздействие на весь организм.
Какая связь между порфирией и вампирами
Согласно мнению ученых-медиков люди, которых считали вампирами, были подвержены болезни под названием порфирия, а иначе у них было редко встречающееся генетическое заболевание крови. Порфирия, в переводе с греческого «porphyros», означает пурпурный и причиной ее возникновения являются родственные браки, чему способствовала низкая миграция населения, особенно в небольших деревнях и городах. Особенно сильно были подвержены порфирии, жители сел Трансильвании около тысячи лет назад, однако, по имеющимся сведениям, эта необычная болезнь не миновала и королевские семьи.
О симптомах порфирии известно с незапамятных времен, а со временем болезнь получила и научное обоснование существования вампиров – места их обитания в совокупности с типичным образом жизни и внешностью, ясно указывают на то, что так называемые вампиры, это попросту страдающие порфирией люди — о вампирах и болезни порфирия.
О наследственности венценосных особ
В 1998 г. английское издательство «Bantam Press» опубликовало книгу Дж. Рёля (историка), М. Уоррена (биохимика) и Д. Ханта «Пурпурная тайна: Гены, безумие и королевские дома Европы» (J.C.G. Röhl, M.J. Warren and D. Hunt. Purple Secret: Genes, «Madness» and the Royal Houses of Europe), исследовавших роль порфирии в генеалогическом лабиринте королевских династий. Острой перемежающейся порфирией страдал король Англии Георг III, однако позже, когда обнаружились указания на повышенную чувствительность кожи короля к солнечному свету, диагноз уточнился на вариегатную порфирию.
Из книги Марка Фалкирка:..»порфирия», симптомами которой являются упадок сил, побледнение кожи и светобоязнь. Затем кожа истончается и начинает гнить, покрываться язвами и рубцами, слизистая десен и внутренней части губ лопается, начинает кровоточить и обнажает корни зубов. Многие века больных этой болезнью принимали за вампиров и оборотней, пытали и казнили.
- [1]
- Порфирия — Гематологический Научный Цент РАМН
- Порфирия — история изучения
- Межрегиональная Благотворительная Общественная Организация Инвалидов «Союз пациентов и пациентских организаций по редким заболеваниям» — поддержка в случае отказов в обеспечении необходимого лечения, консультативная и/или юридическая поддержка для пациентов и врачей будет оказана при получении письменного запроса через сайт организации.
- Российская Ассоциация Порфирии. Дополнительная информация о заболевании, лечении и работе профильной общественной организации пациентов
- Болезнь Гюнтера
Порфирия – дополнительные факторы развития
Хотя порфирия имеет генетическую основу, только в 20% случаев только генетический фактор является достаточным детерминантом клинических симптомов человека. В большинстве случаев за возникновение болезни ответственны дополнительные факторы.
Наиболее важные из них перечислены ниже:
- вирусные заболевания печени,
- алкоголь,
- длительная терапия нестероидными препаратами,
- промышленные краски и лаки,
- органические растворители,
- тяжелые металлы,
- средства защиты растений,
- калорийность,
- стресс
- у женщин также гормональные нарушения.
Про
Механизмы заболевания
Итак, вампиры в реальной жизни не существуют. При данной патологии нарушено производство гемма-небелковой части гемоглобина, что приводит к переизбытку в крови токсических порфиринов, связывающих в организме металлы, в частности, железо и магний. Избыточное содержание вещества отравляет практически весь организм. Существует несколько типов порфирий, и все они, кроме самой поздней формы, поражающей кожу, являются генетическими. Типы наследования каждого вида разнятся, но на первый план выходит аутосомно-доминантный механизм.