- Частота возникновения саркомы Юинга
- Факторы риска развития саркомы Юинга
- Диагностика саркомы Юинга
- Определение стадии (распространенности) саркомы Юинга
- Лечение саркомы Юинга
- После окончания лечения
Саркома Юинга занимает второе место по частоте среди злокачественных опухолей костей у детей (после остеогенной саркомы) была впервые описана Д. Юингом в 1921 году и получила название по имени автора.
Эта опухоль редко встречается у детей младше 5 лет и у взрослых старше 30 лет. Наиболее часто эта опухоль возникает у подростков в возрасте от10 до 15 лет. Встречаются случаи внекостной саркомы Юинга с поражением мягких тканей.
Другая опухоль детского возраста — примитивная нейроэктодермальная опухоль (ПНЕТ) имеет много общих черт с костной и внекостной саркомой Юинга, которая может первично поражать как кости, так и мягкие ткани. Все эти опухоли развиваются из одного и того же типа клеток.
Костная саркома Юинга составляет 87%, внекостная саркома Юинга — 8% и ПНЕТ -5%.
Обычно такие опухоли развиваются в центральной части длинных трубчатых костей верхних и нижних конечностей, однако могут выявляться также в тазовых костях и в костях и мягких тканях, образующих грудную клетку.
Что такое
Данный вид саркомы представляет новообразование злокачественного типа, которое развивается из костной ткани. Процент заболеваемости данным видом саркомы среди других злокачественных костных заболеваний – 15 процентов.
Очень часто это заболевание появляется у детей и подростков. Чаще всего болеют мальчики, девочки – реже. Локация поражения – трубчатые длинные и плоские кости. Иногда эта болезнь возникает не в костях, а в мягких тканях, называясь экстраоссальной саркомой Юинга. Бывают кроме того и периферические примитивные нейроэктодермальные саркомы, относящиеся к разновидностям рассматриваемого заболевания.
Саркома Юинга очень агрессивна и характеризуется ранним появлением метастаз. Для него свойственны боль, отеки, местное повышение температуры и увеличение вен около опухоли. Опухоль чаще всего диагностируется на поздних этапах развития, нередко в месте заболевания возникают переломы патологического характера.
Лечится она комбинированно: хирургическим вмешательством, химиотерапией предоперационного и послеоперационного назначения и лучевой терапией.
Список источников
- Феденко А. А., Бохян А. Ю., Горбунова В. А., Махсон А. Н., Тепляков В. В. Практические рекомендации по лечению первичных злокачественных опухолей костей (остеосаркомы, саркомы Юинга). Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2020 (том 10).17
- Соловьев Ю.Н., Саркома Юинга. Вопросы онкологии 2002; №1 стр. 7–16.
- Нейштадт Э.Л. Опухоли и опухолеподобные заболевания костей / Э.Л. Нейштадт, А.Б. Маркочев. — СПб.: Фолиант, 2007. — 344 с.
- Опухолевые и опухолеподобные процессы у детей /Е. Д. Черствой [и др.]; под ред. Е. Д. Черствого. — Минск: Асар, 2002. — С. 197–199.
- Опухоли и опухолеподобные заболевания костей / Нейштадт Э.Л., Маркочев А.Б. — Санкт-Петербург: Фолиант, 2007. — 342 c.
Локализация
Локализуется саркома Юинга в костях таза, бедра, позвонках, ребрах, лопатках, малоберцовой и большеберцовой костях, плечевой кости.
Когда саркома Юинга возникает в трубчатых костях, то очагом ее распространения становится область диафиза, а затем распространение идет к эпифизу. Часто увеличение раковых клеток идет по костному каналу.
Наиболее часто метастазы при этом виде заболевания возникают в легких, костной ткани и костном мозге.
На последних стадиях метастазирование идет в центральную нервную систему, лимфатические узлы и внутренние органы. При диагностировании заболевания у большого количества людей уже имеется метастазирование.
Факторы риска развития саркомы юинга
В настоящее время известно несколько факторов риска, связанных с возникновением саркомы Юинга.
Пол. Саркома Юинга несколько чаще встречается среди мальчиков по сравнению с девочками.
Возраст. В 64% случаев саркома Юинга встречается в возрасте от 10 до 20 лет.
Раса. Наиболее часто саркома Юинга наблюдается у белого населения.
Профилактика саркомы Юинга, как и большинства других опухолей детского возраста, в настоящее время невозможна, так как образ жизни детей и их родителей не влияет на частоту возникновения данной опухоли.
Симптомы
Один из первых симптомов – болевой синдром в локации поражения. Поначалу он слабый, но не проходит ночью, в периоды отдыха, а, напротив, усиливается в покое.
Далее боли становятся сильнее, пациент не может быть активным в течение дня, не может нормально спать. При пальпации наблюдается болезненность. Бывает местная гипертермия, может быть расширена венозная сетка.
Через несколько месяцев после первых симптомов раковая опухоль стремительно растет, хорошо обнаруживается при пальпации.
На последних стадиях заболевания возникает угроза перелома патологического характера.
Также возникает потеря аппетита, слабость, истощение организма, повышение температуры, анемия.
Если саркома Юинга локализуется в области костей нижних конечностей, то больной может хромать.
Если поражены позвонки, то могут нарушаться функции органов таза.
При локализации саркомы Юинга в грудной области бывает харканье кровью, затруднительное дыхание.
Причины
Точные причины развития саркомы Юинга не установлены. Большинство специалистов-онкологов считают, что существенная роль принадлежит наследственной предрасположенности. Предположительно, фактором высокого риска развития болезни является различные аномалии скелета (энхондрома/аневризмальная костная киста и др.) и нарушения развития мочеполовой системы в период внутриутробного развития (гипоспадия/редупликация почечной системы). Почти в 40% случаев прослеживается тесная связь с предшествующей травмой.
Диагностирование
Обычно данная патология диагностируется после результатов рентгенографии. На снимке видно, что контуры опухоли нечеткие, кортикальная пластинка расслоена.
Если в болезнь вовлекается надкостница, то рентген показывает игольчатые и пластинчатые новообразования. На рентгене будет видно и изменение мягких тканей в размерах при некоторой их однородности.
Далее после рентгенографии проводится обследование у онколога, который назначает КТ или МРТ злокачественных мягких тканей.
Эти исследования определяют размер опухоли, ее распространенность по костномозговым каналам и ее связь с нервами и сосудами в соседних тканях.
Для исследования тканей делается биопсия: берется материал рядом с костномозговым каналом или из мягких тканей опухоли.
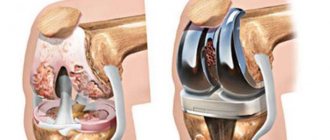
Рак тазобедренного сустава
Преимущества онкологического центра Sofia
- уникальные врачи, которые занимаются лечением даже сложных случаев;
- прием и лечение по полису ОМС (уточняйте информацию у администраторов центра);
- великолепное оснащение: проводится высокотехнологичное лечение с применением всех доступных на сегодня методов;
- многочисленные сертификаты и награды, в том числе JCI;
- одно из самых лучших диагностических оборудований в Москве;
- 30 лет уникального опыта и безупречной репутации;
- повышенный комфорт: уютный, теплый интерьер, кафе и ресторан на крыше с панорамным видом – вы не чувствуете себя в больнице;
- большое количество мест для парковки.
«Sofia» находится в Центральном административном округе (ЦАО) Москвы, рядом сразу с несколькими станциями метро: «Новослободская», «Тверская», «Чеховская», «Белорусская» и «Маяковская».
Записаться можно по телефону +7 (495) 775-73-60 или через онлайн-форму!
Блок стилей «STYLE»
Лечение
Ввиду того, что саркома Юинга имеет агрессивный характер распространения и раннее метастазирование, воздействовать необходимо на весь организм комбинированно.
Химиотерапия
Бывает предоперационной и послеоперационной. Обычно сочетают сразу несколько препаратов. После смотрят ответ опухоли на химиотерапию.
Лучевая терапия
Обычно при такой терапии сразу назначаются высокие дозы облучения. Облучают очаг возникновения заболевания и легкие, если там обнаружены метастазы.
Хирургическое вмешательство
Опухоль могут удалить целиком вместе с соседними мягкими тканями. Если удаляется часть кости, то ее заменяют эндопротезом. Если опухоль полностью удалить нельзя, ее удаляют частично.
При современной медицине стараются не производить, если это возможно, экзартикуляции и ампутации, а сохранить орган или конечность.
Классификация по стадиям заболевания
Степень распространенности первичной опухоли легла в основу классификации по 4 стадиям:
- Злокачественный процесс за пределы кости не выходит, хорошо дифференцирован. Размер — до 8 см, лимфоузлы не поражены.
- Онкопроцесс все еще не распространился за пределы кости, слабо дифференцирован, размер превышает 8 см.
- В первичной зоне присутствует несколько очагов поражения кости. Высокозлокачественная степень дифференцировки (способность к распространению).
- Процесс вышел за пределы кости.
Профилактика рака костей
Каких-либо методов специфической профилактики неоплазмы кости не существует. В качестве общих мер можно рекомендовать:
- Отказаться от табакокурения и злоупотребления алкоголесодержащими напитками.
- Вести физически активный образ жизни.
- Поддерживать иммунитет: прием растительных препаратов, стимулирующих иммунитет, закаливающие водные процедуры, регулярный прием таблеток витаминно-минерального комплекса.
- Придерживаться рационального питания.
- Регулярно проходить профилактические медосмотры.
Однако, следует учитывать, что здоровый образ жизни не является гарантией снижения риска развития каких-либо видов злокачественных заболеваний. Поэтому, если возникло подозрение на рак костей, симптомы даже незначительного характера вас должны насторожить. Обращение за специализированной профессиональной медицинской помощью позволяет рано начать терапию и повысить эффективность лечебных мероприятий.
Диагностика
При подозрении на остеогенную саркому диагностический поиск ведут такие специалисты, как детский онколог, детский хирург, патоморфолог, рентгенолог. Окончательный диагноз устанавливается на основании результатов гистологического исследования.
При первой встрече с юным пациентом врач собирает анамнез, уточняет информацию о наличии или отсутствии каких-либо хронических заболеваний опорно-двигательного аппарата, предшествующих травмах, оперативных вмешательствах, наследственных синдромах, семейной наследственной онкологической патологии. Клинический осмотр пациента включает оценку очага пораженной конечности, регионарных лимфатических узлов, физикального статуса (общего состояния больного).
Диагностический поиск состоит из следующих исследований:
- рентгенография зоны поражения;
- компьютерная томография (КТ) с контрастным усилением пораженной опухолью зоны и органов грудной клетки;
- остеосцинтиграфия;
- магнитно-резонансная томография пораженной зоны.
Наиболее распространенным и простым методом диагностики остеогенной саркомы, выполнение которого возможно на амбулаторном этапе обследования, является рентгенографическое исследование пораженной конечности. Не исключены ситуации, когда образование является случайной находкой при рентгенографии, выполненной по поводу травматического повреждения. В таких ситуациях пациенту показано дообследование.
Характерные рентгенологические признаки остеогенной саркомы (рис. 2):
- деструкция и склероз костной ткани в зоне поражения;
- периостальный козырек Кодмена, представляющий из себя отслоенную опухолью надкостницу;
- игольчатый периостит с множественными костными иглами-спикулами;
- очаги патологического костеобразования в мягких тканях (поля оссификации) в области образования;
- патологический перелом пораженной конечности.
Рис. 2. Рентгенологические признаки остеогенной саркомы
Для более четкой визуализации процесса, уточнения размеров образования, распространения, исключения поражения мягких тканей детям показано выполнение компьютерной томографии. Кроме того, этот метод позволяет выполнить оценку первичной опухоли и выявить наличие отдаленных метастатических очагов.
Сцинтиграфия скелета уже долгое время остается стандартным методом диагностики костных поражений, являясь более чувствительной, чем рентгенологические методы. Она позволяет проводить исследование всего тела человека за небольшой промежуток времени. Данное исследование основано на повышении накопления фосфорных соединений в очаге поражения, что свидетельствует об активности процесса, характерного для злокачественных новообразований (рис. 3).
Рис.3. Патологическое накопление радиофармпрепарата (Технеций mTc)
Магнитно-резонансная томография (МРТ) первичного опухолевого очага с захватом смежного сустава является оптимальным методом локального стадирования. МРТ-контроль на фоне системной терапии позволяет оценить динамику процесса и, соответственно, спланировать объем оперативного вмешательства в дальнейшем.
Одним из ключевых этапов диагностики является биопсия образования и последующее гистологическое и иммуногистохимическое исследование полученного материала.
Есть два различных подхода к получению материала: с применением трепан-иглы и открытый тип биопсии. Манипуляция выполняется под КТ или УЗ-навигацией или с применением электронно-оптического преобразователя (рис. 4).
Рис.4: Биопсия с применением трепан-иглы
Глава 13.
Саркома Юинга является второй по частоте среди злокачественных опухолей костей у детей — составляет 10-15%. Эта опухоль редко встречается у детей моложе 5 лет и у взрослых старше 30 лет. Пик заболеваемости приходится на 10 -15 лет.
Саркома Юинга состоит из мелких круглых клеток со скудной цитоплазмой, круглым ядром, содержащим нежный хроматин и слабо просматривающиеся базофильные нуклеолы. В отличие от остеосаркомы она не продуцирует остеоид.
Существует некоторая связь между возникновением саркомы Юинга и наличием скелетных аномалий (энхондрома, аневризмальная костная киста и т.д.) и аномалиями мочеполовой системы (гипоспадии, редупликация почечной системы). В отличие от остеосаркомы, ионизирующая иррадиация не ассоциируется с возникновением саркомы Юинга.
Цитогенетический анализ показывает в 85% случаев хромосомную транслокацию t(11,22) (q24,q12) в большинстве клеток, выделенных из этой опухоли. Аналогичные изменения выявляются в другой мелкоклеточной опухоли- PNET (примитивной нейроэктодермальной опухоли). И хотя саркома Юинга не имеет анатомической связи со структурами ЦНС или автономной симпатической нервной системы, эти цитогенетические изменения доказывают нейроэктодермальную природу опухоли. Кроме того, в большинстве случаев в клетках опухоли выявляется экспрессия РАХ3 протеина, который в норме определяется в период эмбрионального развития нейроэктодермальной ткани. При саркоме Юинга часто можно определить и другой опухолевый маркер- NSE (сывороточная нейрон-специфичная энолаза).
Саркома Юинга является одной из самых агрессивных злокачественных опухолей. До применения системной терапии почти у 90% больных развивались метастазы. Наиболее частая локализация метастазов на момент первичной диагностики- легкие, кости, костный мозг. 14%- 50% пациентов к моменту установления диагноза уже имеют метастазы, выявляемые рутинными методами исследования, и гораздо больше больных имеют микрометастазы. Лимфогенное распространение метастазов встречается редко и всегда связано с плохим прогнозом. Редко также имеет место ретроперитонеальное и медиастинальное распространение метастазов. 2,2% пациентов имеют метастазы в ЦНС при первичной диагностике, и почти все — при генерализации процесса.
Клиника
Клиническими признаками саркомы Юинга являются усиливающиеся боли, отек над пораженной областью с нарушением функции конечности. Опухоль обычно болезненная при пальпации, быстро увеличивается в размерах. Поражение периферических нервов может вызвать появление неврологической симптоматики. Может возникать лихорадка различной степени. Мягкотканный компонент опухоли часто выражен значительнее, чем костный очаг.
В опухоли часто встречаются геморрагии и некрозы, что вызывает повышение местной температуры, эритему и иммитирует неспецифическое воспаление, что затрудняет диагностику. Такая симптоматика позволяет в первую очередь предположить наличие остеомиелита.
Наиболее частая локализация саркомы Юинга- кости таза, бедро, большеберцовая кость, малоберцовая кость, ребра, лопатка, позвонки, плечевая кость. В противоположность остеогенной саркоме, саркома Юинга чаще всего поражает плоские кости (Рис. 13-1). В трубчатых костях опухоль локализуется преимущественно в диафизе и имеет тенденцию к рапространению к эпифизам кости. В 91% случаев опухоль располагается интрамедуллярно, причем распространение по костномозговому каналу часто больше, чем по кости.
Рентгенологические признаки саркомы Юинга.
-Деструкция кости («изъеденная молью») без четких границ с тенденцией к рапространению по костномозговому каналу (Рис.13-2). -«Луковичный периостит» многослойный линейный периостит, который может сочетаться с игольчатым(Рис.13-3). -В 5% случаев выявляется патологический перелом. При локализации опухоли в проксимальном участке бедренной кости патологический перелом возникает значительно чаще (более чем в 70% случаев). -При рентгенографии мягких тканей выявляется отчетливый мягкотканный компонент однородной структуры. -Поражение ребер часто сочетается с плевритом.
Но, тем не менее, рентгенологические признаки не являются абсолютно патогномоничными. Необходимо проводить дифференциальную диагностику с другими патологическими процессами в костях- с остеомиелитом (в первую очередь), травмой, другими злокачественными опухолями костей (рабдомиосаркома, синовиальная саркома, лимфома, нейробластома).
Диагностика
Проведение всех диагностических процедур необходимо для верификации диагноза, определения степени распространения процесса и определения факторов риска, что, в свою очередь, определяет и тактику лечения пациента.
1. Биопсия опухоли. Проводится трепанобиопсия опухоли. Достаточное количество материала можно иногда получить из мягкотканного компонента. Если это невозможно, материал получают из участка кости, граничащего с костномозговым каналом. Биопсию лучше проводить по передней, задней или медиальной поверхности конечности, нежели по латеральной (т.к. увеличивается риск патологического перелома). Место биопсии, а также все места дренирования раны впоследствии должны быть включены в зону облучения. 2. Рентгенография очага. 3. Рентгенография и КТ легких 4. Аспирационная биопсия или трепанобиопсия костного мозга из нескольких мест (т.к. саркома Юинга имеет тенденцию к метастазированию в костный мозг) 5. Остеосцинтиграфия с Te99- позволяет выявить другие очаги в костях, так как могут быть множественные метастазы в кости. 6. Компьютерная томография и/или ЯМР-томография очага- наиболее точно определяет размеры опухоли, ее связь с окружающими тканями, сосудисто-нервным пучком, распространение опухоли по костномозговому каналу. 7. Ангиография 8. Ультразвуковое исследование
В современных лабораториях проводится цитогенетическое и молекулярно-биологическое исследование опухоли, причем для этого часто достаточно материала, полученного при аспирационной биопсии. Молекулярно-биологические исследования используются также для выявления «минимальной остаточной опухоли» (для этого достаточно наличия 1 опухолевой клетки на 100000 нормальных, тогда как микроскопически опухолевую инфильтрацию в костном мозге можно выявить только, при наличии 5%-10% опухолевых клеток).
Прогностически неблагоприятные факторы: -метастазы в кости и костный мозг (выживаемость этой группы больных составляет менее 10%); -высокий уровень ЛДГ; -поражение костей таза (особенно с высоким уровнем ЛДГ); -метастазы в лимфатические узлы; -объем опухолевой массы (включая мягкотканный компонент) 100 мл и более. По данным исследования CESS-86 7-8 -летняя безрецидивная выживаемость у пациентов с объемом опухоли менее 100 мл составляла 63%, а при объеме 200 мл и более — лишь 34%.
В отличие от остеогенной саркомы, патологический перелом не оказывает влияния на прогноз заболевания.
Лечение
До эры эффективной системной терапии около 90% пациентов с первичной саркомой Юинга кости умирали в течение первых 2 — 5 лет заболевания от системных легочных, костномозговых и/или костных метастазов, несмотря на то, что уже было известно, что, в отличие от остеосаркомы, эта опухоль чувствительна к лучевой терапии. Впечатляющее улучшение выживаемости достигнуто с началом применения химиотерапии — более 50% (для саркомы Юинга показатели выживаемости определяются при сроках 7 -8 лет ремиссии).
Терапия саркомы Юинга включает в себя: 1. Многокомпонентную химиотерапию (используются препараты — винкристин, адриамицин, ифосфамид, циклофосфан, актиномицин, вепезид в комбинации). В современных программах лечения применяется предоперационная и послеоперационная полихимиотерапия, при этом учитывается также гистологический ответ опухоли на лечение. Хорошим ответом опухоли на химиотерапию считается наличие менее 5% живых опухолевых клеток (данные EICESS, EW-93). 2. Лучевую терапию на очаг в высоких дозах — 45-55 Гр (см. Главу Лучевая терапия). При развитии метастазов в легкие проводится лучевая терапия на легкие. 3. Если возможно, радикальное удаление опухоли (включая кость и мягкотканный компонент). Радикальная резекция возможна при очаге в малоберцовой кости, костях предплечья, ребрах, ключице, лопатке.
Операция улучшает локальный контроль опухоли. В сочетании с интенсивной химиотерапией и лучевой терапией полная резекция опухоли значительно снижает риск местного рецидива. Уменьшение частоты местного рецидива отмечается даже после нерадикальных операций. Современная хирургическая техника позволяет проводить органосохраняющие операции при поражении бедренной, плечевой костей, а также резекцию костей таза.
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10%, в последнее время применяется более интенсивное лечение — химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30% больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли к ХТ удается достичь еще более высоких результатов лечения (7-летняя выживаемость составляет около 50%).
Страница 196