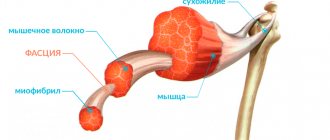
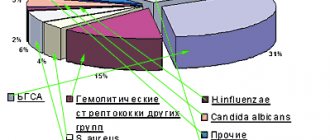
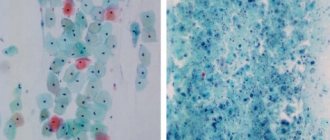
Метод КТ-диагностики для выявления фиброза легких
Фиброз — это разрастание соединительной ткани с появлением рубцов из-за нарушения механизмов заживления раневой поверхности.
Когда заживление протекает неправильно, могут возникать рубцовые изменения, приводящие к тому, что орган не может функционировать в полном объеме.
Соответственно, фиброз легких представляет собой рубцовые изменения ткани легких. Количество клеток, способных насыщать кровь кислородом, уменьшается. Следовательно, снижается дыхательная эффективность — развивается дыхательная недостаточность, приводящая к интоксикации, сначала при нагрузке, при усугублении течения заболевания — в покое, а далее — даже во сне. Рубцовая ткань в легких не только обладает пониженными функциональными свойствами, но и служит прекрасной средой для развития присоединенных инфекций, например, таких как бактериальная (пневмококковая или стафилококковая) пневмония.
Фиброз легких — это исход воспаления тканей во время интерстициального (то есть с поражением межклеточной соединительной ткани) заболевания легких. К причинам развития подобного заболевания могут относиться травмы легких, высокая загрязненность окружающей среды, курение, вдыхание наркотических веществ, плесени, органической, асбестовой, кварцевой и угольной пыли, инфекционные, аутоиммунные, вирусные заболевания и их осложнения — бронхит, туберкулез, пневмония, COVID-19 и многое другое.
Еще недавно синонимом самих интерстициальных заболеваний был пневмофиброз, но, к счастью, было установлено, что не все варианты таких заболеваний легких являются фиброзирующими.
Самый сложный и практически не поддающийся лечению — первичный, или идиопатический фиброз легких — быстро прогрессирующее фиброзирующее заболевание легких, причина которого неизвестна.
Симптомы фиброза легких
Легочный фиброз характеризуется симптомами одышки и сухого кашля (редко продуктивного — с мокротой) при физической нагрузке, непрекращающейся болью в области грудной клетки, быстрой утомляемостью на фоне затрудненного дыхания, похудением без изменения диеты. При аускультации легких (выслушивании с помощью фонендоскопа) выявляются ранние (в фазе вдоха) инспираторные, то есть дыхательные хрипы, чаще всего локализующиеся в нижних задних зонах легких.
Фиброз может развиваться как в одном легком, так и в двух одновременно. Также возможны очаговая и тотальная формы фиброза. При тотальной форме зачастую требуется оперативное вмешательство, так как поражена большая часть легких. При очаговой форме изменения носят локальный характер.
КТ-диагностика фиброза легких
Золотой стандарт диагностики фиброза легких — компьютерная томография высокого разрешения. КТ-диагностика легочного фиброза позволяет достоверно выявить степень поражения легких, определить локализацию рубцовой ткани. Этот метод диагностики признан одним из самых чувствительных неинвазивных методов выявления легочного фиброза. Так, проведенные сравнительные исследования уже в 1990 году показали, что фиброз легких с помощью компьютерной томографии в режиме высокого разрешения (КТВР) был обнаружен в 91% случаев и только в 39% — с использованием рентгенографии органов грудной клетки.
При наличии фиброза легких в серьезной стадии на КТ виден паттерн (термин, принятый для обозначения патологических признаков в медицине) так называемого «сотового» легкого — это состояние видно на сканах как однотипные, расположенные в несколько рядов кисты, содержащие воздух, в пораженных частях одного или обоих легких. На ранних стадиях легочного фиброза подобная картина не наблюдается, поэтому потребовался поиск признаков на КТ, позволяющих выявить болезнь в ее начале. Одним из таких признаков оказалось наличие на снимках картины «матового стекла» — очагов незначительного уплотнения легочной ткани. Также специфические признаки фиброза у пациента можно обнаружить при проведении КТ легких с функциональными пробами. Так, один из признаков — субплевральное усиление периферического легочного интерстиция — ранее считался признаком отсутствия патологии. Подобные изменения практически невозможно отследить при помощи других методов аппаратной диагностики.
На данный момент точность методов КТ-диагностики растет благодаря введению новых протоколов исследований и тщательного изучения результатов многочисленных исследований. При этом ведущая роль в диагностическом процессе отводится врачу-рентгенологу, который трактует видимые изменения как легочный фиброз или его отсутствие. Поиск ранних лучевых признаков фиброзирующей болезни легких — ключевой момент для своевременного назначения противофибротической терапии.
Также именно мультисрезовая КТ при поставленном диагнозе используется для оценки скорости прогрессирования заболевания, выявления благоприятного и неблагоприятного типов фиброзных изменений, успеха лечения и правильности подбора терапевтический препаратов.
Актуальные подходы в терапии идиопатического легочного фиброза
Проведение рентген-морфологических сопоставлений и изучение особенностей патогенеза ИЛФ позволило выделить его отличительные от других интерстициальных заболеваний легких (ИЗЛ) черты. Выявление признаков обычной интерстициальной пневмонии (ОИП) на компьютерной томограмме или в биоптате легочной ткани при отсутствии известных причин и факторов, ассоциирующихся с поражением легочного интерстиция, легло в основу диагностики ИЛФ. Однако до настоящего времени проблема фенотипирования ИЛФ не утратила своей актуальности. Как оказалось, тяжесть болезни, оцененная по скорости прогрессирования легочной дисфункции, не определяется исключительно данными КТ, которые используются для диагностики ИЛФ, а высокий (более 50%) процент не прошедших скрининг пациентов в ряде международных РКИ свидетельствует о наличии большого сходства этой патологии с другими ИЗЛ.
Результаты изучения механизмов фиброзообразования в легочной ткани при ИЛФ позволили сформулировать концепцию развития фиброза как следствие дисфункции альвеолярного эпителия, наступившей спонтанно или возникшей в результате повреждения неизвестным агентом. Нарушение процесса репарации эпителия (вероятно, и сосудистого эндотелия) при персистировании повреждающего механизма сопровождается миграцией миофибробластов в утратившую регенераторную способность альвеолярную ткань, увеличением их местного количества, повышением синтеза компонентов экстрацеллюлярного матрикса и отложением его в легочную ткань, что, в конечном счете, приводит к ее необратимому ремоделированию.
Несмотря на многочисленные исследования, не удается объяснить возникновение ИЛФ у конкретного пациента и существенные различия в скорости прогрессирования ИЛФ у разных больных (кроме случаев генетически детерминированной патологии), что подтверждает концепцию о существовании различных болезней, объединенных единым термином ИЛФ.
Малая продолжительность жизни больных ИЛФ (медиана выживаемости с момента установления диагноза составляет 2–3 года, а 5-летняя выживаемость не превышает 50%) и неэффективность противовоспалительной и иммуносупрессивной терапии обусловили отношение к этому заболеванию как к потенциально фатальному и неподдающемуся терапевтическому лечению, тогда как больший или меньший позитивный эффект глюкокортикостероидов и иммуномодулирующей терапии (азатиоприна, метотрексата, циклофосфамида, циклоспорина, ритуксимаба, микофенолата мофетила) отмечается при других ИЗЛ. Вместе с тем вопрос соотношения пользы и риска применения иммуномодулирующих препаратов при ИЗЛ не решен, их использование при этих заболеваниях не одобрено в большинстве стран мира и остается предметом дискуссий.
Появление в 2014 г. данных исследования эффективности нинтеданиба и пирфенидона у больных ИЛФ доказало возможность медикаментозного воздействия на его патогенетические механизмы и ознаменовало начало нового периода в изучении этой патологии. Ингибитор протеинкиназы нинтеданиб в исследованиях INPULSIS и INPULSIS ON продемонстрировал клиническую эффективность при ИЛФ, достоверно уменьшая скорость потери ФЖЕЛ, частоту обострений заболевания и снижая риск смерти от респираторных причин за время лечения. В настоящее время нинтеданиб одобрен для лечения ИЛФ.
Его противофиброзный эффект реализуется на уровне рецепторов к фактору роста фибробластов, а также тромбоцитарному и сосудистому эндотелиальному факторам роста и заключается в снижении синтеза профиброзных цитокинов, ограничении возможности трансформации фибробластов в миофибробласты, подавлении их миграции в альвеолярный интерстиций и продукции компонентов экстрацеллюлярного матрикса.
Данные проведенных исследований позволяют утверждать об имеющемся различии в клинико-рентгенологических проявлениях ИЛФ, скорости прогрессирования заболевания и реакции на лечение у разных пациентов, что определяет актуальность поиска биомаркеров для группировки больных ИЛФ по их чувствительности к той или иной «таргетной» терапии. Эта задача еще не решена и требует большего количества данных, которые до настоящего времени были получены в основном при ретроспективных исследованиях, проведенных на небольших группах больных. Кроме того, общие с ИЛФ биомаркеры, возможно, существуют при других хронических ИЗЛ.
Картина прогрессирующего легочного фиброза с развитием тяжелой дыхательной недостаточности, резистентность к имуномодулирующей терапии и невысокая продолжительность жизни наблюдается у ряда пациентов с гиперчувствительным пневмонитом (ГП), идиопатической неспецифической интерстициальной пневмонией (НСИП), а также при поражении легких у больных склеродермией, ревматоидным артритом, интерстициальной пневмонией с аутоимунными проявлениями, изменения на КТ у которых соответствуют картине ОИП.
Выявляется схожая зависимость между скоростью снижения ФЖЕЛ и показателем смертности при ИЛФ, ГП, поражении легких при системной склеродермии и ревматоидном артрите. Нарушения структуры и функции альвеолярного эпителия, которые характерны для ИЛФ, были обнаружены при тяжелом течении хронического ГП, саркоидоза легких, НСИП, а также ИЗЛ, ассоциирующихся с диффузными заболеваниями соединительной ткани. Таким образом, процессы фиброзообразования при этих разных по сути болезней протекают (по крайней мере, в определенные этапы своего развития) по схожему сценарию. Полученные данные дают основание для выделения «прогрессирующего фиброзного фенотипа» ИЗЛ, что подразумевает наличие легочного фиброза как составляющей части сложного патогенетического процесса, существующего независимо от начальных триггерных факторов и обладающего способностью к самоподдержанию, прогрессированию и определяющего тяжесть и прогноз заболевания.
Вопрос о целесообразности изменения существующей номенклатуры ИЗЛ и места в ней ИЛФ в настоящее время обсуждается ведущими мировыми экспертами. Объединение заболеваний, различающихся по этио-патогенетическим признакам, в общий «прогрессирующий фиброзный фенотип» требует поиска биомаркеров, отражающих механизмы развития легочного фиброза, и может оказаться актуальным в свете возможности таргетной терапии, модифицирующей течение болезни. В этой связи использование нинтеданиба, доказавшего свою эффективности при ИЛФ, может оказаться перспективным и при других ИЗЛ, протекающих с выраженным легочным фиброзом.
С целью оценки новых возможностей терапии фиброзирующих ИЗЛ были инициированы мультицентровые двойные слепые плацебо-котролируемые клинические исследования эффективности и безопасности нинтеданиба III фазы: SENSCIS и INBUILD. Пациенты с ИЛФ в эти исследования не привлекались. В исследовании SENSCIS, начатом в 2015 году, проводилось изучение эффектов терапии нинтеданибом больных системной склеродермией с поражением легких. Оценивалась скорость прогрессирования заболевания по изменению ФЖЕЛ, а также динамика кожных проявлений системной склеродермии и показателей качества жизни. Завершение исследования ожидается к концу 2021 года. Исследование INBUILD, начатое в 2021 году, ставит целью изучение эффективности и безопасности нинтеданиба у больных с легочными проявлениями системных заболеваний соединительной ткани (ревматоидного артрита, системной склеродермии, смешанного заболевания соединительной ткани), а также пациентов с ГП, НСИП, неклассифицируемым легочным фиброзом, саркоидозом легких, пневмокониозами, асбестозом и другими фиброзирующими ИЗЛ, у которых изменения на КТ соответствуют ОИП либо ОИП без признаков «сотового легкого». Прогрессирующий характер легочного фиброза в этом исследовании оценивался при помощи универсальных критериев для всех включенных нозологий: снижение ФЖЕЛ на 5–10% за 24 месяца, увеличение выраженности признаков легочного фиброза на КТ и усиление одышки. Гипотеза, выдвинутая исследователями, заключается в том, что эффективность нинтеданиба при фиброзирующих ИЗЛ сопоставима с таковой у больных ИЛФ, в частности, замедление потери ФЖЕЛ за год лечения может составить 50%.
Остается полагать, что если эффективность и безопасность нинтеданиба, ранее доказанная при ИЛФ, будет установлена и в ходе этих исследований, появится дополнительное основание для выделения единого фиброзного фенотипа ИЗЛ, а медицинское сообщество получит возможность обоснованно применять нинтеданиб для патогенетической терапии прогрессирующего легочного фиброза у больных различными ИЗЛ.
Идиопатический легочный фиброз (ИЛФ), которому морфологически соответствует обычная интерстициальная пневмония (ИП), может претендовать на роль одного из наиболее прогностически неблагоприятных вариантов интерстициального легочного поражения, для которого характерны быстрый темп формирования практически необратимого ЛФ с тяжелой дыхательной недостаточностью и легочной гипертензией. Тактика лечения ИЛФ остается преимущественно патогенетической, принципиально не отличающейся от используемой при других ИП; при этом ее особенности во многом определяются индивидуальным опытом конкретного клинического центра. В связи с этим значение консенсусных рекомендаций ряда профессиональных обществ, опубликованных в 2011 г., трудно переоценить с точки зрения высокой актуальности попыток унификации тактики ведения ИЛФ. Трудность практической реализации этих попыток понятна прежде всего с учетом явного недостатка клинических исследований, включающих больных ИЛФ, которые были бы проведены с учетом стандартов медицины, основанной на доказательствах.
В рекомендациях 2011 г. ИЛФ определен как специфическая форма хронической прогрессирующей фиброзирующей ИП неизвестного происхождения, наблюдающейся преимущественно среди взрослых, особенно среди пожилых, и не имеющей черт системного заболевания. Диагноз ИЛФ требует обязательного исключения провоцирующей роли известных этиологических факторов интерстициальных заболеваний легких (например, профессиональных), наличия характерных признаков обычной ИП, регистрируемых при компьютерной томографии (КТ) высокого разрешения. Признается, что точность диагноза ИЛФ возрастает при проведении биопсии легких (предпочтительно хирургической, но не трансбронхиальной), а течение заболевания, как правило, отличается неуклонным прогрессированием: только у небольшой части пациентов легочный процесс стабилизируется, но при этом возможны повторные его обострения. Следует подчеркнуть, что ИЛФ безусловно следует рассматривать как один из самых неблагоприятных вариантов интерстициальных заболеваний легких: именно у страдающих им пациентов максимален темп формирования необратимого ЛФ вплоть до стадии сотового легкого и тяжелой хронической дыхательной недостаточности. Названные особенности клинической эволюции ИЛФ во многом связаны с профилем экспрессии воспалительных цитокинов и хемокинов легочной тканью, типичных для данного заболевания: в сопоставлении с другими формами ИП именно при ИЛФ максимальна экпрессия трансформирующего фактора роста-β [3].
Особенности экспрессии медиаторов воспаления и фиброза, а также имеющиеся описания семейных случаев ИЛФ [4] заставляют обсуждать вклад генетических детерминант в его развитие. Вместе с тем уже сегодня очевидно, что ИЛФ не является моногенным заболеванием, не удастся идентифицировать те генетические детерминанты, которые бы четко формировали предрасположенность к болезни и/или модулировали ее развитие у заметной части больных. Неоднократно предпринимались попытки демонстрации вклада полиморфизма отдельных генов в прогрессирование ИЛФ. Продемонстрировано, что у курильщиков, страдающих ИЛФ, достоверно чаще встречается ТТ755-вариант гена матриксной металлопротеиназы-1, выявляемый на фибробластах [5]. Недавно опубликованный мета-анализ N.M. Korthagen и соавт. (2012) [6] показал значение отдельных вариантов гена, кодирующего белок-антагонист рецептора к интерлейкину-1 как фактора риска ИЛФ. Показана также ассоциация ИЛФ с носительством 308А-аллеля гена фактора некроза опухоли α как в гетеро- (вероятность возрастает в 2,9 раза), так и в гомозиготной (вероятность возрастает в 13,9 раза) форме [7]. G6A-полиморфизм гена ангиотензиногена, как продемонстрировали M. Molina-Molina и соавт. (2008) [8], может оказывать влияние на течение ИЛФ, в частности на выраженность респираторных нарушений, но не на формирование предрасположенности к нему. Интенсивное прогрессирование ИЛФ может отражать и максимальная экспрессия матриксной металлопротеиназы-9 клетками из бронхо-альвеолярного лаважа [9]. Сопоставление генетического “портрета” легочной ткани, полученной с помощью биопсии у пациентов с ИЛФ и пневмонитом, обусловленным реакциями гиперчувствительности, показало, что для ИЛФ типична преимущественная экспрессия генов тканевого ремоделирования, пролиферации эпителиоцитов и фибробластов, в то время как гиперчувствительность характеризуется преимущественной экспрессией генов воспаления и активации Т-лимфоцитов [10]. В целом рекомендации 2011 г. подчеркивают, что ИЛФ не следует рассматривать в ряду генетически детерминированных заболеваний. Вместе с тем дальнейший поиск определенных генетических детерминант развития и прогрессирования заболевания, очевидно, оправдан, поскольку позволяет приблизиться к пониманию патогенетических особенностей ИЛФ, которые в будущем могли бы стать объектом для воздействия специально разработанных таргетных терапевтических стратегий.
В рекомендациях 2011 г. подробно обсуждается значение других потенциальных этиологических факторов ИЛФ, представляющих интерес прежде всего в применении соответствующих методов лечения. Среди них особое значение имеет курение. Еще в начале 1990-х гг. H. de Cremoux и соавт. (1990) [11] продемонстрировали, что больные ИЛФ-курильщики отличаются преобладанием лимфоцитов в бронхо-альвеолярном смыве, худшим ответом на глюкокортикостероиды и худшей выживаемостью. Установлено также, что курильщики, страдающие ИЛФ, отличаются наиболее выраженными респираторными нарушениями [12]. Многоцентровое клиническое исследование, включившее 248 больных ИЛФ, показало, что курение сопряжено с достоверным увеличением риска развития ИЛФ в 1,6 раза. Бывшие курильщики также характеризовались повышенным риском ИЛФ (отношение шансов – 1,9), у курильщиков со стажем от 21 до 40 пачколет он был максимальным (отношение шансов – 2,3) [13]. Установлено также, что курильщики, в т. ч. бывшие, имеющие ИЛФ, отличаются заметно худшей выживаемостью [14]. Можно утверждать, что у всех больных ИЛФ следует использовать всевозможные средства лечения никотиновой зависимости, хотя курение и не является облигатным фактором риска ИЛФ.
Среди возможных детерминант ИЛФ называют и различные факторы внешней среды, в т. ч. металлическую пыль (медную, стальную, свинцовую) [15]. В качестве потенциальных факторов развития ИЛФ может также рассматриваться органическая пыль: известны случаи развития ИЛФ среди сельскохозяйственных рабочих, птицеводов, животноводов [16]. Тем не менее с точки зрения эпидемиологии связь между ИЛФ и факторами внешней среды пока убедительно не подтверждена, и каждый конкретный пациент, у которого подобная связь предполагается, нуждается в особенно детальном обследовании и обсуждении, очевидно, консилиумом специалистов. Интерпретация роли экзогенных факторов в развитии ИЛФ должна быть весьма осторожной, особенно когда в качестве одного из доказательств используется профессиональный маршрут пациента.
В качестве провокаторов развития ИЛФ обсуждаются также различные инфекционные агенты, прежде всего вирусы: Эпштейна–Барр, цитомегаловирус, вирусы герпеса типа 7 и 8 [17, 18]. Вместе с тем, несмотря не то что ДНК этих вирусов удавалось обнаружить, в т. ч. и в образцах легочной ткани, полученных при биопсии, частота их выявления в целом не отличается от таковой у пациентов с интерстициальными легочными процессами другой природы. В связи с этим значение подавляющего большинства вирусов, в т. ч. Эпштейна–Барр и представителей группы герпес, которым приписывают роль в развитии многих вариантов иммунопатологических поражений внутренних органов, в частности системных заболеваний, как факторов риска ИЛФ не стоит преувеличивать, тем более необоснованно проведение противовирусной терапии у этой категории больных.
В качестве одного из наиболее реальных факторов риска ИЛФ называют хроническую HCV-инфекцию [19], хотя частота ее обнаружения у этой категории пациентов, по данным различных клинических исследований, существенно варьируется. В первой половине 1990-х гг. T. Ueda и соавт. (1992) [20] продемонстрировали, что в сопоставлении со здоровыми представителями контрольной группы наличие анти-HCV-антител в сыворотке крови больных ИЛФ удается констатировать почти в 8 раз чаще. Обследование коренных жителей Италии, страдавших ИЛФ, показало, что наличие антител к HCV удается обнаруживать у 13,3 % из них, только у 0,3 % доноров крови и у 6,1 % пациентов, страдающих другими интерстициальными заболеваниями легких, но не ИЛФ [21]. Имеются указания на то, что НСV-инфекция не только более распространена среди пациентов с ИЛФ, но и может рассматриваться в ряду факторов риска его развития. Y. Arase и соавт. (2008) [22] наблюдали за группой из 6150 больных HCV-инфекцией и 2050 пациентов с HBV-инфекцией, средняя продолжительность наблюдения составила 8,0 ± 5,9 для HCV- и 6,3 ± 5,5 лет для HBV-инфицированных. В течение периода наблюдения ИЛФ развился у 15 HCV-инфицированных и ни у одного из HBV-инфицированных. Суммарная частота развития ИЛФ при наличии HCV-инфекции составила 0,3 % к 10-му году наблюдения и 0,9 % к 20-му. ИЛФ, таким образом, достоверно чаще развивался среди HCV-инфицированных по сравнению с HBV-инфицированными. Факторами риска ИЛФ у лиц с хронической HCV-инфекцией были возраст ≥ 55 лет, злостное курение или наличие цирроза печени. Cледует подчеркнуть, что развитие ИЛФ при HCV-инфекции может ассоциироваться с криоглобулинемией и типичным для нее поражением внутренних органов: имеются сообщения об эффективности в этой ситуации противовирусной терапии (интерферон-альфа) [23]. По-видимому, каждый случай ИЛФ, ассоциированного с HCV-инфекцией, целесообразно, по крайней мере первоначально, рассматривать как ее внепеченочное проявление; тем не менее у подобных пациентов эффективность противовирусной терапии с точки зрения влияния на легочный процесс не установлена и для них, как правило, приходится применять глюкокортикостероиды и цитостатики.
Рекомендации версии 2011 г. в качестве одного из приоритетных факторов риска ИЛФ рассматривают гастро-эзофагеальный рефлюкс (ГЭР). Считают, что наблюдающиеся при нем микроаспирации агрессивного желудочного содержимого могут обусловливать сочетанное химическое, иммунологическое и бактериальное повреждение легких, реализующееся формированием ИЛФ [24]. По некоторым данным [25], ГЭР может быть выявлен у подавляющего большинства больных ИЛФ, и именно у них он достигает максимальной выраженности. ГЭР удается обнаружить у 65 % больных ИЛФ, являющихся кандидатами на трансплантацию легких. В целом уже сегодня можно говорить, что лечение ГЭР обоснованно для всех пациентов ИЛФ, поскольку, не будучи основным терапевтическим подходом, оно все же может способствовать улучшению прогноза. J.S. Lee и соавт. (2011) [26] недавно опубликовали результаты анализа влияния ГЭР и ее терапии на выживаемость больных ИЛФ. Всего были проанализированы 204 пациента, из которых у 34 % имелись характерные для ГЭР жалобы, у 45 % – наличие подтвержденного ГЭР в анамнезе, 47 % принимали лекарства по поводу ГЭР. Оказалось, что прием лекарственных препаратов, используемых для лечения ГЭР, сопряжен с увеличением выживаемости больных ИЛФ и уменьшением площади ЛФ, оцененной на КТ. Очевидно, что обследование, направленное на выявление ГЭР, и максимально активное его лечения оправданны для всех больных ИЛФ.
В рекомендациях версии 2011 г. четко приведены диагностические критерии ИЛФ:
• отсутствие возможных причин ИЛФ (экзогенные факторы, в т. ч. профессиональные, системные заболевания, прием лекарственных препаратов);
• наличие признаков обычной ИП на компьютерных томограммах высокого разрешения (достаточный признак для тех, кому не выполняли биопсию легких);
• наличие признаков обычной ИП при КТ высокого разрешения и характерных морфологических черт в образцах ткани легкого, полученных при хирургической биопсии.
Принципиально важно, что в данной версии рекомендаций четко постулировано, что ИЛФ не является только клиническим диагнозом и его подтверждение требует обязательного использования КТ, по возможности – проведения хирургической (но не трансбронхиальной) биопсии легкого. Следует, тем не менее, подчеркнуть, что обоснование применения этих методов невозможно без тщательного анализа деталей анамнеза легочного процесса и правильной интерпретации данных, получаемых при общеклиническом обследовании. В целом ИЛФ нередко диагностируют поздно, и назначению патогенетической терапии часто предшествует несколько (не менее 1,5) лет применения повторных курсов различных антибактериальных препаратов [3], применяемых по поводу мнимой “хронической” бактериальной пневмонии. ИЛФ необходимо предполагать всегда, когда при аускультации легких единственным выслушиваемым дополнительным феноменом остается крепитация, особенно билатеральная и распространяющаяся, без смены ее влажными хрипами, типичными при характерном для истинной бактериальной пневмонии вовлечении в воспалительную инфильтрацию стенок мелких бронхов. Лихорадка и другие общие симптомы интоксикации, свойственные пневмонии, при ИЛФ, как правило, отсутствуют: на первый план в клинической картине выступает прогрессирующая дыхательная недостаточность. У подобных пациентов всегда следует в первую очередь исключать интерстициальные заболевания легких, в частности ИЛФ, а длительная терапия антибактериальными препаратами приносит им вред как с точки зрения драматического увеличения риска реализации нежелательных явлений, так и в связи с тем, что при этом не применяются более эффективные методы патогенетической терапии.
В целом сегодня можно говорить о том, что использование КТ высокого разрешения и хирургической (в т. ч. трансторакальной) биопсии легкого позволяет четко подтвердить ИЛФ у большинства пациентов, действительно страдающих этим заболеванием. Признаки ИЛФ, которые следует выявлять с помощью этих диагностических методов, определены в рекомендациях версии 2011 г. (см. таблицу).
В отличие от диагностической тактики при ИЛФ тактика лечения данного заболевания пока далеко не идеальна, прежде всего потому, что в контролируемых клинических исследованиях не удалось подтвердить влияние терапевтических стратегий, использующихся в рутинной клинической практике наиболее часто. В рекомендациях версии 2011 г. признано нецелесообразным применение в лечении ИЛФ глюкокортикостероидов, большинства цитостатиков (циклофосфамид, азатиоприн), циклоспорина, интерферона-гамма-1, ацетилцистеина и антикоагулянтов в монотерапии и в комбинациях. К сожалению, пока не приходится говорить и об обоснованности применения тех препаратов, которые рассматривают в качестве перспективных (этанерсепт, бозентан, который был бы особенно оправдан с учетом наличия у большинства больных ИЛФ легочной гипертензии), в т. ч. антифибротического агента пирфенидона, который, по данным отдельных клинических исследований [26], оказывает положительное влияние на респираторную функцию и выживаемость пациентов с ИЛФ. Обсуждение силденафила (мишень его действия та же, что и у ранее упоминавшегося антагониста эндотелина-1 бозентана) и иматиниба мезилата в рекомендациях 2011 г. не привело к констатации целесообразности или нецелесообразности их использования. Показания к началу длительной оксигенотерапии рекомендовано определять индивидуально. В качестве предпочтительного метода лечения ИЛФ рассматривается трансплантация легких, показавшая позитивное влияние на прогноз [27]. Тем не менее не следует принимать данный раздел рекомендаций безоговорочно, и у больных ИЛФ, особенно при относительно ранней его диагностике, тактика иммуносупрессивной терапии может быть активной, включающей использование глюкокортикостероидов и цитостатиков (например, циклофосфамида), в т. ч. в сверхвысоких дозах. Пассивное ожидание формирования показаний к трансплантации легких недопустимо, в т. ч. и с учетом малой доступности этого вмешательства в нашей стране.
Безусловно рекомендации по ИЛФ версии 2011 г. – важный шаг вперед на пути выработки согласованных позиций экспертов, касающихся ведения данного заболевания. Факторы риска, подходы к диагностике ИЛФ в настоящее время в целом не вызывают сомнений; ключевым является и предложенный комитетом экспертов междисциплинарный подход к ведению ИЛФ. Трудности определения терапевтической тактики и отсутствие четких доказательств эффективности большинства применяемых в настоящее время препаратов должны стать стимулом для проведения новых контролируемых клинических исследований.
Что такое фиброз печени
Фиброз печени – это рубцевание ткани. Печень способна восстанавливаться, однако, эта система не работает на полную мощность, если печень поражена, либо травма является продолжительной и очень серьезной. Все попытки регенерации вызывают скопление соединительной ткани (это жесткие, инертные волокна) вместо функционирующих клеток печени.
Фиброз печени – это не конкретное заболевание, а скорее симптом другой проблемы с печенью. Наиболее частыми состояниями, которые приводят к фиброзу печени, являются алкоголизм, хронический гепатит С и неалкогольная жировая болезнь печени (НАЖБП).
Сам по себе фиброз печени не вызывает никаких симптомов. Врачи могут обнаружить признаки фиброза печени с помощью анализов крови и УЗИ, КТ или МРТ. Если он обнаружен рано, его можно вылечить. Но если он остается незамеченным и повреждение продолжается, фиброз может прогрессировать до цирроза.
Степени фиброза печени у взрослых
Специалисты выделяют 5 степеней рубцевания ткани печени.
Нет фиброза.
В этом случае нет признаков гибели клеток печени (некроза) или рубцевания, несмотря на воспаление печени (гепатит).
Портальный (легкий) фиброз.
В этом случае есть участки некроза и рубцевания, затрагивающие малые и средние ветви воротной вены, несущий кровь из тонкой кишки. Структура и функция печени остаются в норме.
Перипортальный (умеренный) фиброз.
Это вариант с увеличением очагов некроза, рубцеванием и нарушением функции печени.
Мостовидный (тяжелый) фиброз.
На этой стадии рубцевание нарушило нормальный кровоток в печени, и функция еще больше нарушилась.
Цирроз.
Это постоянное рубцевание и необратимая потеря функции печени.
Популярные вопросы и ответы
На популярные вопросы о фиброзе печени мы попросили ответить врача-гастроэнтеролога Валерию Ломову.
Чем опасен фиброз печени?
Опасность фиброза заключается в том, что он никак себя не проявляет в течение длительного времени – пациент не заявляет о жалобах и не обращается за помощью в медицинское учреждение. При этом фиброз может прогрессировать, происходит нарушение всех функций печени, что ведет к катастрофе во всем организме.
У кого вероятен фиброз печени?
В группе риска находятся:
- пациенты с вирусными гепатитами В и С;
- пациенты, употребляющие алкоголь в гепатотоксичиных дозах более 5 лет;
- люди, страдающие ожирением, аутоиммунными заболеваниями печени, а также болезнями накопления (гемохроматоз, болезнь Вильсона).
Развитие фиброза печени также возможно при токсическом действии некоторых групп лекарственных препаратов.
Может ли фиброз вылечить полностью?
Регресс фиброза возможен на всех стадиях. Но если он перешел в цирроз – это уже точка невозврата.
Какие могут быть осложнения при фиброзе печени?
При длительном течении фиброза печени может развиваться цирроз печени, при котором происходит полное замещение здоровой ткани соединительной с нарушением всех функций печени, что может привести к летальному исходу.
Диагностика и лечение
Для диагностики легочного фиброза врач-пульмонолог проводит следующие анализы и исследования: общий анализ крови; рентгенография грудной клетки; компьютерная томография легких, магнитно-резонансная томография легких; биопсия легкого; дыхательные тесты. Лечение фиброза легкихопределяется квалифицированным специалистом в зависимости от особенностей течения заболевания у конкретного человека. К тяжелым формам фиброза применяются глюкокортикоиды, цитостатики и иммунодепрессанты. Пораженные фиброзом легкие часто становятся благоприятной средой для присоединения патогенной микрофлоры и развития воспаления. Чтобы воспрепятствовать этому, назначаются антибактериальные препараты, полезными будут кислородные ингаляции и сердечные гликозиды. При изнуряющем кашле и одышке назначаются бронхорасширяющие препараты. Медикаментозное лечение фиброза легких должно быть подкреплено лечебной дыхательной гимнастикой, в то время как крупные физические нагрузки больному противопоказаны. Также необходимо исключить воздействие на организм провоцирующих фиброз факторов.
Симптомы фиброза легких
На начальном этапе заболевание проявляется общей слабостью и повышенной утомляемостью. У пациентов отмечается бледность кожи с синюшным оттенком, особенно в области носогубного треугольника, носа и на конечностях. Многие больные отмечают сонливость днем и бессонницу ночью, а также немотивированное снижение веса.
Затем к вышеперечисленным жалобам присоединяется одышка. В начале она беспокоит больного только во время физических нагрузок, но по мере прогрессирования патологии начинает возникать и в покое.
У части пациентов отмечается сухой или влажный, малопродуктивный кашель. Во втором случае обнаруживается скудное количество вязкой слизистой мокроты. Появление гнойного отделяемого говорит о присоединении вторичной бактериальной инфекции.
У пациентов, длительно страдающих фиброзом легких, происходит изменение формы ногтей, которые становятся похожи на «часовые стекла» и концевых фаланг пальцев по типу «барабанных палочек».
На пике развития заболевания возникает сердечная недостаточность, проявляющаяся периферическими отеками, сердцебиением, аритмией, пульсацией шейных вен, тяжелой одышкой в состоянии покоя.
Причины
Легочный фиброз может быть вызван различными причинами, в том числе:
- хроническими воспалительными процессами в легких (например, саркоидозом или гранулематозом Вегенера);
- инфекциями, влиянием факторов окружающей среды (асбест, кремний, воздействие некоторых газов);
- воздействием ионизирующих газов (например, лучевой терапии, применяемой для лечения опухолей груди);
- хронических аутоиммунных заболеваний (волчанка, ревматоидный артрит);
- приемом некоторых лекарств.
При аллергической пневмонии фиброз легких может развиваться как следствие повышенной иммунной реакции на органическую пыль или химические вещества, которые попадают в легкие во время вдоха. У некоторых людей фиброз может развиваться без какой-то определенной причины. В этом случае, как правило, говорят об идиопатическом легочном фиброзе, который не поддается терапевтическому лечению, в то время как при других типах фиброза (к примеру, интерстициальной пневмонии) состояние пациента улучшается при правильно подобранном лечении.
Публикации в СМИ
Идиопатический фиброзирующий альвеолит — патологический процесс в лёгких неясной природы, характеризующийся воспалением и прогрессирующим фиброзом лёгочной интерстициальной ткани и воздухоносных пространств, дезорганизацией структурно-функциональных единиц паренхимы, развитием нарастающей дыхательной недостаточности.
Классификации. Ранее идиопатический фиброзирующий альвеолит разделяли на муральную, десквамативную и смешанную формы. В настоящее время используют несколько классификации, разделяя идиопатический фиброзирующий альвеолит в зависимости от морфологии, гистологической картины и клинических проявлений • Морфологическая классификация идиопатических интерстициальных пневмоний •• Обычная интерстициальная пневмония •• Десквамативная интерстициальная пневмония (выделяют также респираторный бронхиолит и интерстициальное заболевание лёгких) •• Облитерирующий бронхиолит с организующейся пневмонией •• Острая интерстициальная пневмония •• Неспецифическая интерстициальная пневмония • Гистологическая классификация идиопатических интерстициальных пневмоний (ATS/ERS, 2000) •• Обычная интерстициальная пневмония •• Альвеолярная макрофагальная пневмония •• Респираторный бронхиолит •• Организующаяся пневмония •• Диффузное альвеолярное повреждение •• Неспецифическая интерстициальная пневмония •• Лимфоцитарная интерстициальная пневмония • Клиническая классификация идиопатических интерстициальных пневмоний (ATS/ERS, 2000) •• Идиопатический фиброзирующий альвеолит (идиопатический лёгочный фиброз, криптогенный фиброзирующий альвеолит) •• Десквамативная интерстициальная пневмония •• Респираторный бронхиолит, интерстициальное заболевание лёгких •• Криптогенная организующаяся пневмония (идиопатический облитерирующий бронхиолит с организующейся пневмонией) •• Острая интерстициальная пневмония •• Неспецифическая интерстициальная пневмония •• Лимфоцитарная интерстициальная пневмония.
Частота • Заболевание чаще наблюдают у лиц в возрасте 50 лет и старше • В США распространённость 20 случаев на 100 000 мужчин и 13 на 100 000 женщин; заболеваемость 11 на 100 000 мужчин и 7 на 100 000 женщин • В Великобритании распространённость 6 случаев на 100 000 населения • В России точных статистических данных нет (за счёт гиподиагностики).
Этиология точно не известна. Факторы, способные вызвать первичное повреждение лёгочной ткани: табачный дым, металлическая, силикатная и древесная пыль, асбест, вирусы (вирусы гепатита С, герпесвирусы, в т.ч. Эпстайна–Барр и цитомегаловирус [ЦМВ]; аденовирусы). Установлена ассоциация между идиопатическим фиброзирующим альвеолитом и рефлюкс-эзофагитом.
Генетические особенности. Выявлена генетическая предрасположенность к избыточному фиброзообразованию в лёгких в ответ на неспецифическое повреждение эпителия (наличие семейных форм заболевания, частое развитие лёгочного фиброза при некоторых наследственных заболеваниях).
Патогенез • Острая стадия (форма) •• Повреждение клеток альвеолярного эпителия или эндотелия вдыхаемыми или поступающими с кровотоком патогенными факторами с последующим развитием интерстициального и внутриальвеолярного отёка (острый альвеолит) •• Выброс хемотаксических факторов активированными воспалительными и иммунными клетками •• Высвобождение медиаторов воспаления (оксидантов, цитокинов) и факторов фиброгенеза (например, фактора роста фибробластов, интерлейкин-1 [ИЛ-1]) •• Возможно как полное обратное развитие, так и прогрессирование до острой интерстициальной пневмонии • Хроническая стадия (форма) •• Процесс прогрессирует до обширного повреждения лёгкого и отложения коллагена (распространённый фиброз) •• Характерны гипертрофия гладкой мускулатуры и увеличение альвеолярных пространств за счёт разрывов стенок альвеол, выстланных атипичными (кубическими) клетками • Терминальная стадия •• Фиброзная ткань полностью замещает нормальные лёгочные структуры с образованием расширенных воздухоносных полостей •• Лёгочная ткань приобретает характерный вид «пчелиных сот».
Патоморфология • Скопление воспалительных клеток (преимущественно лимфоцитов и плазматических клеток), фибробластов и коллагеновых волокон в просвете терминальных и респираторных бронхиол и альвеол (фиброз лёгких) • Изменения преобладают в субплевральной области паренхимы лёгких и заднебазальных сегментах • Характерно развитие плотного фиброза лёгочной паренхимы с негомогенным типом морфологических изменений.
Клиническая картина • Клинические проявления отражают нарастающую дыхательную недостаточность. По скорости нарастания симптомов выделяют острое, хроническое и интермиттирующее течение • Жалобы на инспираторную или смешанную одышку, сухой кашель. Озноб и кашель с мокротой появляются при бактериальном суперинфицировании (осложнении). Часто утомляемость, общее недомогание, боли в груди ноющего характера, усиливающиеся при глубоком вдохе, позднее — снижение массы тела • Физикальное обследование на ранних стадиях может быть неинформативным •• У 40% больных повышается температура тела до субфебрильной и фебрильной, пик повышения приходится на середину дня •• При прогрессировании возникают тахипноэ, тахикардия, цианоз, деформация пальцев рук в виде «барабанных палочек» (при длительном течении заболевания) •• На вдохе слышна крепитация по типу «треска целлофана» (обычно в базальных отделах лёгких), на поздних стадиях — склеросифония (грубая крепитация, напоминающая звук трения пробки из пробкового дерева) •• Появляются признаки правожелудочковой недостаточности.
Лабораторные данные • Данные ОАК варьируют от нормы до выраженных отклонений: увеличение СОЭ, лейкоцитоз (чаще при присоединении бактериальной инфекции); на поздних стадиях характерны эритроцитоз и высокий Ht • Возможны повышение активности лактатдегидрогеназы (ЛДГ) сыворотки крови, наличие циркулирующих иммунных комплексов (ЦИК), сывороточных маркёров идиопатического фиброзирующего альвеолита — протеинов сурфактанта A и D, муциновых Аг KL-6, альвеоломуцина 3EG5.
Инструментальные данные • Рентгенография органов грудной клетки •• При минимальных изменениях на фоне выраженной клинической симптоматики: мелкоочаговая инфильтрация, сетчатость в средних или нижних долях лёгких (ретикулярные изменения) •• На поздних стадиях: картина «сотового лёгкого» • Рентгеновская КТ высокого разрешения: картина «матового стекла», утолщение и нерегулярность бронхиальных стенок; изменения в плевре и лимфаденопатия нехарактерны • ФВД: рестриктивный или смешанный тип нарушений (кривая поток-объём, общая плетизмография тела), снижение диффузионной способности лёгких; снижение растяжимости лёгких • ЭКГ: гипертрофия правых отделов сердца (следствие развития лёгочной гипертензии), возможны признаки гипоксии миокарда • Открытая или видеоторакоскопическая биопсия лёгких позволяет установить диагноз и определить прогноз заболевания (морфологический тип идиопатического фиброзирующего альвеолита) • Фибробронхоскопия позволяет провести дифференциальную диагностику с неопластическими процессами в лёгких (могут проявляться лёгочными диссеминациями) • Бронхоальвеолярный лаваж имеет вспомогательное значение; в лаважной жидкости выявляют преобладание нейтрофилов и эозинофилов, реже — лимфоцитоз.
Диагностическая тактика, алгоритмы диагностики. Для постановки диагноза необходимо присутствие четырёх больших критериев и (как минимум) трёх малых критериев • Большие критерии •• Исключение других интерстициальных заболеваний лёгких, вызванных известными причинами (приёмом ЛС, экспозицией вредных факторов внешней среды, системными заболеваниями соединительной ткани) •• Изменения ФВД, включающие рестриктивные изменения и нарушения газообмена •• Двусторонние ретикулярные изменения в базальных отделах лёгких с минимальными изменениями по типу «матового стекла» по данным КТ высокого разрешения •• По данным трансбронхиальной биопсии или бронхоальвеолярного лаважа нет признаков, свидетельствующих об альтернативном диагнозе • Малые критерии •• Возраст старше 50 лет •• Незаметное, постепенное появление одышки при физической нагрузке •• Длительность заболевания более 3 мес •• Инспираторная крепитация в базальных отделах лёгких.
Сопутствующие заболевания • Патология ССС вследствие преобладания пациентов старших возрастных групп • Ятрогенные состояния, вызванные применением ГК и цитостатиков (синдром Иценко–Кушинга, вторичный иммунодефицит).
Лечение • Общая тактика •• Специфического лечения идиопатический фиброзирующий альвеолит нет •• Противовоспалительная, антифиброзная, антиоксидантная и симптоматическая терапию • Режим зависит от состояния больного • Лекарственное лечение. Основа лечения — ГК и/или цитостатики как минимум в течение 6 мес. Обязателен тщательный контроль возможного развития побочных эффектов терапии •• На ранних стадиях — ацетилцистеин внутрь (600 мг 3 р/сут в течение 3 мес и более) •• ГК (например, преднизолон) ••• При дефиците массы тела в дозе 0,5 мг на 1 кг массы тела в сутки в течение 4 нед ••• При нормальной массе тела 0,25 мг на 1 кг массы тела в сутки в течение 8 нед ••• Затем дозу снижают до 0,125 мг/кг/сут или 0,25 мг/кг через день •• При дефиците массы тела ГК сочетают с азатиоприном в дозе 2–3 мг на 1 кг массы тела в сутки или с циклофосфамидом в дозе 2 мг на 1 кг массы тела в сутки. Максимальная доза для обоих препаратов составляет 150 мг/сут, начальная — 25–50 мг/сут. Дозу повышают на 25 мг каждые 1–2 нед до достижения максимальной дозы •• Антифиброзная терапия (пеницилламин) •• Бронходилататоры (b2-адреномиметики, холиноблокаторы или их сочетание в ингаляциях, аминофиллин в/в или пролонгированные формы теофиллина внутрь) целесообразны только при инструментально доказанной бронхиальной обструкции (не относят к специфическим признаком идиопатического фиброзирующего альвеолита) • Оксигенотерапия показана при paО2 менее 50–55 мм рт.ст • Хирургическое лечение — трансплантация лёгких.
Возрастные особенности • Основную группу пациентов составляют лица пожилого возраста, поэтому необходимо учитывать высокую вероятность сопутствующей патологии ССС • Беременность: целесообразность и риск вынашивания беременности зависит от степени дыхательной недостаточности и проводимой терапии.
Осложнения и их лечение • При развитии бронхоэктазов и их суперинфицировании необходимы антибактериальная терапия и трансбронхиальная санация • При пневмосклерозе, «сотовом лёгком», тяжёлой дыхательной недостаточности необходимо лечение основного состояния в сочетании с симптоматической терапией.
Диспансерное наблюдение, профилактика • Наблюдение у пульмонолога не реже 1 раза в 3 мес, длительно • Мониторинг состояния ФВД (кривая поток-объём, диффузионная способность лёгких), рентгенологическое исследование • Специфической профилактики не существует.
Течение и прогноз • Прогноз благоприятный при отсутствии прогрессирования или объективном улучшении после лечения, в остальных случаях — неблагоприятный • Прогноз зависит от течения: •• острое течение — смерть в течение 6 мес–2 лет c момента появления первых признаков заболевания; •• хроническое течение — постепенное прогрессирование с летальным исходном в среднем через 6 лет; •• рецидивирующее течение — средняя продолжительность жизни 2–5 лет • Благоприятные факторы: молодой возраст (моложе 50 лет), женский пол, менее 1 года c момента появления признаков заболевания, не очень выраженная одышка, сохранность показателей ФВД, наличие изменений по типу «матового стекла» по данным КТ высокого разрешения, увеличение доли лимфоцитов (20–25%) в бронхоальвеолярной лаважной жидкости, клиническое улучшение или стабильное течение заболевания через 3–6 мес терапии ГК.
Синонимы. Болезнь Хаммана–Рича (острая форма) • Синдром Хаммана–Рича (хроническая форма) • Идиопатический лёгочный фиброз • Криптогенный фиброзирующий альвеолит • Синдром Скеддинга • Склерозирующий альвеолит • Интерстициальная пневмония • Интерстициальный пневмонит • Диффузная интерстициальная болезнь лёгких • Фиброзная дисплазия лёгких.
МКБ-10 • J84.1 Другие интерстициальные лёгочные болезни с упоминанием о фиброзе • J84.9 Интерстициальная лёгочная болезнь неуточнённая