Томас В. Краус, висцеральный хирург-онколог
С 2005 года профессор Краус работает главным врачом кафедры общей и висцеральной хирургии клиники Нордвест в г. Франкфурт-на-Майне.
Подробнее о специалисте →
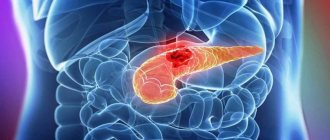
Существует несколько видов кистозных изменений в области поджелудочной железы, которые обнаруживаются, как правило, случайно. В 70-90% случаев речь идет о так называемых псевдокистах (пустотах, наполненных жидкостью), которые могут развиваться после острого или хронического воспаления. Кроме ложных, в 10-15% случаев кисты поджелудочной представляют собой кистозные отеки железы. При этом различают доброкачественные, злокачественные и пограничные новообразования. В последнем случае речь идет о пограничном качестве опухоли между доброкачественным и злокачественным. При гистологическом исследовании они рассматриваются как злокачественные предстадии опухоли.
Истинные доброкачественные кисты поджелудочной железы подразделяются на следующие типы:
- серозные цистоаденомы;
- муцинозные цистоаденомы;
- внутрипротоковые папиллярные муцинозные неоплазии.
Поскольку все эти опухоли имеют потенциал к злокачественному изменению, как правило, показано их хирургическое лечение.
Симптомы заболевания
Небольшие кисты поджелудочной железы, как правило, не имеют симптомов. В случае их появления, пациенты чаще всего жалуются на нехарактерные, иногда опоясывающие боли в области эпигастрия. Позже присоединяются отсутствие аппетита, потеря веса, тошнота и утомляемость. Если опухоль передавливает желчный проток на пути из печени в двенадцатиперстную кишку, может возникнуть желтуха. Однако все эти симптомы скорее являются неспецифическими, и это значительно затрудняет раннюю постановку диагноза. Чтобы выявить кисты поджелудочной железы, не опираясь на первичные признаки их проявления, необходимо регулярно проходить диагностику состояния своего здоровья. В Германии вы можете сделать это с помощью специальной программы чек-апов, разработанной клиникой «Нордвест» для своих пациентов.
Этиология кист забрюшинного пространства
Данный вид кист считается достаточно редким и на начальной стадии практически не проявляет себя, что определяет его опасность: по мере развития развивается нагноение, давление на внутренние органы и увеличивается риск разрыва оболочки. Вышеперечисленное несёт реальную угрозу здоровью пациента. Инициирующие факторы развития кист в забрюшинном пространстве заключаются в следующем:
- травматические повреждения области живота;
- наследственная предрасположенность;
- врождённые аномалии органов брюшной полости;
- паразитарные поражения;
- воздействия химической природы на область брюшины;
- кровоизлияния и воспалительные процессы внутренних органов.
Диагностика кистозных образований
После подробного изучения анамнеза и физикального осмотра пациента, проводится инструментальное обследование. Обычно для выявления кисты поджелудочной железы назначается тонкослойная компьютерная томография (КТ) живота, а также ЭРХПГ (эндоскопическая ретроградная холангиопанкреография), при которой осуществляется визуализация желчного и панкреатического протоков. При этом возможно выполнение эндоскопического ультразвукового обследования (УЗИ) и, в отдельных случаях, необходимо обследование окружающих сосудов, для чего проводят магнитно-резонансную томографию (МРТ).
Предоперационную биопсию при операбельных опухолях во избежание переноса опухоли не проводят.
Риск развития осложнений кисты забрюшинного пространства
Как уже упоминалось, опасность данного вида кист заключается в том, что на начальной стадии развития они практически ничем не проявлены. Пациент не обращается за профессиональной медицинской помощью, а новообразование тем временем растёт и уже через небольшой период времени представляет собой опасность для его здоровья и даже жизни.
Дело в том, что кисты большого диаметра оказывают давление на внутренние ткани и органы. Самым опасным их осложнением является самопроизвольное вскрытие капсулы, которое может случиться из-за удара в живот или вследствие физической нагрузки. В этом случае серозное или гнойное содержимое кисты попадает в брюшную полость и становится причиной интоксикации, которая требует срочной госпитализации.
Терапевтические меры
В зависимости от местоположения и размеров опухоли используются различные операционные методики. Целью всегда является полное удаление кисты поджелудочной железы во время операции в пределах здоровой ткани (R0). Поэтому во время хирургического вмешательства проводится цитологическое исследование тканей, чтобы при необходимости еще во время операции расширить ее объем и полностью удалить опухоль.
При локализации опухоли в области головки поджелудочной железы проводят ее резекцию с сохранением привратника или операцию по Уипплу (панкреатодуоденэктомию). При локализации кисты в хвосте поджелудочной проводят дистальную резекцию железы, при необходимости с удалением селезенки. Если же новообразование распространяется на оба отдела и является злокачественной, в редких случаях может быть показано полное удаление поджелудочной железы.
Гигрома
Артрит
21738 17 Декабря
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гигрома (суставная грыжа, синовиальная киста, ганглий): причины появления, симптомы, диагностика и способы лечения.
Определение
Гигрома – это доброкачественная кистозная опухоль, которая образуется из поверхностных оболочек сустава и представляет собой четко отграниченную капсулу, заполненную вязкой серозной жидкостью. Содержимое кисты – жидкость со слизью, белками и фибрином, что определяет ее желеобразное состояние. Размер образования колеблется от небольшой горошины до габаритов грецкого ореха и даже крупнее. Форма образования чаще всего округлая или вытянутая. Основание гигромы плотно связано с подлежащими тканями, а остальные поверхности подвижны и не спаяны с кожей и подкожной клетчаткой. Кожа над гигромой свободно смещается.
Гигрома представляет собой органоспецифическую кисту, формирующуюся только в непосредственной близости от сустава и не встречающуюся в других органах и тканях.
Причины появления гигромы
Предполагается, что первопричиной развития такой кисты является перерождение клеток соединительной ткани. При этом существует два вида клеток: веретенообразные – образуют капсулу, сферические – наполняются жидкостью, которая при повреждении стенок сухожильного футляра выливается в межклеточное пространство близлежащих тканей.
Перерождению клеток соединительной ткани способствуют травмы или растяжение сухожилий, воспаление суставной капсулы (бурсит, синовит артрит, тендовагинит и др.).
Кроме того, образование гигромы может быть объяснено наследственной предрасположенностью, а также являться следствием неправильно подобранной обуви.
Гигромы локализуются в области пальцев кисти, в области стопы, коленного или локтевого суставов, но наиболее частой локализацией (около 70%) является область лучезапястного сустава. Причина такой «избирательности» — каждодневная монотонная физическая нагрузка на упомянутые суставы и сухожилия у представителей определенных профессий. В группу риска входят:
- спортсмены (теннисисты, игроки в гольф, настольный теннис, бадминтон),
- музыканты (пианисты, скрипачи, виолончелисты),
- программисты,
- наборщики текста,
- массажисты, швеи, вышивальщицы и др.
Гигрома распространена как среди детей, так и среди взрослых, но чаще всего наблюдается у людей в возрасте 20–45 лет. Это кистозное образование не может исчезнуть самостоятельно, без лечебных мероприятий. Однако следует отметить, что гигромы никогда не перерождаются в рак, так что прогноз весьма благоприятный.
Классификация заболевания
Гигромы могут быть однокамерными и многокамерными. Последние появляются в результате нескольких излияний серозной жидкости и нередко локализуются в одной или нескольких областях.
По строению гигромы делятся на следующие виды:
- изолированная гигрома – вылившаяся жидкость находится в замкнутом пространстве, не имеет соединительного «русла» с сухожильным влагалищем;
- соустье – образуется новая полость, жидкость которой свободно перемещается из нее в сухожильное влагалище и обратно;
- клапан – серозная жидкость полностью перемещается в новое место, поскольку сформировавшийся в тканях барьер, называемый клапаном, препятствует ее возвращению в опустевшее влагалище.
Симптомы гиромы
В подавляющем большинстве случаев гигрома развивается медленно, бывает единичной, имеет диаметр не более 3 сантиметров, не вызывает боли и дискомфорта, поэтому ее замечают, когда она достигает достаточно внушительных размеров. Ранняя стадия заболевания характеризуется формированием небольшой кисты, возвышающейся над поверхностью кожи. Примерно в 35% случаев гигрома протекает бессимптомно. Достаточно редко, когда киста расположена под связкой, она может долгое время оставаться незамеченной. В таких случаях пациенты обращаются к врачу из-за боли и неприятных ощущений при сгибании сустава.
Если гигрома начинает сдавливать нервные окончания, то пациент может испытывать болезненные ощущения. Тупая боль распространяется на окружающие ткани и усиливается после интенсивной нагрузки.
В зависимости от локализации встречаются как совсем мягкие, эластичные, так и твердые опухолевидные образования, напоминающие по плотности кость или хрящ.
Кожа над гигромой может оставаться неизмененной либо становиться грубой, приобретать красноватый оттенок и шелушиться. После активных движений гигрома способна немного увеличиваться, но в покое снова возвращается к первоначальному размеру.
Диагностика гигромы
Обычно диагноз выставляется на основании анамнеза и характерных клинических проявлений.
Ультразвуковое исследование дает возможность не только увидеть кисту, но и оценить ее структуру, определить, есть ли в стенке гигромы кровеносные сосуды.
Послеоперационный период
После операции несколько дней пациент находится под наблюдением в палате интенсивной терапии. Уже с первого дня важна мобилизация пациента, дыхательные упражнения для предотвращения воспаления легких. Особое внимание уделяется показателям сахара в крови, чтобы своевременно распознать возможный сахарный диабет, вызываемый подобными операциями. Проводят постепенное восстановление питания, лечебную гимнастику, дыхательную терапию. При удалении большой части поджелудочной железы, начинают заместительную терапию вырабатываемых поджелудочной железой ферментов. Как правило, пациента выписывают на 10-14 день после операции.
Патогенез
Развитие кисты ПЖ происходит под воздействием провоцирующих факторов, в результате чего возникает в поджелудочной железе дискомплексация панкреатоцитов с развитием мелких диффузных некрозов ацинарных (секретирующих) клеток. Как следствие наблюдается нарушение секреции в просвет протоков и парапедез секреторных гранул в интерстиций. Разрушенные клетки способствуют интерстициальной/внутриклеточной активации трипсина, который активирует панкреатические гидролитические/протеолитические ферменты, которые в свою очередь способствуют аутоферментной агрессии и развитию очагов некроза, который проявляется региональнымм реологическими расстройствами и выраженным интерстициальным отёком.
Резорбция из интерстиция ферментов ПЖ способствует аутолитическогму повреждению кровеносных сосудов с последующим развитием тромбогеморрагического локального синдрома.
В основе формирования жидкостных скоплений лежат процессы лизиса очагов инфильтратов/некроза. Формирование жидкостных скоплений обеспечивается преимущественно за счет экссудативной реакции воспалённых тканей и в меньшей степени за счет панкреатического сока, поступающего из-за нарушения оттока сока по главному панкреатическому протоку. В результате выраженного нарушения проницаемости капилляров практически в течение 1–2 часа после разрушения ацинусов в тканях появляется множество тучных клеток/лейкоцитов, активно выделяющих биологически активные вещества, что приводит к формированию демаркационного вала вокруг очага некроза, состоящего из лейкоцитов, фибрина, гистеоцитов, лимфоплазмоклеточных компонентов и ядерного детрита.
Активизация фибробластов способствует интенсивному образованию элементов соединительнотканных структур/коллагена, которые и служат основой формирования барьера, который в последующем являться базой капсулы постнекротической кисты.
Стоимость хирургического лечения кист поджелудочной железы в Германии
Прежде чем удалить опухоль, важно пройти обследование и получить клинические рекомендации от лечащего врача в клинике «Нордвест». Точное следование предписанной схеме лечения помогает избежать возможных осложнений после удаления кисты поджелудочной железы и быстро вернуться к привычному ритму жизни. Лечение в Германии поможет вам справиться с заболеванием и максимально устранить последствия его проявления в организме. С пациентами больницы работают лучшие врачи, неоднократно подтвердившие свою высокую квалификацию на практике. Цены на удаление кист поджелудочной железы можно уточнить при первом обращении. Стоимость всего лечения включает консультацию с доктором, диагностические исследования, оперативное вмешательство, а также реабилитационный период после.
Острый панкреатит.
Острый панкреатит – это острое воспаление поджелудочной железы.
Острый панкреатит обычно появляется на фоне злоупотребления человеком спиртными напитками и перенесенными алкогольными отравлениями.
К острому панкреатиту также могут привести:
- неправильное или некачественное питание (употребление жирной, острой пищи, частое переедание);
- мочекаменная болезнь – наличие камней в почках;
- наследственность;
- травмирование поджелудочной железы: перенесенные операции, травмы, механические повреждения;
- неконтролируемый прием медикаментов, антибиотиков;
- эндокринные заболеваний, гормональные нарушения.
- инфекции и вирусы.
Симптомы острого панкреатита в Нижнем Новгороде.
Главный симптом панкреатита – острейшая боль в подложечной зоне, подреберьях (правом и левом). Боль со временем начинает принимать опоясывающий характер, захватывать спину, нижние и боковые участки живота.
Выявление острого панкреатита в Нижнем Новгороде.
При подозрении на развитие панкреатита в организме, врач гастроэнтеролог назначает следующий комплекс обследований:
- общий анализ крови, который позволяет узнать о наличии воспалительного процесса;
- УЗИ брюшной полости, которое позволяет увидеть изменения во внутренних органах;
- общий анализ мочи для выявления амилазы в моче, наличие которой говорит о развитии панкреатита;
- ФГДС.
Присутствие панкреатического абсцесса
Ограниченное скопление гноя внутри или рядом с ПЖ традиционно описывалось как инфицированная псевдокиста, состояние требующее оперативного вскрытия и дренирования. Недавно эндоскопическое дренирование было использовано у группы пациентов с высокой степенью операционного риска в связи с наличием системных осложнений панкреатита [35]. Важными факторами являются адекватное дренирование, необходимость устранения обструкции оттоку и прилежное обучение и наблюдения пациента. Мы предпочитаем трансмуральный подход к дренированию абсцесса т.к. он позволяет в дальнейшем выполнить дренирование цистэнтеростомического канала, ввести назогастральный ирригационный катетер и множественные стенты для предупреждения сложностей связанных с недостаточной функцией катетера и остаточным содержимым.
Возможности дренирования
В прошлом, когда дренирование становилось необходимым в связи с осложнениями или некурабильными симптомами связанными с ПК хирургическое дренирование оставалось единственным способом лечения. В настоящее время имеются еще две возможности лечения которые достигли все возрастающей популярности: чрезкожное и эндоскопическое дренирование. Остающимся противоречием остается вопрос какой из этих методов должен быть предложен пациенту в качестве начального вида терапии. В настоящее время нет рандомизированных сравнительных исследований этих двух методов и врачи используют тот которым они лучше владеют. Недостатком чрезкожного дренирования является длительное нахождение катетера и возможное формирования наружного свища.
Внутреннее хирургическое дренирование.
Большинство хирургов при возможности используют технику внутреннего дренирования, методика которой зависит от локализации псевдокисты:
- Цисто-гастро или дуоденостомия при спаивании кисты с желудком или ДПК.
- Цистоеюностомия может применяться при других анатомических вариантах.
- ПК хвоста поджелудочной железы могут быть удалены при его резекции, в этих условиях часто необходима папилосфинктеротомия.
Сообщаемый уровень осложнений внутреннего дренирования приблизительно 15 % со смертностью менее 5 %. Уровень послеоперационного рецидива около 10 % [22-26]. При наличии обструкции главного панкреатического протока ниже уровня анастомоза некоторые хирурги предпочитают резекцию ПК, а не внутреннее дренирование в попытке минимизировать уровень рецидивов.
Наружное хирургическое дренирование
может быть необходимым при невозможности создания внутреннего анастомоза. Наружные панкреатические свищи являются частым исходом подобного подхода [27].
Чрезкожное дренирование катетером.
Чрезкожное дренирование катетером является таким же эффективным как хирургическое дренирование в дренировании и закрытии как стерильных так и инфицированных кист [28-30]. Необходимо поддерживать проходимость катетера путем аккуратной ирригации. Катетер оставляется до тех пор пока уровень отделяемого снизится до 5-10 мл. в день. В одном исследовании включающим 52 пациента средний срок дренирования составил 42 дня [28]. Если такое снижение уровня отделяемого не происходит то назначение октреотида (50- 200 мг. подкожно, каждые 8 часов) может быть полезным. Контрольное КТ должно быть выполнено при уменьшении количества отделяемого для уверенности, что катетер не сместился из полости ПК. Основным осложнением этой процедуры является проникновение по катетеру инфекции, которое в одном исследовании происходила у половину пациентов [28]. Неизвестно должна ли обструкция главного панкреатического протока удерживать от выполнения чрезкожного дренирования.
Эндоскопический подход.
Множественные сообщения подтверждают высокий уровень эффективности эндоскопической цисто-гастро (ЭЦГ) и цисто-дуоденностомии (ЭЦД). ЭЦД является процедурой выбора из-за ее более высокой безопасности, более легкого достижения перпендикулярного подхода к кисте во время дренирования и большей заинтересованности ДПК чем желудка в большинстве случаев ПК. Уровень разрешения ПК при эндоскопическом лечении варьирует от 65 до 89 %. Основными осложнениями эндоскопического дренирования являются кровотечение (которое по свое тяжести требует хирургического лечения в до 5 % случаев), ретроперитониальная перфорация, инфекция и не достижение разрешения ПК. Смертность связанная с этой процедурой практически отсутствует с уровнем рецидива в 6-18 %. Количество случаев перфорации или кровотечение может быть минимизировано путем обнаружения ПК до эндоскопической пункции. Мы предпочитаем обнаружение ПК путем эндоскопической пункции, хотя увеличение популярности эндоскопического УЗИ может сделать это методику приемлемой альтернативой.
Рекомендуемый подход
В настоящее время мы рекомендуем активную тактику у пациентов с ПК возникшими как осложнение хронического или острого панкреатита с наличием симптомов и длительности существования ПК минимум 4 недели. Мы выполняем РХПГ когда считаем, что пациент является кандидатом для попытки эндоскопического дренирования. Во время эндоскопии необходимо исключить портальную гипертензию и обструктивные нарушения эвакуации из желудка. РХПГ выполняется для обнаружения признаков сдавления билиарного древа, в особенности ели повышены печеночные показатели. Панкреатография необходима у всех пациентов для выявления лежащей в основе обструкции панкреатического протока. Неожидаемые стриктуры и конкременты панкреатического протока часто выявляются, может даже встретиться стриктура вызванная злокачественной опухолью. Т.к. эндоскопическое дренирование может быть выполнено как путем трансмуральной пункции так и чрезпапилярной установки стента, панкреатограмма очень важна для выбора между этими двумя возможностями. Эндоскопическое УЗИ может быть полезным в дифференциальной диагностике с кистозными поражениями ПЖ и дренировании ПК, хотя в рутинном порядке не используется. У пациентов с большими, упорными или увеличивающимися ПК часто обнаруживаются тяжелые повреждения панкреатического протока, что определяет необходимость и вид используемого лечения [10]. По нашему опыту обструкции панкреатического протока и его полные стриктуры часты в этой группе пациентов и они не разрешаются после разрешения псевдокист. В отличии от этого подтекание из периферических ветвей закрываются после эндоскопического лечения приводящего к разрешению кисты.
Рекомендуем:
- Роль внутрипросветных эндоскопических вмешательств в комплексном лечении хронического панкреатита и его осложнений
- Диагностическая РХПГ. Техника выполнения
- Диагностика и лечение псевдокист поджелудочной железы
- Эндоскопияприпервичномсклерозирующемхолангите: клиническиерекомендацииЕвропейскогообщества
- Рекомендации хирургического лечение хронического панкреатита 2016
- Стентирование и ЭРХПГ под УЗИ
- Проект национальных клинических рекомендаций «Механическая желтуха»
Статьи по теме — смотрите подборку статей в нижней части страницы
Роль эндоскопического УЗИ
Популярность эндоскопического УЗИ в диагностике псевдокист ПЖ в настоящее время растет в связи с тем, что эта методика позволяет распознать сложную структуру стенок и содержимого ПК. В комбинации с аспирационной биопсией она может помочь в дифференциальной диагностики ПК и кистозной неоплазмы [31]. Наличие хорошо дифференцируемых септ, эхогенного муцина и объемных образований указывает на кистозную неоплазму требующую резекции а не дренирования. Как было сказано выше эндоскопическое УЗИ может помогать в выборе места пункции псевдокисты — исключить наличие крупных вен или артерий в области дренирования [32]. Таким образом существует теоретически эта методика может иметь преимущество за счет снижения риска кровотечения и перфорации, хотя это не было продемонстрировано при проведении контролируемых исследований.