Внезапная смерь
Определение
. Внезапная сердечная смерть (ВСС) определяется как: «естественная смерть, наступившая вследствие сердечных причин, проявляющаяся внезапной потерей сознания в течение одного часа с момента появления симптомов; может быть известно о наличии заболевания сердца, однако время и механизм наступления смерти непредсказуемы». Ключевые концепции, являющиеся ведущими в определении внезапной смерти, это нетравматическая причина и то, что наступление смерти мгновенно и непредсказуемо. При рассмотрении проблемы внезапной смерти в пределах заболеваний сердца, в термин введено слово «сердечная».
Причины
Эпидемиология
. Одной из ведущих причин смертности взрослого населения развитых стран является ВСС вследствие коронарной болезни сердца. У пациентов с внезапным сердечно-сосудистым коллапсом наиболее часто на ЭКГ определяется ритм фибрилляции желудочков ( в 75-80% случаев ), тогда как брадиаритмии являются причиной ВСС у минимального числа больных. В 5-10% случаев внезапной сердечной смерти у пациентов не выявляется коронарной болезни сердца либо застойной сердечной недостаточности. Согласно данным статистики, ежегодно получаемым в западных странах, частота ВСС варьирует от 0. 6 – 1.28 на 1000 человек в год. В эти исследования включаются только данные о погибших или реанимированных службой скорой помощи; таким образом, официальные данные ниже, чем реальное количество случаев ВСС в общей популяции.
Профилактика внезапной сердечной смерти: общая популяция и группа высокого риска. Среди взрослого населения частота ВСС составляет 1 на 1000 в год. Проведение профилактических мероприятий для снижения риска внезапной сердечной смерти в данной группе населения представляется нецелесообразным и нерентабельным, так как затраты включают остальных 999 на 1000 человек в год, у которых отсутствует риск ВСС. Таким образом, в общей популяции рекомендуются общие принципы здорового образа жизни.
Подгруппы, в которых ежегодный риск внезапной сердечной смерти прогрессивно возрастает, являются относительно немногочисленными. Из этого следует, что пропаганда здорового образа жизни среди населения закономерно приведет к снижению количества больных с коронарной болезнью сердца, что в свою очередь позволит снизить количество случаев внезапной сердечной смерти.
Что такое имплантируемый дефибриллятор?
Имплантируемый дефибриллятор это устройстройство, похожее на кардиостимулятор (искусственный водитель ритма), применяемое с начала 90-ых годов. Оно имеет небольшие габариты — не больше пейджера — и вживляется под кожу верхней части грудной клетки. В устройстве находятся батарея и микрокомпьютер, необходимые для коррекции Вашего ритма. Имплантируемый дефибриллятор связан с сердцем тонкими проводками с изоляцией — электродами. Если устройство выявляет нарушение Вашего сердечного ритма, оно посылает электрические сигналы, чтобы его восстановить. Большинство имплантируемых дефибрилляторов работают 5-7 лет, после чего необходимо провести замену.
Факторы риска внезапной сердечной смерти в популяции
| Немодифицируемые факторы риска | Модифицируемые факторы риска |
| Возраст | Курение |
| Мужской пол | Гипертензия |
| Семейный анамнез коронарной болезни сердца | Повышенный уровень ЛПНП |
| Генетические факторы | Сахарный диабет |
| Ожирение |
Профилактика ВСС: рекомендации европейского общества кардиологов
Группа специалистов по внезапной сердечной смерти европейского общества кардиологов представляет рекомендации, направленные на снижение частоты ВСС. Рекомендации представлены в таблицах и распределены следующим образом:
Класс I:
достоверные доказательства и/или единство мнений экспертов в том, что данная процедура или вид лечения целесообразны, полезны и эффективны.
Класс II:
противоречивые доказательства и/или расхождение во мнениях экспертов о пользе/эффективности процедуры или лечения.
Класс IIa:
преобладают доказательства и/или мнения экспертов за пользу/эффективность.
Класс IIb
: польза/эффективность недостаточно хорошо подтверждена доказательствами и/или мнениями экспертов.
В настоящих рекомендациях термины «первичная» и «вторичная» профилактика используется в основном в контексте желудочковой аритмии. Терапия, назначаемая с целью предотвращения развития устойчивой желудочковой аритмии пациентам без эпизодов жизнеугрожающих желудочковых аритмий в анамнезе, однако отнесенным к группе высокого риска их развития, относится к «первичной» профилактике. Терапия, рекомендуемая пациентам с остановкой сердца и синкопами/гипотензией на фоне пароксизма желудочковой тахикардии, является «вторичной» профилактикой.
Основные виды прекращения сердечной деятельности и механизмы их развития
Причины остановки сердца по механизму развития скрыты в резком нарушении его функциональных способностей, особенно возбудимости, автоматизма и проводимости. От них зависят виды остановки сердца. Сердечная деятельность может прекратиться двумя путями:
- асистолией (у 5% пациентов);
- фибрилляцией (в 90% случаев).
Асистолия представляет собой полное прекращение сокращения желудочков в фазе диастолы (при расслаблении), редко — в систоле. «Приказ» об остановке может поступить в сердце с других органов рефлекторно, например, при операциях на желчном пузыре, желудке, кишечнике.
При рефлекторной асистолии миокард не поврежден, имеет достаточно хороший тонус
В данном случае доказана роль блуждающего и тройничного нервов.
Другой вариант — асистолия на фоне:
- общей кислородной недостаточности (гипоксии);
- повышенного содержания углекислоты в крови;
- смещения кислотно-щелочного равновесия в сторону ацидоза;
- измененного баланса электролитов (рост внеклеточного калия, снижение кальция).
Эти процессы, вместе взятые, негативно воздействуют на свойства миокарда. Становится невозможным процесс деполяризации, являющийся основой сократимости миокарда, даже если не нарушена проводимость. Клетки миокарда теряют активный миозин, необходимый для получения энергии в виде АТФ.
При асистолии в фазе систолы наблюдается гиперкальциемия.
Фибрилляция сердца — это нарушенная связь между кардиомиоцитами в координированных действиях для обеспечения общего сокращения миокарда. Взамен синхронной работы, вызывающей систолическое сокращение и диастолу, появляется множество разрозненных участков, которые сокращаются сами по себе.
Частота сокращений доходит до 600 в минуту и выше
При этом страдает выброс крови из желудочков.
Затраты энергии значительно превышают нормальные, а эффективного сокращения не происходит.
Если фибрилляция захватывает только предсердия, то отдельные импульсы доходят до желудочков и кровообращение поддерживается на достаточном уровне. Приступы кратковременной фибрилляции способны закончиться самостоятельно. Но подобное напряжение желудочков не может длительно обеспечивать гемодинамику, истощаются энергетические запасы и возникает остановка сердца.
I. Инфаркт миокарда и сердечная недостаточность
А. Стратификация риска
Для определения риска ВСС в группе пациентов с инфарктом миокарда в анамнезе используются как неинвазивные, так и инвазивные тесты.
Стратификация риска у пациентов, перенесших ИМ
с развитием / без развития СН
| Класс | I | IIa | IIb |
| Демографическая изменчивость ФВ ЛЖ ВР или чувствительность БР Объем ЛЖ | ЭС неустойчивая ЖТ ЧСС покоя | Поздние потенциалы ЭФИ Динамичность з. Т Проходимость инфаркт– зависимой артерии |
ФВ ЛЖ – фракция выброса левого желудочка; ВР – вариабельность ритма
БР – барорефлекс; ЭС – экстрасистолия; ЖТ – желудочковая тахикардия
ЧСС – частота сердечных сокращений; з. Т – зубец Т
Б. Первичная и вторичная профилактика ВСС у пациентов с ИМ в анамнезе
Наиболее часто внезапная сердечная смерть встречается среди пациентов, перенесших инфаркт миокарда. В этой группе к первичной профилактике относится медикаментозное лечение бета-блокаторами, аспирином, ингибиторами АПФ и холестеринснижающими препаратами. У больных с документированной устойчивой ЖТ или ЖФ, альтернативой является имплантируемый кардиовертер-дефибриллятор (КД) или амиодарон, а в отдельных случаях абляция или хирургическое лечение. У пациентов с ИМ в анамнезе, снижением ФВ ЛЖ меньше или равно 40% (меньше или равно 5%) и клинически симптомными пароксизмами неустойчивой ЖТ, либо индуцируемой устойчивой или неустойчивой ЖТ при программированной электростимуляции (ЭФИ), рекомендованным методом лечения является имплантация КД. Для вторичной профилактики ВСС применение КД рекомендовано реанимированным после ФЖ и пациентам с гемодинамически симптомными пароксизмами ЖТ.
Первичная профилактика у пациентов, перенесших ИМ с развитием / без развития СН
| Класс | I | IIa | IIb |
| ИМ в анамнезе | Бета-блока-торы Ингибиторы АПФ Холестерин-снижающие препараты Аспирин | Полинена-сыщенные жирные кислоты Амиодарон | |
| ИМ + дисфункция ЛЖ | Бета-блока-торы Ингибиторы АПФ Блокаторы рецепторов альдостерона | Амиодарон | |
| Гемодинамически бессимптомные ЖТ | Амиодарон Бета-блока-торы | КД Абляция Хирургическое лечение | |
| ФВ ЛЖ меньше или равно 40% + пароксизмы неустойчивой ЖТ + индуцируемая устойчивая ЖТ при ЭФИ | КД |
Вторичная профилактика у пациентов, перенесших ИМ с развитием / без развития СН
| Класс | I | IIa | IIb |
| ФЖ | КД | ||
| Гемодинамически симптомная устойчивая ЖТ | КД | Амиодарон Бета-блокаторы |
II. Кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП)
ГКМП является относительно часто встречаемой патологией сердца (частота среди взрослых около 1:500), при которой внезапная сердечная смерть является наиболее вероятным исходом в любом возрасте, но наиболее часто у молодых, нередко асимптомных пациентов. Имплантация КД для профилактики внезапной сердечной смерти серьезно обоснована у больных, выживших после остановки сердца (вторичная профилактика). Профилактическое использование КД также возможно у пациентов с двумя и более факторами риска.
Гипертрофическая кардиомиопатия
| Класс | I | IIa | IIb |
| Стратификация риска | Устойчивая ЖТ ФЖ | Семейный анамнез ВСС Синкопы Гипертрофия ЛЖ (ТМЖП больше см) Неустойчивая ЖТ Гипотония во время выполнения нагрузочного стресс-теста | Высокий риск мутаций |
| Первичная профилактика | КД | Амиодарон | |
| Вторичная профилактика | КД |
ТМЖП – толщина межжелудочковой перегородки
Аритмогенная дисплазия правого желудочка (АДПЖ)
АДПЖ является одной из основных причин внезапной сердечной смерти в «до-коронарной» возростной группе. Не смотря на то, что предрасполагающие факторы ВСС еще не достаточно изучены в больших проспективных исследованиях, внезапная сердечная смерть случается более часто у пациентов с выраженными изменениями правого желудочка, а также с вовлечением в процесс ЛЖ. У реанимированных после ВСС (вторичная профилактика), у пациентов с устойчивой ЖТ и неэффективной терапией антиаритмиками и у больных из группы высокого риска с документированными пароксизмами ЖТ, наиболее адекватным лечением является имплантация КД.
Аритмогенная дисплазия правого желудочка
| Класс | I | IIa | IIb |
| Стратификация риска | Устойчивая ЖТ/ФЖ Дилатация ПЖ Дисфункция ПЖ Индуцируемая ЖТ/ФЖ при ЭФИ | Семейный анамнез ВСС Поздние потенциалы + дисфункция ЛЖ ЖТ Индуцируемая ЖТ/ФЖ при ЭФИ | |
| Первичная профилактика | КД | Антиаритмические препараты | |
| Вторичная профилактика | КД |
ПЖ – правый желудочек; ЭФИ – электрофизиологическое исследование
Дилатационная кардиомиопатия (ДКМП)
ВСС является одной из наиболее частых механизмов смерти при ДКМП, особенно на ранних стадиях заболевания. Доказано, что фракция выброса (ФВ) является наиболее точным предиктором исхода как в отношении внезапной сердечной смерти, так и смерти при прогрессирующей СН. Частота синкопальных эпизодов также считается одним из достоверных факторов риска внезапной сердечной смерти.
Общая терапевтическая стратегия, направленная на снижение риска ВСС у пациентов с ДКМП, включает использование ингибиторов АПФ, бета-блокаторов и антагонистов рецепторов альдостерона, тогда как амиодарон и имплантация КД используются в индивидуальных случаях. В нескольких исследованиях, изучавших роль антиаритмических препаратов у больных с ДКМП, получены данные (не доказанные статистически) что медикаментозное лечение, рекомендуемое больным, перенесшим ИМ с развитием СН, столь же эффективно у больных ДКМП. Использование КД для вторичной профилактики считается допустимым, имплантация КД также рекомендуется пациентам из группы высокого риска с целью первичной профилактики внезапной сердечной смерти.
Дилатационная кардиомиопатия
Класс
| I | IIa | IIb | |
| Стратифика-ция риска | Устойчивая ЖТ ФЖ | Синкопы | Снижение ФВ Неустойчивая ЖТ |
| Первичная профилактика | Ингибиторы АПФ Бета-блокаторы | КД Блокаторы рецепторов альдостерона | Амиодарон |
| Вторичная профилактика | КД Ингибиторы АПФ Бета-блокаторы | Блокаторы рецепторов альдостерона | Амиодарон |
Что происходит во время процедуры имплантации?
Обычно процедура имплантации выполняется быстро, безопасно и, как правило, под местной анестезией. При этом не требуется операции на открытом сердце, и большинство пациентов возвращаются домой в течение суток. Следующий раздел представляет собой общее описание того, что происходит во время процедуры имплантации. Ваш случай может отличаться, все детали Вы можете обсудить с Вашим врачом.
Во время имплантации.
Обычно перед началом процедуры пациенты получают успокаивающие препараты и не чувствуют боли. Ваш врач выполнит небольшой разрез в верхнем отделе грудной клетки и через вену проведёт в Ваше сердце электроды. Затем врач подключит электроды к имплантируемому дефибриллятору и запрограммирует устройство. Далее имплантируемый дефибриллятор будет помещен под кожу и разрез будет зашит. Врач проверит, правильно ли работает имплантируемый дефибриллятор.
После процедуры.
После имплантации устройства пациент обычно проводят ночь в палате, а утром может вернуться домой. Под кожей в месте расположения устройства Вы сможете ощущать небольшой бугорок, это место может быть чувствительным. Обычно рекомендуется ограничить движения рукой на стороне имплантации на 2-6 недель. Более подробные инструкции по уходу Вы сможете получить от Вашего врача. Всё же Вы можете рассчитывать на скорое возвращение к прежней активности после операции. Если у Вас возникнут вопросы, пожалуйста, обратитесь к Вашему врачу или медсестре.
Начало жизни с имплантируемым дефибриллятором: первые шесть недель.
Пришло время начать вновь полноценную жизнь. Мы надеемся, что она будет наполнена надеждой и уверенностью. Конечно же, пока не наступит излечение, вы можете испытывать некоторый дискомфорт. Также, чтобы не вызвать смещение электродов, возможно, придётся немного ограничить движения левой рукой. Обычно эти ограничения рекомендуются в течение 2-6 недель. Ваш врач расскажет Вам подробнее, каких движений и нагрузок следует избежать. Если у Вас появятся вопросы о том, что можно или нельзя делать до выздоровления, не стесняйтесь спросить Вашего врача или медсестру. Вашей семье и друзьям будет интересно узнать о Вашем имплантируемом дефибрилляторе. Возможно, Вы захотите показать место имплантации и рассказать об операции. Расскажите всем, как Вы рады чувствовать выздоровление после болезни. Самое время рассказать друзьям и близким о том, чем Вы вскоре планируете заняться. Выберите одно из Ваших любимых занятий и постройте планы, подумайте о том, как займётесь этим снова. Вера в себя и занятие приятными, доставляющими удовольствие делами вносит большой вклад в процесс выздоровления.
Жизнь с успехом: Достижение необходимой Вам уверенности.
Новое устройство для Вашего сердца поможет Вам чувствовать себя спокойно и уверенно. Оно всегда начеку, постоянно заботясь о Вашем сердце 24 часа в сутки. Если Ваш имплантируемый дефибриллятор выявляет расстройство ритма, он посылает восстанавливающий его электрический импульс. Вы можете представить, что это бригада скорой помощи, которая всегда рядом. И очень скоро Вы ощутите вклад этих положительных эффектов в повседневную жизнь. Помните о том, что вам всё равно необходимо продолжать принимать лекарства и периодически проверять работу устройства у Вашего кардиолога и электрофизиолога (специалиста по сердечному ритму). В любом случае, Ваша жизнь в Ваших руках, так что наслаждайтесь ей. Продолжайте строить планы. Расскажите всем, как хорошо себя чувствуете, чего благодаря этому добились, чем собираетесь заниматься. Для высокого качества жизни определите, чем Вам нравится заниматься, и возвращайтесь к активному образу жизни. Всегда помните, что если у Вас появятся вопросы о каких-либо особых занятиях, например, вождении автомобиля или возвращении на работу, то необходимо проконсультироваться с Вашим врачом.
Что происходит после разряда: подготовьте план.
Если Ваш имплантируемый дефибриллятор обнаруживает нарушение ритма Вашего сердца, он автоматически выполнит терапию — нанесет высокоэнергетический разряд. Пациенты, перенесшие такую терапию, описывают этот разряд как внезапное чувство дискомфорта, иногда даже болезненное, однако быстро проходящее. Также это означает, что имплантируемый дефибриллятор выполнил свою работу и, возможно, спас Вашу жизнь. Ваш врач даст вам особые указания о том, что делать после разряда. Разработайте вместе с ними подходящий Вам план действий. Этот план может включать то, что Вам сразу будет необходимо сделать, и те из Ваших любимых дел, которыми вы сможете продолжить заниматься после разряда. Храните план в удобном месте, чтобы Вы смогли к нему обратиться. Также обязательно расскажите об этом плане Вашим близким и тем, кто о Вас заботится, чтобы они могли понять, как Вам помочь. Важно понимать, что то, чем Вы занимались во время разряда, не вызывало его. Как правило, вы сможете продолжать наслаждаться любимыми занятиями. Обсудите с врачом, когда Вы сможете вернуться к вашим занятиям и необходимо ли вносить какие-нибудь изменения. Несмотря на то, что разряд может временно вызвать у Вас беспокойство, важно вернуться к повседневным занятиям и сосредоточиться на любимых делах.
Вы сами создаёте свою жизнь.
Жизнь состоит из мгновений, поэтому, чем больше удовольствия мы от них получаем, тем более плодотворной наша жизнь становится. Имплантируемый дефибриллятор может помочь Вам получать от жизни больше удовольствия, чтобы вы могли с уверенностью смотреть в будущее, которое так много для Вас значит. Это могут быть простые, «земные» радости, например прогулки в парке, работа в саду или общение с Вашими близкими. Важно то, что эти мгновения часто делают жизнь богаче, так что спешите ими насладиться.
III. Генетическая патология ионных каналов
Удлинение интервала QT
Синдром «удлиненного QT» ассоциируется с высоким риском внезапной сердечной смерти. Стратификация риска в основном базируется на наличии синкопальных эпизодов, Torsades de Pointe (ЖТ «пируэт»)и остановки сердца в анамнезе. Первичная профилактика ВСС в целом основана на лечении бета-блокаторами. Имплантация КД рекомендована для вторичной профилактики, а также у больных с ЖТ/ФЖ на фоне адекватного лечения бета-блокаторами в анамнезе.
Удлинение интервала QT
| Класс | I | IIa | IIb |
| Стратифика-ция риска | ЖТ «пируэт»/ ФЖ/остановка сердца Синкопы Синдром Жервелла– Ланге-Нильсена Удлинение интервала QT | QT больше 600 мс Развитие ЖТ/ФЖ в детском возрасте Удлинение QT + AV-блокада Макроскопи-чески динамич-ные зубцы Т Женский пол Послеродовый период | Семейный анамнез ВСС Повышение дисперсии интервала QT |
| Первичная профилактика | Избегать использо-вания препаратов, удлиняющих интервал QT Бета-блокаторы Избегать интенсивных физических нагрузок | Симпатическая денервация ЛЖ ЭКС | |
| Вторичная профилактика | КД + бета-блокаторы + избегать использо-вания препаратов, удлиняющих интервал QT Избегать интенсивных физических нагрузок |
ЭКС – электрокардиостимулятор
Синдром Бругада
Диагностика синдрома Бругада (СБ) основана на наличии спонтанной или индуцируемой элевации сегмента ST в отведениях V1-V с/без блокадой правой ножки пучка Гиса (БПНПГ). Стратификация риска до настоящего времени недостаточно определена, обсуждается роль ЭФИ для выявления пациентов с факторами высокого риска. У выживших после остановки сердца рекомендуется имплантация КД. Профилактическое использование КД в группе высокого риска настоятельно рекомендуется, однако данный подход ограничен отсутствием четко определенных критериев риска.
Синдром Бругада
| Класс | I | IIa | IIb |
| Стратификация риска | Устойчивая ЖТ ФЖ | Синкопы Семейный анамнез ВСС | Индуцируемая ЖТ/ФЖ при ЭФИ |
| Первичная профилактика | КД у пациентов с синкопами/ЖТ | КД у асимптомных пациентов с ЖТ инду-цируемыми при ЭФИ | |
| Вторичная профилактика | КД |
Катехоламинэргическая полиморфная желудочковая тахикардия
До настоящего времени отсутствует точное определение катехоламинергической полиморфной желудочковой тахикардии (КПЖТ), так как проведение крупномасштабных исследований не возможно. Это заболевание ассоциируется с высоким риском внезапной сердечной смерти в молодом возрасте, но критерии для стратификации отсутствуют. Профилактика внезапной сердечной смерти основана на применении бета-блокаторов; КД рекомендованы для вторичной профилактики, так как значимость КД для первичной профилактики не определена.
Катехоламинэргическая полиморфная желудочковая тахикардия
| Класс | I | IIa | IIb |
| Стратифика-ция риска | ФЖ | Семейный анамнез ВСС Неустойчивая ЖТ/синкопы в детском возрасте | Синкопы |
| Первичная профилактика | Бета-блокаторы | КД | |
| Вторичная профилактика | КД + бетаблокаторы | Бета-блокаторы |
Внезапная остановка сердца ассоциированная с ранней реполяризацией
МЕТОДЫ. Мы рассмотрели данные 206 пациентов в 22 центрах, которые были реанимированы после остановки сердца из-за идиопатической фибрилляции желудочков и оценили распространенность электрокардиографической ранней реполяризации. Последний определялся как повышение QRS-ST-соединения, по меньшей мере, на 0,1 мВ от исходного уровня в нижнем или боковом отведении, проявляющееся как блуждание или насечка QRS. Контрольная группа включала 412 пациентов без сердечных заболеваний, которые соответствовали возрасту, полу, расе и уровню физической активности. Последующие данные, которые включали результаты мониторинга с имплантируемым дефибриллятором, были получены для всех пациентов.
РЕЗУЛЬТАТЫ. Ранняя реполяризация была более частой у лиц с идиопатической фибрилляцией желудочков, чем у контрольных субъектов (31% против 5%, р <0,001). Среди субъектов исследования те, у кого была ранняя реполяризация, чаще были мужчинами и имели в анамнезе синкопальное состояние (обморок) или внезапную остановку сердца во время сна, чем пациенты без ранней реполяризации. У восьми испытуемых происхождение эктопии, которая инициировала желудочковые аритмии, были расположены в участках, соответствующих локализации аномалий реполяризации. Во время среднего (± SD) наблюдения в 61 ± 50 месяцев мониторинг дефибриллятора показал более высокую частоту рецидивов фибрилляции желудочков у пациентов с аномалией реполяризации, чем у пациентов без такой патологии (отношение рисков, 2,1, 95% доверительный интервал , От 1,2 до 3,5, P = 0,008).
ВЫВОДЫ. Среди пациентов у которых в анамнезе есть идиопатическая фибрилляция желудочков наблюдается повышенная распространенность ранней реполяризации.
Внезапная остановка сердца остается. Одна из основных проблем общественного здравоохранения, которая ежегодно составляет около 350 000 смертей в Соединенных Штатах. Несмотря на достижения в области неотложной медицинской помощи, только 3-10% пациентов, у которых случилась остановка сердца вне больницы, успешно реанимируются. Большинство таких внезапных остановок сердца вызвано желудочковыми тахиаритмиями, которые встречаются у лиц без структурной болезни сердца в 6-14% случаев. Некоторые из последних случаев связаны с хорошо распознанными электрокардиографическими аномалиями, которые влияют на реполяризацию желудочков (например, длинные или короткие интервалы QT или синдром Бругада), тогда как в других случаях, когда нет признаков во время синусового ритма, описываются как идиопатическая фибрилляция желудочков. Ранняя реполяризация является обычной электрокардиографической находкой, которая затрагивает от 1 до 5% людей. Хотя это состояние обычно считается доброкачественным, его потенциальная аритмогенность была предположена экспериментальными исследованиями. Однако подтверждающих клинических доказательств нет. Мы провели исследование случай-контроль, включавшее 206 пациентов с идиопатической фибрилляцией желудочков, чтобы оценить распространенность ранней реполяризации и оценить ее потенциальную связь с любыми наблюдаемыми аритмиями и последующим исходом, контролируемым имплантируемыми дефибрилляторами.
Методика.
ИЗУЧЕНИЕ НАСЕЛЕНИЯ. Случаи заболевания людей в возрасте до 60 лет регистрировались в 22 территориальных центрах занимающихся аритмиями. Все пациенты с диагнозом идиопатической фибрилляции желудочков в этой возрастной группе были отобраны из баз данных пациентов, которые получили имплантируемый дефибриллятор; Все пациенты в возрасте 60 лет и старше были исключены, чтобы минимизировать риск субклинической структурной болезни сердца. Устное информированное согласие было получено от всех зачисленных пациентов.
Мы оценивали базовые электрокардиограммы на наличие ранней реполяризации, которая определялась как повышение QRS-ST-соединения (точка J) по меньшей мере в двух отведениях во время имплантации дефибриллятора. Амплитуда высоты точки J должна была быть по крайней мере на 1 мм (0,1 мВ) выше базового уровня, либо как смазывание QRS (плавный переход от сегмента QRS к сегменту ST), либо надреза (положительное J-отклонение вписанное на S-волне) в нижнем отведении (II, III и aVF), боковом отведении (I, aVL и V4 до V6) или обоих. Передние грудные отведения (от V1 до V3) были исключены из анализа, чтобы избежать включения пациентов с дисплазией правого желудочка или синдромом Бругада.
На основании опубликованных рекомендаций пациенты были классифицированы как имеющие идиопатическую фибрилляцию желудочков, если у них не было структурной болезни сердца, выявленных нормальными эхокардиографическими бивентрикулярными размерами и функцией, не было выявлено ишемической болезни коронарных артерий при коронарной ангиографии или нагрузочных тестах, а также не было выявлено никаких аномалий реполяризации. Пациенты были исключены, если они имели интервал QT с поправкой на частоту сердечных сокращений (QTc) менее 340 мс (короткий интервал QT) или более 440 мс (длительный интервал QT) в начале исследования и перед аритмией. Также исключались пациенты с синдромом Бругада, определяемые по блокаде правой ветви п. Гиса и повышение сегмента ST (> 0,2 мВ) в грудных отведениях V1-V3 без вмешательства или после инфузии блокатора натриевых каналов (антиаритмиков). Кроме того, были исключены пациенты с катехоламинергическими аритмиями, определяемые как аритмии во время инфузии катехоламинов или нагрузочного тестирования.
Мы оценили распространенность и амплитуду ранней реполяризации в контрольной группе из 412 испытуемых. Эта группа была составлена сотрудниками здравоохранения с нормальными эхокардиографическими бивентрикулярными размерами и функцией и без синкопальных состояний (обмороков) в анамнезе. Для согласования использовались следующие факторы (возраст, пол, раса и уровень физической активности).
Сбор данных.
Мы собрали следующие клинические данные: синкопальные состояния в анамнезе, внезапная остановка сердца, внезапная смерть в семейном анамнезе (у родственников) (в возрасте <60 лет), уровень физической активности (> 10 часов или ≤10 Часов активности в неделю), результаты усредненной по сигналам электрокардиографии (как стандартной амплификации, так и высокой амплификации) и результаты фармакологического тестирования и инвазивного электрофизиологического тестирования. Электрокардиографические показатели измерялись с использованием автоматизированного онлайн-программного обеспечения и проверялись вручную. Интервал QTc рассчитывали после коррекции сердечного ритма с помощью формулы Базетта.
ЭЛЕКТРОФИЗИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ. Мы проводили электрофизиологическое исследование с использованием многоэлектродных катетеров, вводимых чрескожно через бедренные сосуды. Запрограммированную желудочковую стимуляцию выполняли с использованием максимум двух или трех желудочковых экстрастимуляций из двух отдельных участков желудочков. Фибрилляция желудочков считалась индуцируемой, если она продолжалась более 30 секунд или требовала электрической кардиоверсии. Ни один пациент не имел индуцируемой мономорфной желудочковой тахикардии.
В случае субъектов с рецидивирующей фибрилляцией желудочков, несмотря на введение антиаритмических препаратов, выполнялась катетерная абляция, направленная на инициирующую желудочковая эктопию, как описано ранее. Такая эктопия была локализована путем картирования самой ранней электрической активности, либо Пуркинье, либо миокарда, относительно начала комплекса QRS. Абляция выполнялась с использованием радиочастотной энергии.
ТЕРАПИЯ И ПОСЛЕДУЮЩАЯ ДЕЯТЕЛЬНОСТЬ. Все пациенты с эпизодами получали имплантируемый дефибриллятор, который обеспечивал точную информацию о рецидиве фибрилляции желудочков. Пациенты наблюдались регулярно каждые 6-12 месяцев для клинического осмотра и проверки устройства или, по мере необходимости, в случае появления симптомов или разряжения батареек устройства. В субъектах с рецидивирующими аритмиями выбор антиаритмических препаратов производился лечащими врачами.
СТАТИСТИЧЕСКИЙ АНАЛИЗ. Непрерывные переменные указывались как среднее ± SD или медианы (с 25-м и 75-м процентилями), в зависимости от ситуации. Сравнение между этими двумя группами проводилось с t-критерием Стьюдента или непараметрическим критерием Уилкоксона, в зависимости от случая, и с t-критерием Стьюдента для парных данных. Категориальные переменные сравнивались с точным тестом Фишера. Распространенность ранней реполяризации сравнивалась между субъектами исследования и контрольной группой с использованием логистического регрессионного анализа (сообщалось как отношение шансов с 95% доверительными интервалами) и корректировалось на соответствие переменных. Число рецидивов фибрилляции желудочков сравнивалось с использованием теста Уилкокинсона, а частота рецидивов оценивалась с использованием актуарных кривых. Для оценки относительного риска, связанного с ранней реполяризацией, использовались коэффициенты опасности от моделей пропорционального риска Кокса. Все тесты были двухсторонними, а значение Р менее 0,05 считалось статистически значимым.
РЕЗУЛЬТАТЫ.
РАННЯЯ РЕПОЛЯРИЗАЦИЯ.
В группе пациентов с идиопатической фибрилляцией желудочков было 123 мужчины и 83 женщины со средним возрастом 36 ± 11 лет. Контрольная группа включала 412 человек, которые соответствовали возрасту (36 ± 12 лет), полу (270 мужчин и 142 женщины), расе (380 белых, 27 азиатов и 5 негров) и физической активности (44 субъекта занимались больше чем 10 часов активности в неделю).
Ранняя реполяризация произошла у 64 пациентов (31%) по сравнению с 21 контрольной группой (5%, Р <0,001) и была выше по величине у субъектов исследования, чем у контрольных испытуемых (точка J Высота 2,0 ± 0,9 мм против 1,2 ± 0,4 мм, P <0,001). После корректировки на возраст, пол, расу и уровень физической активности отношение шансов на наличие ранней реполяризации у субъектов исследования по сравнению с контрольными субъектами составило 10,9 (95% доверительный интервал [ДИ], 6,3-18,9).
Случаи с ранней реполяризацией чаще встречались у мужчин, имели в анамнезе необъяснимый обморок или внезапную остановку сердца во время сна и имели более короткий интервал QTc, чем у пациентов без ранней реполяризации.
На начальной стадии ранняя реполяризация присутствовала в передний отведениях у 28 субъектов, в боковых отведениях у 6 испытуемых, а также у нижних и базальных отведений у 30 пациентов. Эта картина считалась реполяризацией, а не поздней деполяризацией из-за ее более медленной записи, спонтанного колебания морфологического рисунка или амплитуды перед устойчивыми комплексами QRS и амплитуды, изменяющейся одновременно с сегментом ST. Отсутствие поздних потенциалов на электрокардиографии с высокой амплификацией дополнительно поддерживало реполяризационный паттерн. Эта картина происходила в изоляции или сопровождалась отрицательным увеличением T-зубца или дискретным подъемом сегмента ST (горизонтальная или отображающая вверх изогнутость). Электрокардиограммы, которые были получены за несколько недель до внезапной остановки сердца, были доступны для 22 субъектов и показали картину ранней реполяризации (как описано выше).
Электрокардиографию выполняли в течение аритмического периода (включая частоту желудочковой эктопии и эпизоды фибрилляции желудочков) у 18 субъектов все исследования показали последовательное увеличение амплитуды ранней реполяризации по сравнению с исходным уровнем. Амплитуда J-точки увеличилась с 2,6 ± 1 мм до 4,1 ± 2 мм (P <0,001). В большинстве случаев эктопия имела положительный QRS морфологический паттерн в отведениях V1 до V2, что указывало на возникновение из левого желудочка и короткий интервал взаимодействия, инициирующий фибрилляцию желудочков (в среднем, 326 ± 41 мс, диапазон от 260 до 400) .
Нагрузочные тесты или инфузия изопротеренола последовательно уменьшали или устраняли раннюю реполяризацию. Изопротеренол, введенный двум субъектам во время повторных эпизодов фибрилляции желудочков, устранил все аритмии, когда частота сердечных сокращений синусового узла была увеличена более чем на 120 ударов в минуту. Напротив, бета-блокаторы усиливали аномалии реполяризации. Их неэффективность приводила к попыткам катетерной абляции желудочковых преждевременных сокращений, которые приводили к фибрилляции желудочков у некоторых субъектов.
КОРРЕКТИРОВКА ЭКТОТИИ В РАННЕЙ РЕПОЛЛАРИЗАЦИИ. Картирование было выполнено у восьми пациентов. В двух случаях, картирование обоих желудочков не показало результатов во время деполяризации желудочков, которые совпадали с широкими терминальными QRS аномалиями, подтверждая, что последний был связан с реполяризацией. Всего 26 эктопических паттернов были картированы либо на миокард желудочка (16 паттернов), либо на ткань Пуркинье (10 паттернов). У шести пациентов с ранней реполяризацией, зарегистрированной только в нижних отделах, вся эктопия возникла из нижней стенки желудочка. У двух пациентов с широко распространенной ранней реполяризацией, которая регистрировалась как низкими, так и боковыми линиями, эктопия возникла из нескольких регионов. Катетерная аблация устраняла всю эктопию у пяти испытуемых и не устраняла состояние у трех испытуемых.
ВЗАИМОСВЯЗЬ СУБЬЕКТОВ. Таблица 2 суммирует результаты в течение среднего периода в 61 ± 50 месяцев (медиана, 51 месяц, межквартильный диапазон от 19 до 90) После начального события, при этом ни один субъект не потерял контроль. Аритмические рецидивы были более частыми у субъектов с ранней реполяризацией, чем у пациентов без такой реполяризации (41% против 23%). Коэффициент риска рецидива составил 2,1 (95% ДИ, от 1,2 до 3,5, Р = 0,008), даже после поправки на пол. У трех пациентов с наивысшим уровнем J-точки (> 5 мм) было более 50 эпизодов фибрилляции желудочков, приведшим к смерти в одном случае. Четырем больным с множественными эпизодами назначали хинидин, что уменьшало аномалии реполяризации и устраняло рецидивы аритмии.
ОБСУЖДЕНИЕ. Внезапная остановка сердца от аритмии может возникать у лиц, у которых нет структурного сердечного заболевания или очевидных электрокардиографических нарушений во время синусового ритма. В нашем исследовании такие субъекты исследования имели значительно более высокую распространенность ранней реполяризации, чем контрольные субъекты, у которых распространенность была сходной с таковой среди здоровых субъектов в ранее сообщавшихся исследованиях. Почти у трети пациентов были доступны электрокардиограммы, полученные до остановки сердца, и они показали раннюю реполяризацию, которая показала, что эта аномалия не может быть результатом травмы после внезапной остановки сердца, реанимации или препаратов, используемых для реанимации.
Маловероятно, что эта аномалия более распространена среди выживших пациентов с сердечными заболеваниями, чем среди не выживших, поскольку единственным наиболее важным фактором, определяющим успешную реанимацию, является доступ к быстрой дефибрилляции. Эта электрокардиографическая картина также была связана с увеличением частоты рецидивов желудочковых аритмий во время мониторного наблюдения дефибриллятора.
Наши результаты показывают связь между ранней реполяризацией и внезапной остановкой сердца, вывод, который противоречит, казалось бы, доброкачественной природе этого распространенного явления. Во-первых, это открытие может быть связано с определением ранней реполяризации, поскольку мы специально включили аномалии в нижне-боковые отведения, в то время как широкое традиционное определение ранней реполяризации включало в себя различной амплитуды, конфигурации и протяженности электрокардиографических паттернов, чаще всего в правых грудных отведениях. Во-вторых, немногие из субъектов исследования в нашем исследовании относились к подгруппам, у которых высокая распространенность ранней реполяризации (например, у спортсменов и чернокожих), что предполагает, что кофакторы влияют на ассоциацию с внезапной остановкой сердца. В-третьих, благоприятный характер ранней реполяризации оспаривается экспериментальными данными, свидетельствующими о наличии формы трансмуральной электрической неоднородности , может быть резко усилен при определенных условиях (использование специфических лекарств и различных уровней автономного тонуса и электролитов), что приводит к злокачественным аритмиям . Потенциальная аритмогенность, таким образом, зависит от дефектной модуляции реполяризации, которая соответствует динамическим изменениям, временным образом связанным с аритмиями, которые мы наблюдали в нашем случае.
Взаимосвязь между этой электрокардиографической картиной и злокачественными аритмиями подтверждается усиленной реполяризацией до наступления аритмии у субъектов исследования и возникновения триггерных сокращений в области ранней реполяризации. Хинидин, который, как было показано, восстанавливает трансмуральную электрическую однородность и отменяет аритмическую активность в этом состоянии, уменьшает электрокардиографическую картину и устраняет повторяющиеся аритмии у четырех субъектов.
Наконец, хотя, насколько нам известно, ни одно многоцентровое исследование не изучало ассоциацию между ранней реполяризацией и внезапной остановкой сердца, отдельные сообщения (в основном из Юго-Восточной Азии) описали пациентов, у которых внезапная остановка сердца была связана с аномальными J-волнами. Аномалия реполяризации, которая регистрируется в передне-боковой области может быть маркером базовой электрической уязвимости, которая увеличивает риск смертельных аритмий в условиях, которые необходимо исследовать. Эти условия включают наличие генетических дефектов, связанных с каналами сердечных ионов, что подтверждается тем фактом, что у 10 из наших пациентов была внезапная остановка сердца в семейном анамнезе.
Эти результаты потенциально важны для оценки пациентов с синкопальными состояниями (обмороками) или семейной историей внезапной смерти. Аритмии, связанные с аномалией реполяризации, могут быть ответственными за долю необъяснимых смертей, преимущественно у молодых мужчин, как сообщалось ранее. Такие аритмии могут также быть причиной некоторых недиагностированных причин обморока, которые, как сообщалось, увеличивают риск преждевременной смерти.
Результаты нашего исследования, которые требуют подтверждения со стороны других исследователей, имеют несколько ограничений. Хотя когорта включала субъектов со строго определенными общими чертами, сбор данных был неравномерным среди центров. В нашем изучаемом населении у нас не было субъектов со структурной болезнью сердца и у не много спортсменов или чернокожих, поэтому результаты могут не относиться к этим подгруппам. Самое главное, хотя наши результаты свидетельствуют о том, что ранняя реполяризация является маркером расстройства, связанного с злокачественными аритмиями, исследования предсказывают благоприятный курс для большинства из этих пациентов. Необходимы дальнейшие исследования для выявления факторов, которые модулируют лежащую в основе аритмогенность и предсказывают, какие пациенты подвергаются риску.
В заключение, это многоцентровое исследование показало более высокую, чем ожидалось, распространенность ранней реполяризации у пациентов моложе 60 лет, у которых была идиопатическая фибрилляция желудочков, которая вызвала обморок и внезапную остановку сердца.
IV. Патология клапанов
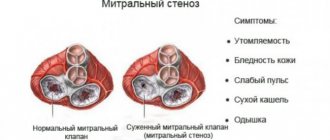
Аортальный стеноз
Среди пациентов, причиной смерти которых является аортальный стеноз (АС), около 20% составляет внезапная сердечная смерть. При отсутствии симптомов, выживаемость больных с АС высока даже без замены клапана. Прогностическое значение различных гемодинамических и электрофизиологических исследований ограничено. Асимптомные пациенты с гемодинамически выраженным аортальным стенозом должны находиться под постоянным наблюдением и при развитии симптомов – безотлагательно прооперированы. У пациентов с документированной устойчивой желудочковой тахикардией должна рассматриваться возможность имплантации КД.
Аортальный стеноз
| Класс | I | IIa | IIb |
| Стратифика-ция риска | Синкопы Стенокардия | ЖТ, в том числе индуцируемые при ЭФИ Снижение толерантности к физической нагрузке | Значимый стеноз |
| Первичная профилактика | Хирургическое лечение | Амиодарон | |
| Вторичная профилактика | КД |
Пролапс митрального клапана
Пролапс митрального клапана (ПМК), как правило, имеет благоприятный прогноз; имеются предположения о риске внезапной сердечной смерти, однако доказательства отсутствуют. Большинство случаев ВСС описано у пациентов, перенесших ранее синкопы или остановку сердца, семейный анамнез ВСС в молодом возрасте, с выраженным пролабированием или миксоматозным изменением створок митрального клапана. Пациентам, выжившим после остановки сердца, рекомендуется имплантация КД.
Пролапс митрального клапана
Класс
| I | IIa | IIb | |
| Стратификация риска | Устойчивая ЖТ ФЖ | Семейный анамнез ВСС Выраженное пролабирование или миксоматозное изменение створок | Удлинение интервала QT Частые/групповые ЭС Индуцируемая ЖТ/ФЖ при ЭФИ Регургитация на митральном клапане Поздние потенциалы |
| Первичная профилактика | |||
| Вторичная профилактика | КД |
Диагностические признаки остановки сердца
Синдром остановки сердца включает ранние признаки состояния клинической смерти. Поскольку данная фаза считается обратимой при проведении эффективных реанимационных мероприятий, симптомы должен знать каждый взрослый человек, так как на раздумье отпущено несколько секунд:
- Полная потеря сознания — пострадавший не реагирует на окрик, тормошение. Считается, что мозг умирает через 7 минут после остановки сердечной деятельности. Это усредненная цифра, но время может изменяться от двух до одиннадцати минут. Мозг первым страдает от кислородной недостаточности, прекращение метаболизма вызывает смерть клеток. Поэтому рассуждать, сколько проживет мозг пострадавшего, некогда. Чем раньше начата реанимация, тем больше шансов на выживание.
- Невозможность определить пульсацию на сонной артерии — этот признак в диагностике зависит от практического опыта окружающих. При его отсутствии можно попытаться прослушать сердечные сокращения, приложив ухо к обнаженной грудной клетке.
- Нарушенное дыхание — сопровождается редкими шумными вдохами и промежутками до двух минут.
- «На глазах» происходит нарастание изменения цвета кожи от бледности до посинения.
- Зрачки расширяются через 2 минуты прекращения кровотока, реакция на свет (сужение от яркого луча) отсутствует.
- Проявление судорог в отдельных мышечных группах.
Если на место происшествия прибывает «Скорая помощь», то подтвердить асистолию можно по электрокардиограмме.
V. Патология коронарных артерий
Аномальное отхождение коронарных артерий
Наиболее часто ВСС случается у пациентов с аномальным отхождением ствола левой коронарной артерии от правого либо некоронарного синусов Вальсальвы. Следовательно, особое внимание должно уделяться молодым пациентам с болью в груди, похожей по описанию на ангинозную. Хирургические вмешательства являются наиболее подходящим методом лечения у пациентов с высоким риском внезапной сердечной смерти.
Аномальное отхождение коронарных артерий
| Класс | I | IIa | IIb |
| Стратификация риска | ФЖ | Молодые пациенты со стенокардией или положительным нагрузочным тестом | |
| Первичная профилактика | Хирургическое лечение | ||
| Вторичная профилактика | Хирургическое лечение |
Миокардиальные мосты
Долгосрочный прогноз у пациентов с наличием миокардиальных мостов представляется благоприятным, однако в некоторых случаях данная патология может быть причиной развития тахиаритмий или внезапной сердечной смерти. У симптомных пациентов для диагностики миокардиальных мостов используется количественная коронароангиография, доплеровское исследование и внутрисосудистый ультразвук. Медикаментозное лечение с использованием бета-блокаторов, хирургическое лечение, ангиопластика и стентирование коронарных артерий являются альтернативными методами лечения.
Миокардиальные мосты
| Класс | I | IIa | IIb |
| Стратификация риска | Симптомная ЖТ ФЖ | Ишемия миокарда | |
| Первичная профилактика | Хирургическое лечение у пациентов с ишемией миокарда | Бета-блокаторы | |
| Вторичная профилактика | Хирургическое лечение у пациентов с ишемией миокарда |
Негативное влияние лекарственных средств
Лекарства, вызывающие остановку сердца, применяются для лечения. В редких случаях предумышленная передозировка вызывает смертельный исход. Это следует доказывать судебно-следственным органам. Назначая препараты, врач ориентируется на возраст, вес пациента, диагноз, предупреждает о возможной реакции и необходимости повторного обращения к врачу или вызова «Скорой помощи».
Явления передозировки наступают при:
- несоблюдении режима (прием таблеток и алкоголя);
- намеренном увеличении дозы («забыл выпить утром, так приму сейчас сразу две»);
- сочетании с народными способами лечения (трава зверобоя, пастушьи ушки, самостоятельно приготовленные настойки из ландыша, наперстянки, горицвета);
- проведении общего наркоза на фоне непрекращенного приема препаратов.
Применение травы зверобоя следует очень ограничить, по силе действия она сравнивается с противоопухолевыми цитостатиками
Наиболее частыми причинами остановки сердца служит прием:
- снотворных средств из группы барбитуратов;
- наркотических препаратов для обезболивания;
- группы β-адреноблокаторов при гипертензии;
- лекарственных средств из группы фенотиазинов, назначаемых психиатром в качестве успокаивающего;
- таблеток или капель из сердечных гликозидов, которые используются для лечения аритмий и декомпенсированной сердечной недостаточности.
Подсчитано, что 2% случаев асистолии связаны с лекарственными препаратами.
Определить, какие лекарства имеют наиболее оптимальные показания и обладают наименьшими свойствами к накоплению, привыканию, может только специалист. Не следует делать это по совету знакомых или самостоятельно.
VI. Синдром Вольфа-Паркинсона-Уайта (WPW)
По данным современных исследований, у пациентов с синдромом WPW частота внезапной сердечной смерти составляет 0,15% в год. Основной причиной ВСС является переход фибрилляции предсердий с быстрым желудочковым ответом в фибрилляцию желудочков. Выжившие после реанимации по поводу внезапной сердечной смерти, как правило, характеризуются отсутствием симптомов, укорочением интервалов R-R (меньше 250 мс) во время пароксизма фибрилляции предсердий, наличием множественных или задне-перегородочных дополнительных путей проведения. Электрофизиологическое исследование с возбуждением предсердий и определением интервалов R-R между предвозбужденными комплексами QRS имеет высокую чувствительность, но специфичность и значимость при определении положительного предиктора ограничены. У пациентов с высоким риском ВСС рекомендована катетерная абляция, в особенности у реанимированных после фибрилляции желудочков или больных с клиническими проявлениями во время приступов фибрилляции предсердий с быстрым ответом желудочков.
Синдром Вольфа-Паркинсона-Уайта
| Класс | I | IIa | IIb |
| Стратифика-ция риска | меньше 250 мс продолжительность цикла при ФП меньше 270 мс антероградный рефрактерный период дополнительных путей проведения Множественные дополнительные пути проведения | Прекращение предвозбуждения при лечении аймалином | |
| Первичная профилактика | Абляция при фибрилляции предсердий и наличии быстрого проведения через дополнительные пути | Абляция у асимптомных пациентов с – семейным анамнезом ВСС – спортсменов | Амиодарон Антиаритми-ческие препараты классов Ia и Iс |
| Вторичная профилактика | Абляция |
VII. Брадиаритмии
Установлено, что брадиаритмии являются причиной внезапной сердечной смерти в 15-20% случаев. Факторами риска брадиаритмической смерти являются AV блокада высокой степени с нарушениями внутрижелудочкового проведения, однако при наличии структурных изменений в сердце эти факторы могут предрасполагать к развитию тахиаритмий. Электрокардиостимуляция является средством выбора у пациентов группы высокого риска с брадиаритмией: она купирует симптоматику и может снизить летальность.
Стратификация риска при нарушениях сердечной проводимости
| Класс | I | IIa | IIb |
| Проибретенная AV блокада | AV блокада III степени AV блокада II степени, тип II Синкопы Сочетание заболевания сердца с ХСН | ||
| Врожденная AV блокада III степени | Синкопы Удлинение интервала QT Врожденные заболевания сердца | ||
| Хроническая двух– или трехпучковая блокада | Сочетание заболевания сердца с ХСН | Синкопы Проведение от пучка Гисса к желудочкам 100 мс (интервал HV 100 мс) Внутрижелудочковые блокады Блокады, индуцируемые при проведении ЭФИ |
Какие последствия вызывает остановка сердца
Последствия остановки кровообращения зависят от скорости и правильности оказания неотложной помощи. Длительная кислородная недостаточность органов вызывает:
- необратимые очаги ишемии в головном мозге;
- поражает почки и печень;
- при энергичном массаже у пожилых людей, детей возможны переломы ребер, грудины, развитие пневмоторакса.
Масса головного и спинного мозга вместе составляет всего около 3% всей массы тела. А для их полного функционирования необходимо до 15% общего сердечного выброса. Хорошие компенсаторные возможности дают возможность сохранения функций нервных центров при снижении уровня кровообращения до 25% от нормы. Однако даже непрямой массаж позволяет поддерживать только 5% от нормального уровня кровотока.
Последствиями со стороны головного мозга могут быть:
- нарушение памяти частичного или полного характера (пациент забывает о самой травме, но помнит, что было до нее);
- слепота сопутствует необратимым изменениям в зрительных ядрах, зрение восстанавливается редко;
- приступообразные судороги в руках и ногах, жевательные движения;
- разные типы галлюцинаций (слуховые, зрительные).
Внегоспитальная реанимация
Выживаемость после остановки сердца варьирует от 5% до 60% в зависимости от характеристик остановки сердца (то есть сердечной этиологии или нет; верифицированная или нет; фибрилляция желудочков или нет). На результат сердечно-легочной реанимации (СЛР) влияет не только успешность ее проведения, но и состояние пациента до начала СЛР.
В настоящее время общепринятым считается тот факт, что время, прошедшее до электрической дефибрилляции является единственным и наиболее значимым определяющим фактором выживаемости после остановки сердца.
Инструкция к автоматическому наружному дефибриллятору позволяет проводить дефибрилляцию в случаях внегоспитальной фибрилляции желудочков или желудочковой тахикардии людям немедицинских профессий, часто за много минут до прибытия бригады скорой помощи. Эта стратегия известна на Западе как «дефибрилляция, проведенная первым отреагировавшим», по принципу взаимопомощи.
Что происходит при остановке сердца
Через несколько секунд от ее начала развиваются:
- слабость и головокружение;
- через 10-20 секунд — потеря сознания;
- еще через 15-30 секунд развиваются так называемые тонико-клонические судороги, дыхание редкое и агональное;
- на 2 минуте наступает клиническая смерть;
- зрачки расширяются и перестают реагировать на свет;
- кожа бледнеет или приобретает синеватый оттенок (цианоз).
Шансы на выживание невелики. Если больному повезло и рядом оказался человек, способный провести непрямой массаж сердца — вероятность пережить синдром внезапной остановки сердца возрастает. Но для этого необходимо «запустить» сердце не позднее, чем через 5-7 минут после того, как оно остановилось.