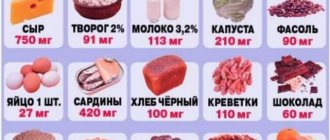
Женский гормон эстроген – вещество, определяющее здоровье женщины. Выделяют более 30 эстрогеноподобных веществ, но самыми значимыми являются эстрадиол, эстрон и эстриол. Механизм действия этих фракций заключается в поддержании репродуктивной, сердечно-сосудистой, нервной систем и опорно-двигательного аппарата.
За что отвечает гормон эстроген?
Эстроген у женщин производится из андрогена в результате ферментативных реакций.
Роль эстрогенов в работе женского организма заключаются в следующем:
- построение силуэта по женскому типу, особое скопление жира в нижней части тела;
- рост матки, труб, яичников;
- рост груди у подростков;
- оволосение по женскому типу, пигментирование сосков и внешних половых органов;
- тонус матки в период овуляции, сократительные движения труб для продвижения сперматозоидов;
- регулярный менструальный цикл, возможность зачатия;
- торможение роста холестериновых бляшек, своевременный вывод «вредного» холестерина (поддержание в норме липидного обмена);
- снижение риска остеопороза;
- поддержание баланса ферратов и меди в крови;
- нормализация когнитивных способностей – запоминания, концентрации;
- обеспечение адекватного течения беременности;
- поддержание здоровья ногтей, волос и кожных покровов.
Эстрогены – производные прогестерона – оказывают комплексное влияние на организм женщины. Они принимают участие в работе сердечной мышцы, поддерживает терморегуляцию организма, процесс усвоения кальция. Именно под их воздействием у девочек-подростков формируются вторичные половые признаки – женственный голос, фигура.
Наряду с тем, как эстроген – отвечает за женственность, тестостерон (стероидный гормон) – ответственный за мужественность. Если у мужчины преобладает эстроген перед тестостероном, у него проявляются женские черты.
МЕТАБОЛИЗМ ЭСТРОГЕНОВ У ЖЕНЩИН
(общие представления и клиническая практика)
ЧАСТЬ II
МЕТАБОЛИЗМ ЭСТРОГЕНОВ У ЖЕНЩИН (ОБЩИЕ ПРЕДСТАВЛЕНИЯ И КЛИНИЧЕСКАЯ ПРАКТИКА).
ЧАСТЬ 2. ЛЕЧЕНИЕ ГИПЕРЭСТРОГЕНЕМИИ
Доминирование эстрогенов является достаточно частым нарушением метаболизма женских половых гормонов и проявляется развитием у женщины следующих заболеваний: эндометри-оз, полипы эндометрия, дисплазия шейки матки, фиброзно-кистозная мастопатия, фибромиома матки и т.д. Наличие перечисленных заболеваний у пациентки свидетельствует о нарушении метаболизма эстрогенов, причем степень метаболического дисбаланса находится за пределами компенсаторных возможностей организма. Мириться с этими болезнями нельзя, так как усугубление нарушения метаболизма эстрогенов может привести к развитию злокачественных новообразований матки и молочной железы. По нашему мнению, использовать для лечения этих заболеваний синтетические гормоны нежелательно. Это связано с тем, что метаболизм синтетических гормонов в основном происходит по генотоксическому пути и, кроме того, они могут блокировать ключевые ферменты, которые детоксицируют женские половые гормоны. Так, по данным исследований, метаболиты синтетических гормонов эквилин и эквивелин преобразуются в печени в 4-гидрокси-о-квинон-глютатион конъюгаты. Насыщенное бета-кольцо этих гормонов переключает синтез 2-гидроксиметаболитов женских половых гормонов на 4-гидрокси-путь. [1]. Помимо этого, эндогенный 4-гидроксиэстрон обладает более слабым эффектом в отношении индуцирования повреждений ДНК и апоптоза в клеточных культурах рака молочной железы по сравнению с 4-гидроксиэквиленином [2]. О влиянии метаболитов синтетических гормонов на активность ключевых ферментов детоксикации свидетельствуют следующие данные. Так, 4-гид-роксиэквиленин является необратимым ингибитором СОМТ, которая катализирует метилирование 4-гидроксиэстрадиола [3]. 4-гидрокси-эквиленин, так же как 4,17-гидроксиэквиленин. существенно снижает активность глютатион-S-трансферазы буквально через несколько МИНУТ после введения в организм [4].
1 ПРИЧИНЫ ЗАБОЛЕВАНИЙ
Первостепенная задача врача перед началом лечения заключается в том, чтобы постараться найти причины, которые привели к развитию этих заболеваний.
Вот далеко не полный их перечень: курение, прием гормональных препаратов, хроничесюш стресс, некачественное и несбалансированное питание, воздействие токсических веществ на производстве и в быту (фталаты, пестициды, тяжелые металлы и т.д.), чрезмерные физические нагрузки, недостаточное потребление витаминов, минералов, незаменимых жирных кислот, антиоксидантов, сопутствующие заболевания, в частности, заболевания органов пищеварения, эндокринных органов, ожирение и т.д.
Особое внимание хотелось бы обратить на постоянный или периодический прием фармацевтических средств. Оказывается, ряд лекарств достаточно негативно воздействует на обмен женских половых гормонов. Так. препарат, который широко используется для лечения язвенной болезни и заболеваний, связанных с повышенной кислотностью — омепразол. является мощным стимулятором цитохрома Р-450 1В1, активация которого приводит к ТОМУ, что в организме женщины образуется больше конпе-рогенного метаболита эстрогенов — 4-гидрокси-эстрона. Фенобарбитал и другие барбитфать:. сахароснижающие препараты (троглитаэон, пиоглитазон), противотуберкулезные препараты (рифампицин) сильно активируют работу другого фермента — цитохрома ЗА4, превращающего эстрон в 16-гидроксиэстрон. Последний представляет собой очень активный метаболит женских половых гормонов, повышение концентрации которого связывают с долгосрочным риском рака матки и молочной железы.
2 ЛЕЧЕНИЕ. ОСНОВНЫЕ НАПРАВЛЕНИЯ КОРРЕКЦИИ МЕТАБОЛИЗМА ЭСТРОГЕНОВ
Основным объектом воздействия лечения в случае доминирования эстрогенов является коррекция метаболизма женских половых гормонов. Подобная тактика позволит не только успешно вылечить заболевание, но и устранить возможность повторного рецидива болезни.
1. Стимулирование предпочтительного (2-гидрокси-) пути детоксикации женских половых гормонов
Очень часто у пациенток с гиперэстрогенемией выявляется низкий уровень 2-гидроксиэстрон — «хорошего» метаболита женских половых гормонов, что свидетельствует о сниженной активности этого пути превращения гормонов. Для его стимулирования, прежде всего, необходимо: уменьшить вдвое количество выкуриваемых сигарет (бензопирен — токсин, который образуется в результате курения, разрушается по этому же пути). В рационе необходимо увеличить потребление сырых крестоцветных овощей (капуста, брюссельская капуста, брокколи, кресс-салат, цветная капуста), а также назначить следующие препараты: индол-3-карбинол (I3C), соевые изофлавоны, омега-3 жирные кислоты.
А. Индол-З-карбинол (I3C)
Индол-З-карбинол (I3C) — мощный активатор цитохрома Р450 1А1, который превращает эстрогены в 2-гидроксиметаболиты. Это вещество получают из крестоцветных овощей, и оно очень нестабильно. Поэтому препараты высокого качества всегда имеют капсулированную форму, в которую добавляют антиоксидант для стабилизации, и обычно срок годности их не превышает 1 года с момента производства. Доза I3C должна составлять 300-450 мг в сутки. Длительность лечения не менее 3 месяцев и определяется по данным повторных лабораторных исследований. Восстановление нормальной концентрации 2-гидроксиэстрогенов и соотношения 2-гидрокси- к 16-гидроксиэстрогенам является основанием для прекращения терапии или перевода на поддерживающую дозу.
Благодаря мощной активации цитохрома Р450 1А1 в организме женщины происходит возрастание концентрации 2-гидроксиэстрогенов, наиболее предпочтительных метаболитов в период до менопаузы [5].
Кроме стимулирования 2-гидроксилирования I3C оказывает множество разнообразных воздействий на клетки организма. Так, было установлено, что I3C стимулирует апоптоз предраковых и раковых клеток молочной железы, и этот эффект связан с тем, что I3C блокировал активацию NF-kappa-B, вызванную трансфекцией Akt гена. Благодаря такому эффекту авторы статьи пришли к заключению, что I3C обладает превентивным действием в отношении некоторых форм рака молочной железы [6]. Полученные данные согласуются с результатами других исследований, которые показали, что I3C индуцирует апоптоз клеток рака молочной железы независимо от р53 и Ьах генов [7]. Подобные данные были получены и при исследовании клеток рака предстательной железы. I3C стимулировал апоптоз этих клеток за счет снижения активации NF-kappa-B и ингибировал их рост благодаря торможению GT фазы клеточного цикла [8]. Исследование влияния I3C на клетки шейки матки показало, что он ингибировал антиапоптотический эффект эстрадиола на эпителиальные клетки, подвергшиеся воздействию потенциальных мутагенных субстанций [9].
Исследование влияния I3C на клеточные линии эпителиальных клеток толстой кишки человека показало, что это вещество обладает противораковым действием благодаря СТИМУЛЯЦИИ апоптоза и усилению детоксикационных возможностей клеток в ответ на воздействие потенциальных мутагенных субстанций [10]. Приведенные данные согласуются с результатами исследований, показавших, что I3C уменьшает риск рака и полипов толстой кишки на экспериментальных моделях животных [11].
Противораковое действие I3C связано не только с его влиянием на метаболизм эстрогенов. Так, установлено, что I3C блокирует анги-огенез в ткани опухоли [12]. оказывает влияние на канцерогенез благодаря связыванию свободных радикалов [13]. I3C также повышает активность глютатион-Б-трансферазы и квинонредуктазы. Это приводит к снижению концентрации квинонов и семиквинонов — канцерогенных метаболитов женских половых гормонов [14]. Индукция детоксикационных ферментов второй фазы детоксикации, таких как глютатион-Б-трансфераза, повышает защиту клеток организма от соединений, которые обладают мутагенным действием. Так, было обнаружено, что I3C индуцирует активность, по крайней мере, 11 различных ферментов второй фазы детоксикации [15].
Таким образом, анализируя вышеприведенные научные данные, можно утверждать, что I3C стимулирует 2-гидрокси-путь — предпочтительный путь детоксикации женских половых гормонов, обладает модулирующим действием на рецепторы эстрогенов, стимулирует апоптоз раковых клеток, обладает антиоксидантными свойствами и стимулирует ферменты как первой, так и второй фаз детоксикации в организме.
Б. Соевые изофлавоны
В случае гиперэстрогенемии положительный эффект мы получали от применения соевых изофлавонов. Существует несколько механизмов их терапевтического действия. Прежде всего, соевые изофлавоны стимулируют 2-гидроксилирование эстрогенов и таким образом увеличивают соотношение 2- к 16-гидроксиэстрогенам. Некоторые авторы рассматривают этот эффект соевых изофлавонов в контексте их противоракового действия [16]. Потребление соевых изофлавонов в дозе 65-132 мг в день снижало экскрецию 4-гидроксиэстрона, потенциально канцерогенного метаболита эстрогенов у женщин в период менопаузы [17]. Подобные данные были получены и при исследовании влияния соевых изофлавонов на метаболизм женских половых гормонов в период до менопаузы [18]. Еще одним положительным эффектом соевых изофлавонов является их способность индуцировать синтез белка, связывающего половые гормоны, в сыворотке крови. Повышение его концентрации уменьшает биодоступность эстрадиола для эстроген-чувствительных тканей [19].
Терапевтическая доза соевых изофлавонов должна составлять 90-180 мг в день в течение нескольких месяцев. Прекращение или перевод на поддерживающую дозу 45-90 мг проводится только после достижения нормальных значений уровней эстрогенов и их метаболитов и при условии клинической регрессии заболеваний.
Следует помнить, что соевый белок не может быть хорошим источником изофлавонов, так как они теряются во время промышленной обработки сои.
В. Другие факторы, влияющие на метаболизм эстрогенов
Оказалось, что потребление омега-3 жирных кислот стимулирует 2-гидроксилирование эстрогенов. Однако механизм действия омега-3 жиров остается неизвестным.
Изучение уровня физической активности у женщин показало, что дозированные физические нагрузки повышают соотношение 2- к 16-гидроксиэстрогенам [20].
2. Ингибирование нежелательных (16-гидрокси- и 4-гидрокси-) путей метаболизма женских половых гормонов
Как упоминалось ранее, 16- и 4-гидрокси-пути метаболизма женских половых гормонов менее желательны для женщин в период до менопаузы. Поэтому снижение активности ферментов, которые участвуют в метаболизме эстрогенов по этим путям, является достаточно важной терапевтической задачей.
Снижение активности цитохрома Р450 ЗА4 приведет к снижению образования 16-гидроксиэстрона — метаболита, который в 8 раз активнее эстрадиола и таким образом существенно ослабит его действие на рецепторы к эстрогенам. Наиболее мощным ингибитором активности цитохрома Р450 ЗА4 является нарингенин — флавоноид, содержащийся в грейпфрутах. По данным некоторых исследований, один стакан грейпфрутового сока снижает активность цитохрома Р450 ЗА4 на 30% в течение 12 часов [21]. Другими натуральными ингибиторами активности этого фермента могут быть корень солодки, чеснок и зверобой.
Снижение активности цитохрома Р450 1В1 возможно с помощью изофлавонов, обнаруженных в растении кюдзю (Pueraria lobata). Наиболее активным изофлавоном этого растения является пуэрарин, который обладает способностью ингибировать активность некоторых цитохро-мов Р450. Было установлено, что он ингибирует активность цитохромов ЗА, 2Е1 и 2В1, поэтому может снижать образование 4-гидроксиэстроге-нов. Помимо этого он стимулирует активность цитохрома 1А2, что вызывает увеличение продукции 2-гидроксиэстрогенов [22].
3. Модулирование функции рецепторов женских половых гормонов
А. Соевые изофлавоны
Соевые изофлавоны обладают способностью модулировать рецепторы эстрогенов.
Исследования in vitro и in vivo показали, что эстрогены оказывают слабый эстрогенный эффект, который примерно в 1000 раз слабее эффекта эстрадиола [23]. В другом исследовании было показано, что изофлавоны, связываясь с рецепторами эстрогенов, могут конкурировать с эстрадиолом за рецептор или даже блокировать функцию рецептора [24].
Б. Индол-З-карбинол (I3C)
Было показано, что продукт метаболизма I3C в организме может выступать в качестве лиганда к рецепторам эстрогенов и демонстрировать эффект, похожий на тамоксифен, в отношении эстроген-зависимых тканей [25].
В других исследованиях показано, что 13С является антагонистом ос-эстрогеновых рецепторов. Кроме того, это вещество, с одной стороны, супрессирует эстроген-чувствительные гены pS2 и катепсин-D, а с другой — повышает активность гена BRCA1, который, в свою очередь, блокирует транскрипционную активность альфа-рецептора эстрогенов [26].
В. Нарингенин и ресвератрол
Нарингенин — флавоноид, содержащийся в грейпфрутах, и антиоксидант ресвератрол, имеющийся в красном винограде, влияют на передачу сигналов эстрогенов благодаря прямому и непрямому блокирующему эффекту на а-рецептор эстрогенов [27]. Причем механизм действия этих нутриентов различен [28].
Г. Витамин В6
Пиридоксин (витамин В6) влияет на передачу сигналов стероидных гормонов, в том числе и эстрогенов. Исследования показали, что витамин В6 взаимодействует с гормон-рецептор-ным комплексом и снижает его связывание с ДНК и таким образом нарушает передачу гормонального сигнала к ДНК клетки [29]. Исходя из этого, пациентки с высоким уровнем эстрогенов должны получать достаточно высокие дозы витамина В6 (30-50 мг в сутки).
4. Борьба с оксидативным стрессом
Оксидативный стресштриводит к образованию семиквинонов и квинонов — метаболитов женских половых гормонов, вызывающих необратимые повреждения ДНК клеток. Для борьбы с оксидативным стрессом следует выполнить две задачи. Во-первых, обеспечить необходимыми нутриентами собственную антиоксидантную систему. Так. медь и цинк необходимы для супероксиддисмллазы. селен и ацетилцис-теин — для глютатионпероксидазы. витамин ВЗ — для глютатионредуктазы. железо — для каталазы. Во-вторых, назначить растительные антиоксиданты, такие как катехины зеленого чая, ликопен, куркума, лимонен, витамины С и Е, |3-каротин, способные инактивировать реакционные частицы кислорода.
5. Поддержание ферментов второй фазы детоксикации, которые принимают участие в окончательной инактивации женских половых гормонов
Лечебные мероприятия для поддержания окончательной элиниминации женских половых гормонов должны охватывать 3 основных пути второй фазы детоксикации.
А). Важным условием нормального функционирования процессов метилирования в организме является потребление достаточного количества белка. Это связано с тем, что универсальным донором метиловых группировок в организме является s-аденозин-метионин, который, в свою очередь, образуется из аминокислоты метионина, потребляемой, в основном, с животным белком. Поэтому необходимо провести всестороннюю оценку питания женщины и в случае недостаточного потребления белка ввести в рацион белковую пишу. Для точной оценки потребности в белке лучше использовать специальные компьютерные программы, позволяющие не только правильно оценить качество рациона женщины, но и восстановить обнаруженный дисбаланс. С этими программами можно ознакомиться на сайте www.anti-aging.kiev.ua.
Помимо белка для процессов метилирования необходимы микронутриенты, являющиеся кофакторами ферментативных систем метилирования.’ Поэтому в лечебный план должны входить следующие витамины и минералы:
— фолиевая кислота в дозе 400-1000 мг в сутки;
— витамин В6 в дозе 10-40 мг в сутки;
— витамин В2 в дозе 15-30 мг в сутки;
— витамин В12 в дозе 250-500 мкг в сутки;
— магний в дозе 400-800 мг в сутки.
Однако не у всех пациенток вышеприведенная терапия может оказаться эффективной. Это связано с тем, что примерно у 25% европейцев обнаруживается генетический полиморфизм MTHFR- ключевого фермента процессов метилирования в организме. У этих пациентов восстановить процессы метилирования можно или с помощью метилированной формы фолиевой кислоты (5-метил-тетрагидрофолата), или с помощью соляно-кислого бетаина, выступающего донором метиловых группировок, независимо от 5-метил-тетрагидрофолата. Таким образом, если не известны генетические особенности пациентки, лучше назначать комплекс витаминов группы В, содержащий метилированную форму фолиевой кислоты и соляно-кислый бетаин.
Б). Конъюгирование с глютатионом участвует в инактивации квинонов, генотоксических метаболитов женских половых гормонов. Для нормального протекания этой реакции необходим N-ацетилцистеин — аминокислота, ограничивающая синтез глютатиона. Показано, что назначение этой аминокислоты приводит к существенному возрастанию концентрации восстановленного глютатиона в тканях и ускорению протекания конъюгирующих реакций с глютатионом [30]. Силимарин также стимулирует эндогенный синтез глютатиона [31].
В). Для поддержания активности сульфитации следует назначать молибден и неорганические сульфаты.
Г). Для активации процессов глюкуронизации необходима глюкоза. Поэтому абсолютная недостаточность инсулина или инсулиноре-зистентность, которые сопровождаются снижением концентрации глюкозы внутри инсулин-зависимых клеток, всегда сопровождаются в той или иной степени нарушениями глюкуронизации. Помимо углеводного обмена на активность процессов глюкуронизации активно влияет трийодтиронин — самый активный гормон щитовидной железы. ТЗ стимулирует экспрессию генов УДФ-глюкоронозилтранс-феразы, причем эта активация зависит от обеспеченности организма витамином А [32]. Наряду с ТЗ глюкозонилаты, присутствующие в кресс-салате и других крестоцветных овощах, являются мощными индукторами ключевого фермента глюкуронизации — УДФ-глюкороно-зилтрансферазы [33]. Подобным эффектом обладает и экстракт артишока [34].
6. Предупреждение тонкокишечно-печеночной рециркуляции женских половых гормонов
Для предупреждения всасывания женских половых гормонов в кишечнике, прежде всего, необходимо потреблять достаточное количество клетчатки. Женщины, которые следуют этой рекомендации, имеют в крови более низкий уровень эстрогенов [35]. Наиболее активно сорбирует эстрогены соевая клетчатка и клетчатка семян льна. Большую роль в рециркуляции эстрогенов из кишечника играет (З-глюкурони-даза, фермент бактерий, который отщепляет глюкуроновую кислоту от детоксицированых соединений (эстрогенов). Наиболее сильным ингибитором активности этого фермента является кальция глюкарат — нутриент, присутствующий в некоторых овощах [36]. Кроме этого силимарин и корень солодки также снижают его активность [37].
7. Снижение активности ароматазы
Как упоминалось ранее, ароматаза — это фермент, превращающий андоростендион в эстрон и тестостерон — в эстрадиол. Однако в некоторых случаях (при ожирении, воздействии гербицидов [38], воздействии пестицидов [39, 40], избыточном потреблении алкоголя [42]) активность этого фермента существенно возрастает, что приводит к образованию большого количества эстрогенов. О высокой активности фермента свидетельствует нормальный или с тенденцией к снижению уровень андростен-диона и тестостерона в периферической крови, сопровождающийся высокой концентрацией эстрадиола и эстрона. На сегодня существует достаточно большое количество ингибиторов ароматазы, использующихся для лечения рака молочной железы. Среди этих препаратов можно выделить «Anastrasol», «Arimidex». Кроме того, существует ряд натуральных соединений, которые обладают способностью снижать активность фермента. Среди них можно выделить кризин, апигенин, нарингенин [41]. Однако использовать ингибиторы ароматазы необходимо с осторожностью, так как их назначение может вызвать относительное или абсолютное доминирование андрогенов. Это приведет к появлению акне, особенно непосредственно перед менструацией или в период менструации, образованию кист в яичниках и других симптомов доминирования андрогенов.
3 ЗАКЛЮЧЕНИЕ
Таким образом, в лечении заболеваний, связанных с доминированием эстрогенов, появилась безопасная и высоко эффективная альтернатива гормонотерапии и терапии, направленной на ингибирование секреции гонадотропинов, которая оказывает достаточно стойкий положительный эффект на течение заболевания. Хорошие клинические результаты этого подхода обусловлены воздействием лечения на причины, которые привели к доминированию эстрогенов, пониманием всей сложной цепочки метаболизма эстрогенов, комплексным подходом к коррекции гормональных нарушений и использованием безопасных натуральных соединений, которые оказывают мощное модулирующее действие на процессы превращения эстрогенов.
БИБЛИОГРАФИЯ
- Zhang F, Chen Y, Pis ha E, Shen L, Xiong Y, van Breemen KB, Bolton JL. The major metabolite of equilin, 4-hydroxyequilin, autoxidizes to an o-quinone which isomerizes to the potent cytotoxin 4-hydroxyequiknin-o-quinone. Zhang E, Chem Res Toxicol 1999 12(2):204-213.
- Chen Y, Liu X, Pisha E, Constantinou AI, Hua Y, Shen L, van Breemen RB, Elguindi EC, Blond SY, Zhang F, Bolton JL. A metabolite of equine estrogens, 4-hydroxyequilenin, induces DNA damage and apoptosis in breast cancer cell lines. Chem Res Toxicol (United States) May 2000, 13(5):342-350.
- Yao J, Li Y, Chang M, Wu H, Yang X Goodman JE, Liu X Liu H Mesecar AD, Van Breemen RB, YagerJD, Bolton JL. Catechol estrogen 4-hydroxyequilenin is a substrate and an inhibitor of catechol-O-methyltransferase. Chem Res Toxicol (United States) May 2003;16(5):668-675.
- Yao J, Chang M, Li Y, Pisha E, LiuX, Yao D, Elguindi EC, Blond SY, Bolton JL. Inhibition of cellular enzymes by equine catechol estrogens in human breast cancer cells: specificity for glutathioneS-transferase Pl-1. Chem Res Toxicol (United States) Jul 2002;15(7):935-942.
- Michnovicz JJ, Adlercreutz H, Bradlow HL. Changes in levels of urinary estrogen metabolites after oral indole-3-carbinol treatment in humans. J Natl Cancer Inst, May 21 1997;89(10):718-723.
- Rahman KM, Li Y, Sarhar FH. Inactivation of akt and NF-kappaB play important roles during indole-3-carbinol-induced apoptosis in breast cancer cells. Nutr Cancer 2004;48(l):84-94.
- Ge X Fares FA, Yannai S. Induction of apoptosis in MCF-7 cells by indole-3-carbinol is independent of p53 and bax. Anticancer Res, Jul-Aug 1999; 19(4B):3199-3203.
- Chinni SR, Li Y, Upadhyay S, Koppolu PK, Sarhar FH. Indole-3-carbinol (I3C) induced cell growth inhibition, Gl cell cycle arrest and apoptosis in prostate cancer cells. Oncogene May 24 2001;20(23):2927-2936.
- Chen D, Carter TH, Auborn KJ. Apoptosis in cervical cancer cells: implications for adjunct anti-estrogen therapy for cervical cancer. Anticancer Res Sep-Oct 2004;24(5A):2649-2656.
- Bonnesen C, Eggleston IM, Hayes JD. Dietary indoles and isothiocyanates that are generated from cruciferous vegetables can both stimulate apoptosis and confer protection against DNA damage in human colon cell lines. Cancer Res (United States) Aug 15 2001;61(16):6120-6130.
- Kim DJ Shin DH, Ahn B, KangJS, Nam KT, Park CB, Kim CK, HongJT, Kim YB, Yun YWJangDD, YangKH. Chemoprevention of colon cancer by Korean food plant components. Mutat Res Feb-Mar 2003;523-524:99-107.
- Chang X, Той JC, Hong C, Kim HA, Riby JE, Firestone GL, Bjeldanes LF. 3,3′-Diindolylmethane inhibits angiogenesis and the growth of transplantable human breast carcinoma in athymic mice. Carcinogenesis Apr 2005;26(4):771-778.
- ArnaoMB, Sanchez-Bravo J, Acosta M. Indole-3-carbinol as a scavenger of free radicals. Biochem Mol Biol Int (Australia) Aug 1996;39(6): 1125-1134.
- Staack R,KingstonS] Wallig MA, Jeffery EH. A comparison of the individual and collective effects of four glucosinolate breakdown products from brussels sprouts on induction of detoxification enzymes. Toxicol Appl Pharmacol Mar 1998;149(l):17-23.
- Wallig MA,KingstonS, Staack R, Jefferey EH. Induction of rat pancreatic glutathione S-transferase and quinone reductase activities by a mixture of glucosinolate breakdown derivatives found in Brussels sprouts. Food Chem Toxicol (England) May 1998;36(5):365-373.
- Kishida T, Beppu M, Nashiki К Izumi T, Ebihara К Effect of dietary soy isoflavone aglycones on the urinary 16alpha-to-2-hydroxyestrone ratio in СЗН/HeJ mice. Nutr Cancer (United States) 2000;38(2):209-214.
- Xu X,DuncanAM, Wangen KE, Kurzer MS. Soy consumption alters endogenous estrogen metabolism in postmenopausal women. Cancer Epidemiol Biomarkers Prev Aug 2000;9(8):781-786.
- XuX Duncan AM, Merz BE, Kurzer MS. Effects of soy iwflavones on estrogen and phytoestrogen metabolism in premenopausal women. Effects of soy isoflavones cm estrogen and phytoestrogen metabolism in premenopausal women. Cancer Epidemiol Biomarkers Prev Dec 1998;7(12):1101-1108.
- Adlercreutz H, Hockerstend K, Bannwart, et al. Effect of dietary components, including lignans and phytoestrogens, on enterohepatic circulation and liver metabolism of estrogens and on sex hormone-binding globulin (SHBG). J Steroid Biochem 1987;2 7(4-6):1135-1144.
- Matthews CE, FowkeJH, Dai Q, Leon Bradlow H,Jin F, Shu XO, Gao YT, Longcope C, HebertJR Zheng W. Physical activity, body size, and estrogen metabolism in women. Cancer Causes Control (Netherlands) Jun 2004;15(5):473-481.
- Yee GC, Stanley DL, Pessa LJ, et al. Effect of grapefruit juice on blood cyclosporine concentration. Lancet 1995;345:955-956.
- Guerra MC, Speroni E, Brocolli M, et al. Companion between Chinese medical herb Pueraria lobata crude extract and its main isoflavone puerarin. Antioxidant properties and effects on rat liver CYP-catalysed drug metabolism. Life Set 2000;67:2997-3006.
- Miksicek RJ. Commonly occurring plant flavonoids have estrogenic activity. Mol Pharmacol 1993;44:37-43.
- Pollard JW. Modifiers of estrogen action. Sci Med Jul/Aug 1999:38-47.
- Riby JE, Feng C, Chang YC, Schaldach CM, Firestone GL, Bjeldanes LF. The major cyclic trimeric product of indole-3-carbinol is a strong agonist of the estrogen receptor signaling pathway. Biochemistry (United States) Feb 8 2000;39(5):910-918.
- Meng Qj Yuan F, Goldberg ID, Rosen EM, Aubom K, Fan S. Indole-3-carbinol is a negative regulator of estrogen receptor-alpha signaling in human tumor cells. J Nutr Dec 2000;130(12):292 7-2931.
- Yoon K, Pellaroni L, StonerM, Gaido K, Safe S. Differantial activation of wild-type and variant forms of estrogen receptor a by synthetic and natural estrogenic compounds using a promoter containing three three estrogen-responsive elements. J Steroid Biochem Mol Biol 2001;78:25-32.
- Yoon K, Pellaroni L, Ramamoorthy K, Gaido K, Safe S. Ligand structure-dependant differences in activation of estrogen receptor alfa in human HepG2 liver and U2 osteogenic cancer cell lines. Mol. Cell Endocrinol 2000;162:211-220.
- Bender DA. Novel function of vitamin B6. Proceedings Nutr Soc 1994;53:625-630.
- DeFlora S, Benniceli C, Camoiriano A et al. In vivo effects of N-acetylcysteine on glutatione metabolism and on biotransformation of carcinogen and/or mutagenic compounds. Carcinogenesis. 1985;6:1735-1745.
- Wellington K,Jarvis B. Silymarin: a review of its clinical properties in the management of hepatic disordes. BioDrugs 20()1;15(7): 465-489.
- Haberkorn V, HeydelJM, MounieJ, Artur Y, Gaudonnet H. Influence of vitamin A status on the regulation of uridine (5~~-) diphosphate-glucuronosyltransferase (UGT) 1A1 and UGT1A6 expression by L-triiodthyronine. British J Nutr 2001;85:289-297.
- Kassie F, Robot S, Uhl M et al. Chemoprotective effects of garden cress (Lepidium sativum) and its constituents towards 2-amino-3-methyl-imidazol[4,5-f]quinolin (IQJ-induced genotoxic effects and colonic preneoplastic lesions. Carcinogenesis 2002;23(7):1155-1161.
- KirchhoffR Beckers CH, KirchhoffGM, Trinczek-Gartner H. Petrowicz O, Reimann HJ. Increase in choleresis by means of artichoke extract. Phytomed 1994;1:107-115.
- Goldin BR Adlercreutz H, Gorbach SL. Et al. Estrogen excretion patterns and plasma levels in vegetarian and omnivorous women. New EnglJ Med 1982;307:1542-1547.
- Dwivedi C, Heck Wf, Downie AA, Larroya S, Webb ТЕ. Effect of calcium glucarate on fl-glucoronidase activity and glucarate content of certain vegetables and fruits. Biochem Med Metab Biol 1990;43:83-92.
- KumagaiA, Nishino K, Shimomura A, Kin T, Yamamura. Effect of glycyrrhizin on estrogen action. Endocrinol Japan 1967;14(l):34-38.
- HeckerM, Park JW, Murphy MB, Jones PD, Solomon KR, Van DerKraak G, CanJ A, Smith EE, du Preez L, Kendall RJ, Giesy JP. Effects of atrazine on CYP19 gene expression and aromatase activity in testes and on plasma sex steroid concentrations of male African clawed frogs (Xenopus laevis). ToxicolSci (United States) Aug 2005;86(2):273-280.
- Holloway AC, Stys KA, Foster. DDE-induced changes in aromatase activity in endometrial stromal cells in culture. Endocrine (United States)Jun 2005;27(1):45-50.
- Sanderson JT, Boerma J, Lansbergen GW, van den Berg M, Induction and inhibition of aromatase (CYP19) activity by various classes of pesticides in H295R human adrenocortical carcinoma cells. Toxicol Appl Pharmacol (United States) Jul 1 2002;182(l):44-54.
- Sanderson JT, HordijkJ, Denison MS, Springs teel MF, Nantz MH, van den Berg M. Induction and inhibition of aromatase (CYP19) activity by natural and synthetic flavonoid compounds in H295R human adrenocortical carcinoma cells. ToxicolSci (United Stales) Nov 2004;82(l):70-79.
- Etique N, Chardard D, Chesnel A, Merlin JE, Flament S, Grillier-Vuissoz I. Ethanol stimulates proliferation, ERalpha and aromatase expression in MCF-7 human breast cancer cells. Int J Mol Med (Greece) Jan 2004;13(l):149-55.
Виды женского гормона
Три базовые фракции:
- Эстрадиол – важнейший гормон. До наступления фазы полового созревания у мальчиков и девочек его концентрация в крови одинакова, содержание меняется примерно в 12–13 лет. Участвует в скоплении жировых тканей на груди, бедрах, развитии молочных желез, поддерживает тонус кожи. В пубертатной фазе формирует половые признаки, у взрослых женщин поддерживает здоровье кожных покровов, волос, замедляет клеточное старение, участвует в построении костной ткани, утилизирует вредный холестерин, влияет на эмоциональную стабильность. В гестационном периоде способствует увеличению размеров матки вместе с ростом плода, повышает интенсивность обмена веществ, формирует костные ткани плода и обеспечивает его питательными компонентами и кислородом.
- Эстрон . Синтезируется корой надпочечников, яичниками и жировыми клетками. Является «промежуточным» гормоном, организмом используется как исходное сырье для выработки эстрадиола.
- Эстриол . Практически не влияет на фон гормонов у женщин, малоактивен в организме, содержится в незначительных количествах. Но сразу после зачатия уровень его повышается под влиянием гонадотропина, чтобы подготовить матку к росту при увеличении плода. Также формирует протоки в груди для лактации, снижает риск тонуса матки, предотвращает спазмы, усиливает кровоток в маточной полости. Продуцируется плацентарной тканью.
Прогестерон
Поскольку существует тесная связь между эстрогеном и прогестероном, стоит упомянуть, что доминирование эстрогена также могут вызывать низкие уровни прогестерона. Под этим подразумевается, что даже если у вас в организме достаточно эстрогена, вы все равно можете страдать от эстрогенного доминирования, если уровень прогестерона очень низок.
Низкий уровень прогестерона обычно наблюдается у женщин, которые испытывают хронический стресс, постоянно подвергаются воздействию эстрогена и придерживаются диеты, в которой не хватает необходимых питательных веществ.
Норма эстрогена
Нормальное содержание гормонов определяется по периодам менструального цикла:
| Вид эстрогена | 1 фаза | 2 фаза | Беременность | Климакс |
| Эстрадиол | 15-60 нг/л | 27-246 нг/л | 17-18 тыс. нг/л | 5-30 нг/л |
| Эстрон | 5-9 нг% | 3-25 нг% | 1500-3000 нг % | — |
| Эстриол | — | — | 0,7-110 нмоль/л | — |
Эстриол вырабатывает только плацентой, начиная с момента зачатия до 40 недели. Сначала синтезируется из холестерола матери надпочечниками, затем – печенью плода.
В гестационном периоде важными значениями являются не только содержание эстриола у матери, но и у плода. В составе околоплодной жидкости во 2 триместре его должно быть в пределах 3,5–27,1 нмоль/л, в 3 – 7,3–69 нмоль/л.
Основные причины увеличения эстрогена в крови
- Увеличение нагрузок на печень. Избыток гормона выводится этим органом, если печень перегружена токсинами, то не сможет вовремя справляться с этой задачей. Накопление негативных форм эстрогена может привести к эндометриозу и раку груди.
- Длительные запоры. Чем дольше время пребывания токсинов в виде негативных форм эстрогена в кишечнике, тем больше у них шансов попасть обратно в кровь и вызвать гормональный сбой.
- Недосыпание или бессонница. При длительных нарушениях сна, повышается уровень стресса, который связан с выбросом кортизола. Кортизол разрушает прогестерон и гормональный дисбаланс прогрессирует.
- Проблемы с избыточным весом. Жировая ткань помогает накапливаться токсинам и вновь попадать в кровь, перегружая печень. Эта нагрузка провоцирует накопление лишнего эстрогена.
- Ксеноэстрогены. Это гормоны, которые не относятся к организму человека, но имитируют действие эстрогена и блокируют работу настоящего гормона. Поступают они из окружающей среды – это синтетические вещества, содержащиеся в продуктах, косметике, бытовых предметах.
Для выявления гормонального дисбаланса необходимо обратиться к гинекологу-эндокринологу. Самолечение никогда не приводит к положительным результатам.
ОНЛАЙН-ЗАПИСЬ в клинику ДИАНА
Вы можете записаться по бесплатному номеру телефона 8-800-707-15-60 или заполнить контактную форму. В этом случае мы свяжемся с вами сами.
Симптомы дисбаланса
Эстрогены активно влияют на женский организм от первой менструации до развития менопаузы. Как повышение, так и снижение их объёма угнетают репродуктивную функцию, портят внешний вид женщины, состояние сердечно-сосудистой системы, структуру костей и хрящей.
Признаки избытка гормона у женщин
В норме синтез эстрогена увеличивается в фазе полового созревания и при наступлении беременности, если она протекает без патологий. В другие периоды повышение концентрации нередко вызвано неправильной работой организма или поступлением гормона из продуктов питания и окружающей среды.
Причины доминирования эстрогена:
- употребление продуктов с высоким содержанием фитоэстрогенов;
- неправильно подобранная заместительная гормонотерапия;
- частое употребление алкоголя;
- лишний вес;
- заболевания сосудов, сердца, диабет, гипертония;
- неконтролируемый прием ОК (оральных контрацептивов).
Симптомами переизбытка эстрогена являются:
- Чрезмерный набор массы тела
. При повышенном уровне женских гормонов жировая ткань скапливается в основном в области талии, ягодиц, бедер. - Нерегулярный цикл
– скудные или, наоборот, обильные выделения, прорывные кровотечения, гиперполименорея, аменорея и другие нарушения. - Чувствительность и припухлость груди
. В норме это состояние наблюдается за несколько дней до наступления месячных и во время беременности. Если молочные железы болят в средине цикла, это может говорить о повышении уровня эстрогена. - Повышенная эмоциональность
. Может развиваться ПМС, резкие смены настроения, депрессия, беспокойство, панические атаки, бессонница. - Регулярные головные боли
. Чаще всего они связаны с приближающейся менструацией. - Выпадение волос
, облысение, ухудшение состояния ногтей и волос. - Нарушение памяти
. Болезнь Альцгеймера некоторые ученые связывают с пониженным уровнем женского эстрогена. - Хроническая усталость
.
Важно! Осложнения гиперэстрогении – гиперплазия эндометрия, повышенный риск кровотечений, миома, эндометриоз, нарушение цикла.
Выделяют относительную и абсолютную формы:
- относительная гиперэстрогения
– понижение уровня прогестерона при прежнем объёме эстрогенов; - абсолютная гиперэстрогения
– повышение эстрогена при прежней концентрации прогестерона.
У взрослых женщин гиперэстрогенизм может вызывать состояние, аналогичное проявлениям климакса – потливость, приливы, раздражительность, частые головные боли.
Симптомы при недостатке гормона
Эстрогенная недостаточность может быть вызвана такими факторами: прием гормональных средств, патологии щитовидки, терапия эстрогенозависимых опухолей у женщин, приём ноотропов или антидепрессантов, резкое похудение, заболевания гипофиза, несбалансированное питание.
Определить дефицит эстрогена можно по таким симптомам:
- В период полового созревания возможна задержка формирования вторичных половых признаков – отсутствие менархе до 15–16 лет, нерегулярные месячные, формирование у девочек фигуры по мужскому типу с узким тазом, широкими плечами и развитой мускулатурой. Также дисбаланс проявляется уменьшением размеров матки, недоразвитием как внешних, так и внутренних органов половой сферы.
- При климаксе понижение эстрогенов является нормой. Если же концентрация гормонов падает в 40–45 лет и ранее, симптомы менопаузы проявляются ярче – частое сердцебиение, обильное выделение пота, приливы, головокружение, мигрени.
- В возрасте после 35–40 основными симптомами являются увеличение массы тела, сбой в работе ЖКТ, появление морщин, целлюлита, растяжек, родинок и папиллом в большом количестве, снижении либидо, высокой частоте пульса, нарушении кровообращения в головном мозге.
- У молодых женщин дефицит эстрогенов приводит к частым кольпитам, вагинитам, сбоям цикла, ярко выраженному ПМС, снижению работоспособности, болям в суставах, перепадам кровяного давления, отсутствию смазки во влагалище.
При беременности такая патология чревата сбоями в развитии плаценты, отслойкой, выкидышем, аномалиями в формировании нервной и сердечной систем ребенка, маточными кровотечениями. Также повышается риск отклонений генетического характера у плода, в частности синдрома Дауна.
Уровень гормонов в организме во время менструации
Во время месячных матка должна освободиться от верхнего слоя эндометрия. Этому способствует максимальное снижение показателей гормонов прогестерона и эстрогена. Начинается кровотечение, которое не должно длиться более 5 дней в нормальном и здоровом состоянии организма.
Основные симптомы, характеризующие состояние женщины во время месячных:
- появление отеков на ногах, животе и лице – связано с повышением уровня эстрогена;
- наблюдаются колебания веса — внезапно появляются несколько кг и также внезапно исчезают;
- смена настроения — как следствие колебания уровня гормонов;
- набухание груди — продолжается действие прогестерона, но постепенно снижается.
Особенность! Для женщин старше 30 лет характерно снижение обменных процессов, поэтому лишний эстроген постоянно накапливается в организме, вызывая неприятные симптомы.
Все этим симптомы не страшны в малых проявлениях, которые не приносят значительного дискомфорта женщине. Если симптомы усиливаются, продолжаются в течение длительного времени, то это говорит о слишком высоком уровне эстрогенов и требуется консультация специалиста.
Как проверить уровень эстрогена?
Базовый анализ на эстроген – обследование крови.
В ней содержатся все 3 фракции гормона, определяется соотношение каждого вида в соответствии с такими факторами:
- возраст;
- наличие или отсутствие беременности;
- приём препаратов, содержащих любые гормоны;
- вес.
Сдавать анализ важно в соответствии с продолжительностью цикла:
- если цикл составляет 20–21, кровь берут на 2–3 день от начала первого кровотечения;
- при цикле в 28 дней – 3–5 сутки;
- более 28 суток – в интервале 5–7 дней от начала месячных.
Если цикл нерегулярный, предварительно проводят тест на овуляцию. В течение 24 часов с момента ее наступления концентрация эстрогена достигает своего пика.
Перед сдачей анализов женщине рекомендуют ограничить прием гормоносодержащих средств, исключить половую жизнь, физическую активность. Последний приём пищи возможен не позже, чем за 10 часов. Узнать ответ можно через 20–30 минут.
К чему могут привести недостаток или переизбыток эстрогена
Как уже понятно, от уровня эстрогена в крови напрямую зависит физическое и психологическое состояние женщины, поэтому очень важно следить за данным показателем и принимать меры при любом дисбалансе.
Последствия падения уровня эстрогенов:
- различные боли, в основном головные и сердечные, а также болезненные ощущения в пояснице, спине;
- ухудшение терморегуляции, в частности, приливы жара;
- хрупкость костей;
- сужение сосудов;
- ухудшение памяти;
- появление морщин;
- колебания эмоционального фона.
При избытке эстрогенов у женщин возникают:
- различные воспаления;
- вздутие живота;
- повышение давления;
- агрессия, раздражительность и проблемы со сном;
- всевозможные боли.
Причин снижения и повышения эстрогена в организме женщины несколько. Это может быть
- расстройство функционирования гипофиза,
- несбалансированное питание,
- слишком высокие физические нагрузки,
- менопауза и предшествующий ей период.
Избыток эстрогена встречается нечасто, обычно приходится корректировать именно нехватку данного гормона. Самая распространенная ее причина — возрастные изменения в женском организме, которые начинаются после 40 лет. Избежать их и обеспечить себе вечную молодость, к сожалению, невозможно, но есть способы замедлить подобные процессы.
Лечение гормонального дисбаланса
Основная задача терапии – нормализовать этапы выработки эстрогенов, повысить или понизить концентрацию до нормы.
В пубертатную фазу, при менопаузе и или беременности лечение гормонами (гестагенами и эстрогенами) не проводится.
Лекарства
Если при дефиците гормона необходимо принимать препараты, способные восстановить эстроген, то при его избытке категорически запрещено лечится такими лекарственными средствами.
Для повышения уровня эстрогена
Если эстроген синтезируется у женщины в малых количествах, назначают такие препараты:
| Наименование | Действие |
| Премарин | Конъюгированный эстроген. Содержит натуральные эстрогены. Применяют при эстрогеновом дефиците, после оперативного вмешательства на матке, яичниках, с целью профилактики остеопороза в фазу менопаузы. |
| Прогинова | Содержит эстрадиола валерат, восстанавливает объём стероидных гормонов, улучшает состояние хрящевой и костной тканей, убирает проявления менопаузы, улучшает состояние кожи, замедляет старение. |
| Верошпирон | Включает спиронолактон, оказывающий эстрогеноподобный эффект. Обладает мочегонным действием, снижает концентрацию тестостерона, используется в терапии поликистоза яичников, менструальных нарушений. Уменьшает проявления женской алопеции, проблемы кожи, оволосение по мужскому типу. |
| Гемафемин | Содержит пантогематоген марала, повышает концентрацию эстрогена в женском организме, дополнительно включает витамины C, E. Влияет на работу яичников, устраняет приливы, скачки давления. Не используется при беременности, с осторожностью – при нарушении свертывающей способности крови, тромбозах. |
| Стелла | Стимулирует выработку эстрогена, уменьшает активность папилломавируса, снижает риск развития опухолей, продуцирующих эстрогены. В составе – экстракт брокколи, диоксид кремния, зелёный чай, лактоза, экстракт сои. |
| Овестин | Содержит эстриол. Используется для снижения яркости климакса, в терапии бесплодия, после хирургической экстирпации матки, яичников, труб. |
| ОК (Эстрогенолит, Жанин, Активель, Линдинет, Фемоден) | Монофазные контрацептивы содержат синтетические эстрогены в малых дозах. Усиливают естественный процесс продуцирования гормонов, прекращают овуляцию. |
Средства этого вида выпускаются чаще в таблетках, восполняют нехватку эстрогенов. Препараты заместительной гормонотерапии применяются при климаксе, дефиците эстрогена, бесплодии. Оральные контрацептивы чаще назначают для нормализации цикла, при эндометриозе, прорывных кровотечениях.
Для снижения уровня эстрогена
В этом случае практикуют антиэстрогенные препараты.
Назначают в зависимости от причины низкого содержания женского гормона:
- Противоопухолевые лекарственные средства: Аримидекс, Фемара.
- При раке матке, яичников и ановуляторном бесплодие: Тамоксифен.
- При раке груди: Летрозол.
Обзор таблеток, содержащие эстроген →
Эстроген в продуктах питания
{banner_banstat9}
Улучшить эффект медикаментозного лечения, можно с помощью правильно подобранного питания.
Для роста показателей
Активность выработки эстрогена можно увеличить при включении в меню продуктов, которые богаты гормоноподобными веществами:
- овощи
– баклажаны, томаты, морковь, тыква, свёкла; - зелень, травы
– сельдерей, петрушка, спаржа, шпинат, базилик; - фрукты и ягоды
– гранаты, финики, вишня, дыни, абрикосы, папайя, виноград, малина; - молочные продукты
– сыр, сливочное масло, сметана, творог, кефир; - семя подсолнечника
, льна, тыквы, арахис, кунжут; - чеснок
, горчица.
Чтобы максимально сохранить пользу продуктов, подвергайте их минимальной термообработке, включайте в меню ежедневно, выбирайте только свежие овощи и фрукты, готовьте она один раз.
Для снижения показателей
{banner_banstat10}
Цель диеты: снижение веса, нормализация работы пищеварительного тракта:
- исключить консервы, жирные сорта мяса, колбасу, кофе, пиво и алкоголь в целом;
- больше употреблять: грибов, цитрусовых, зеленого чая;
- коровье молоко заменить на кокосовое или рисовое.
Народные средства, повышающие эстроген
Обмен эстрогенов, а также концентрацию гормонов можно нормализовать с помощью народных средств:
- Возьмите 20 свежих листьев малины, на один час залейте 200 мл кипятка. Пейте вместо обычного чая 2 раза в день, предварительно отцедите и охладите. Начинайте прием в средине цикла менструации.
- Залейте 5 шишек хмеля 100 мл кипятка, проварите 5 минут на огне, затем добавьте 5 листьев мяты, настаивайте 40 минут. Пейте по половине стакана трижды в сутки в течение 1 месяца.
- Залейте 100 г семян подорожника 50 мл свежего льняного масла. Оставьте на сутки. Затем принимайте по одной чайной ложке перед едой трижды в день.
- Измельчите 100 г свежих листьев крапивы, выжмите сок из половины лимона, кожуру натрите, всё смешайте. Проварите с 300 мл воды на медленном огне 10 минут, настаивайте под закрытой крышкой полчаса. Затем процедите, принимайте в день до 3 стаканов вместо чая.
- Возьмите в равных количествах сушеную мелиссу, шиповник, залейте водой так, чтобы она покрывала сухие составляющие. Проварите около получаса, остудите, отцедите и пейте по 1 стакану утром и перед сном вместо чая.
Повысить синтез естественных гормонов в женском организме можно при помощи ароматерапии. Используйте масло кипариса, розы, лаванды, мяты, бергамота, апельсина, березовых почек. Также их можно применять для принятия ванн, массажа.
Основные причины снижения уровня гормона в крови
- Рождение ребенка: организм истощается и теряет способность интенсивно вырабатывать гормоны.
- Нерегулярность половых отношений: некоторые исследователи считают, что активная половая жизнь благоприятно сказывается на выработке женских гормонов.
- Малоподвижность: общее снижение активности организма, особенно области таза, проявляется и в снижении выработки эстрогена
- Неправильный рацион питания: некоторые продукты питания блокируют работу эстрогена (жирная пища, газировка, фастфуд в целом).
- Стресс: нервные расстройства негативно сказываются на работе яичников.
- Климакс: завершение детородной функции происходит на фоне снижения общего уровня женских гормонов.
- Химиотерапия: разрушающее действие на злокачественные и доброкачественные клетки угнетает организм и вызывает гормональный сбой.
Возможные последствия и осложнения
Если эстрогены секретируются в недостаточном объёме, терапия отсутствует, развиваются патологические состояния:
- ожирение;
- разрушение костей;
- тромбоз;
- бесплодие;
- мастопатия;
- новообразования в груди;
- нарушения метаболизма;
- патологии щитовидки;
- психические и нервные расстройства;
- кисты яичников;
- расстройства цикла месячных.
При избытке эстрогена также растет вес, ухудшается состояние кожи, увеличивается чувствительность груди, повышается давление. Страдает сон, работа ЖКТ, психоэмоциональный фон.
Основная задача эстрогенов – обеспечить женщине возможность забеременеть и выносить плод. Также именно благодаря этому гормону у девочек формируется типично женская фигура, более тонкая и эластичная кожа, чем у мужчин, нет волос в области груди и живота. При переизбытке или дефиците всех фракций эстрогена нарушается гормональный фон, что чревато осложнениями для здоровья и трудностями в зачатии и вынашивании плода.
Содержание гормонов в организме после менструации
После менструации уровень эстрогена постепенно увеличивается, что помогает расти эндометрию в матке. Постепенно нормализуется общее состояние женщины.
Основные симптомы, характеризующие состояние женщины после менструации:
- нормализация настроения — устанавливается правильный баланс гормонов;
- улучшение состояния кожи — прогестерон вырабатывается не так активно;
- появление энергии и увеличение работоспособности — является следствием увеличения эстрогена.
Интересно! Эстроген считается гормоном женской красоты. Он делает женщину женщиной и стимулирует ее сексуальность.
Отметим, что в этот период женщина выглядит наиболее привлекательно.