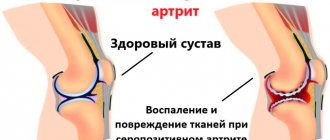
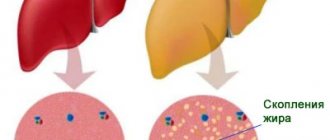
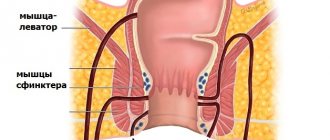
Ахалазия кардии (ахалазия пищевода) — заболевание характеризующиеся отсутствием открытия нижнего пищеводного сфинктера в ответ на прохождения пищи или жидкости по пищеводу, вследствие нарушения проведения нервного импульса к мышцам пищевода и кардии. Необходимо сразу пояснить как правильно называется заболевание, потому что люди называют и ахалазия кардии и ахалазия пищевода. Раньше некоторые врачи считали, что правильно говорить ахалазия пищевода, но международная классификация болезней 10 пересмотра поставила точку в этих спорах, в ней указано ахалазия кардии, а значит это и есть правильное название этой болезни Ахалазия поражает одинаково часто как мужчин, так и женщин, чаще всего в возрасте 30 — 45 лет. Встречается это заболевание в 3 — 20% всех заболеваний пищевода. Раньше считалось, что ахалазия встречается у 1 человека на 100000 населения, но с улучшением диагностики и накоплением данных, стали появляться сообщения, что она встречается с частотой 5 и некоторые авторы считают, что даже 10 человек на 100000 населения
Причина возникновения ахалазии кардии
Сразу необходимо сказать, что достоверно причина ахалазии кардии не известна. Существую различные теории возникновения этого заболевания. Генетическая теория основывается на том, что у пациентов с ахалазией пищевода находят изменения в одних и тех же локусах генов, кроме того риск заболевания ахалазией у детей с синдромом Дауна выше в 200 раз, чем в популяции Инфекционная гипотеза — основывается на том, что при инфицировании Trypanosoma cruzi, которая вызывает болезнь Чагаса, также наблюдается дисфагия, по своему механизму похожая на ахалазию кардии. Кроме того рассматривается возможность развития ахалазии на фоне инфицирования вирусом Herpes zoster и вирусом кори Аутоимунная теоррия — основывается на том, что у пациентом с ахалазией пищевода часто встречаются аутоимунные заболевания. Так у пациентов с ахалазией кардии, риск развития таких заболеваний как увеличивается: сахарного диабета 1-го типа в 5,4 раза, гипотиреоза в 8,5 раза, синдрома Шегрена в 37 раз, системной красной волчанки в 43 раза, увеита в 259 раз. Но не одна из этих теорий, на сегодняшний день не получила убедительных подтверждений, поэтому нельзя говорит о том что известна причина этого заболевания
Что способствует заболеванию ахалазией
Конкретную причину, вызывающую развитие заболевания, специалисты не называют. Связывают его с инфекциями, сдавливанием пищевода, воспалениями, опухолями злокачественного происхождения, инфильтративными поражениями и т.д. В детском возрасте ахалазию пищевода обнаруживают обычно после пяти лет.
Первые проявления заболевания остаются незамеченными, поэтому диагностируется оно с опозданием. Если у ребенка дисфагия и после приема пищи у него начинается рвота, необходимо бить тревогу. Это распространенные симптомы, характерные для ахалазии.
Классификация ахалазии кардии
Классификация ахалазии кардии важна, так как в зависимости от степени заболевания, принимается решение о выборе той или иной тактики лечения. Всего различают 4 стадии:
I стадия (ранняя) — преходящие нарушения прохождения пищи, диаметр и перистальтика пищевода вне приступа не изменены ; II стадия — устойчивое нарушение прохождения пищи, перистальтика пищевода усилена, пищевод не значительно расширен; III стадия – выявляется стриктура кардиального отдела пищевода, последний значительно расширен, перистальтика вялая, поверхностная. В пищеводе натощак имеется жидкость; IV стадия – стадия осложнений с изъязвлениями и эрозиями пищевода. Последний расширен до 10 см, S образно изогнут, перистальтика либо отсутствует полностью, либо разнонаправленная, поверхностная.
Лечение
На начальном этапе, когда проблемы с глотанием незначительны, может быть использована консервативная терапия; используемые препараты направлены на устранение спазма и облегчение состояния пациента. Для расширения суженного участка в пищеводе может также выполняться эндоскопическое бужирование. Для получения результата потребуется несколько процедур, но эффект от дилатации непродолжительный.
Весьма эффективным способом лечения ахалазии пищевода является эзофагомиотомия — хирургическое вмешательство, в ходе которого часть стенки пищевода рассекается, но лишь до подслизистого слоя — без вскрытия просвета, таким образом возможно восстановление нормального глотания. При наличии противопоказаний к оперативному лечению, а также пожилым пациентам с рецидивом болезни, которые ранее уже перенесли операцию, показана эндоскопическая дилатация.
Если есть противопоказания к хирургическому вмешательству и к эндоскопической кардиодилятации, возможно эндоскопическое введение интрасфинктерной инъекции ботулотоксина А. Процедура безопасна, подходит даже пациентам с тяжелыми заболеваниями сердечно-сосудистой и дыхательной систем. Но эффект длится лишь 2-3 месяца, поэтому могут потребоваться неоднократные процедуры.
В нашей клинике для каждого пациента подбирается методика, которая окажется наиболее эффективной именно в его случае. Если в зоне сужения отсутствуют следы от выполненной в прошлом кардиодилатации, также нет истощения мышечной стенки пищевода, рекомендована операция; ее своевременное проведение приводит к выздоровлению. Хирургическое вмешательство выполняется методом лапароскопии и даже при растянутой стенке пищевода приводит к хорошим результатам.
При этом сама операция выполняется с использованием видеоэндоскопического оборудования, позволяющего хирургу выполнять все манипуляции с максимальной точностью, исключая повреждения расположенных в этой зоне структур (сосуды, нервы, фасциальные пространства). Наши специалисты усовершенствовали методику, поэтому пациенты могут рассчитывать не только на более короткий период восстановления, нам удалось свести к минимуму случаи интраоперационных осложнений и рецидивов. На сегодняшний день этот показатель не превышает 0,2%.
Клиническая картина ахалазии кардии
Чаще всего опытному гастроэнтерологу или хирургу не составит труда заподозрить ахалазию пищевода по жалобам пациента. Чаще всего пациенты жалуются на дисфагию, затруднение или полная невозможность прохождения пищи по пищеводу. Часто возникает так называемая парадоксальная дисфагия. когда твердая пища проходит легче чем жидкая. Со временем дисфагия прогрессирует и в особо тяжелых случаях пациенты теряют возможность питаться через рот, что приводит их к истощению. Частым симптомом ахалазии кардии является так называемый симптом мокрой подушки, когда у пациента появляется заброс содержимого расширенного пищевода в рот, и если человек спит то содержимое вытекает на подушку, это может быть как мокрота так и остатки пищи. Часто боли усиливаются на фоне стрессовых ситуаций, либо когда пациент нервничает, что нередко приводит пациентов с ахалазией кардии на прием к психиатру, вместо хирурга.
Нередко данное заболевание сопровождается достаточно интенсивными болями. В начале заболевания боли спастического характера, приступообразные, по мере прогрессирования заболевания боли становятся менее интенсивными, но практически постоянными.
Еще одним частым симптомом ахалазии кардии является регургитация, это заброс содержимого расширенного пищевода в рот, так называемая пищеводная рвота. Это состояние на самом деле напоминает рвоту, но в отличии от нее пациент не испытывает тошноты, и возникает она чаще всего при наклонах или в положении лежа.
Нередким симптомом ахалазии пищевода также является кашель, и развитие бронхитов, а иногда и воспаления легких. Проблема в том что во время регургитации агрессивное и инфицированное содержимое попадает в дыхательные пути, что и вызывает вышеуказанные осложнения.
Часто встречающиеся симптомы
В симптоматике ахалазии главной считается дисфагия, встречающаяся почти у всех заболевших. Время между появлением первых симптомов и визитом к доктору может составлять от одного до десяти лет. Второй по распространенности признак – застойные явления в пищеводе. Проявляется кашлем и приступами удушья ночью.
Изжога и болезненные ощущения в грудной клетке также могут быть признаками ахалазии. Локализуясь в основном за грудиной, сжимающие или сдавливающие боли ощущаются в нижней челюсти, шее и спине. Нередко ахалазию ошибочно принимают за желудочно-пищеводный рефлюкс или другое заболевание, сопровождающееся изжогой. Если она возникает не от еды и не проходит после употребления антацидных препаратов, есть вероятность, что проблема имеет отношение к ахалазии пищевода.
Диагностика ахалазии кардии
Диагностика ахалазии кардии чаще всего не составляет большого труда. ФГДС (гастроскопия) — необходимо начинать обследование именно с этой процедуры. При выполнении ФГДС выявляется сужение пищевода в месте его впадения в желудок, эндоскопически аппарат проходит в желудок с усилием. При ахалазии 3 и 4 степени, пищевод расширен, содержит натощак остатки пищи, нередко выявляются язвы и эрозии пищевода.
Рентгенография пищевода с барием — позволяет оценить скорость прохождения контраста по пищеводу у пациентов с ахалазией пищевода. Также оценивается поперечный размер пищевода, перистальтика, и наличие изгибов. Именно на основании рентгенографии выставляется степень ахалазии кардии.
КТ исследование — выполняется для оценки наличия или отсутствия воспаления в окружающих тканях, наличие бронхита или пневмонии Моторика пищевода — считается “золотым стандартом” диагностики ахалазии кардии, однако оборудование для его выполнения крайне дорогостоящее, и при этом его применение достаточно ограничено. В связи с этим такое оборудование имеет несколько клиник, в основном научно исследовательских.
Какие бывают осложнения
При ахалазии во всем организме происходят необратимые изменения. Среди наиболее распространенных осложнений, связанных с заболеванием пищевода, называют:
- рак плоскоклеточный;
- безоары;
- объемные образования на шее;
- отслаивающийся подслизистый слой;
- дивертикул дистального отдела;
- варикозное расширение вен;
- заболевание легких;
- перикардит гнойный;
- пневмоперикард и др.
При продолжительном протекании заболевания пищевод расширяется, истончаются его стенки, что и становится причиной осложнений. У страдающих ахалазией в большинстве случаев (85%) отмечают заметное снижение веса.
Комментарий врача
Если симптомы, характерные для ахалазии кардии, доставляют физические и психологические страдания, у вас есть возможность избавиться от заболевания быстро и безболезненно, заодно отказавшись от множества медикаментов, приносящих лишь временное облегчение. Существует несколько способов лечения данного заболевания, мы подберем вам именно тот, который окажется эффективным в вашем случае. Малотравматичная операция проводится с помощью эндоскопического оборудования, что позволяет выполнять все манипуляции максимально деликатно. Более того, усовершенствованная методика позволяет проводить хирургическое вмешательство без риска развития рецидивов в дальнейшем. Не дожидайтесь развития осложнений и не тратьте напрасно времени на малоэффективную консервативную терапию, своевременное лечение дает все шансы на быстрое восстановление!
Руководитель хирургической службы SwissClinic Пучков Константин Викторович
Модифицированная лапароскопическая кардиомиотомия – максимальный эффект при минимальном риске
Профессор Константин Викторович Пучков, возглавляющий Швейцарскую университетскую клинику в Москве – один из лучших хирургов Европы, блестящий специалист в области классической и лапароскопической хирургии с 25-тысячным опытом операций усовершенствовал методику Геллера. Принципиальные отличия его модификации:
- малоинвазивная операция через несколько проколов-разрезов брюшной стенки длиной 5-10 мм;
- тщательная ревизия дна разреза пищевода и ушивание микроповреждений атравматичными иглами рассасывающимся шовным материалом;
- дублирование дна разреза пищевода, передней стенкой желудка, подшивающейся по всему периметру дефекта. Этот этап операции очень сложен, поэтому большинством хирургов не практикуется. Но профессор К.В. Пучков выполняет его всегда, тем самым минимизируя риск осложнений и рецидива болезни;
- максимальное сохранение анатомического взаиморасположения пищевода, желудка и диафрагмы;
- усиление кардиального сфинктера пищевода фундопликацией на 120о. Так называют складку-манжету, формирующуюся из дна желудка, препятствующую недостаточности сфинктера и рефлюксу (забросу) содержимого желудка в пищевод;
- применение электрохирургических инструментов на платформе «LigaSure», позволяющих работать бескровно, точно и максимально щадяще для тканей;
- использование современных противоспаечных средств для профилактики спаечной болезни;
- послеоперационный период без установки желудочного зонда. Самостоятельный прием жидкой пищи уже на следующий день.
Профессор К.В. Пучков убежден, что к хирургическому лечению следует прибегать, не теряя времени на малоэффективные и небезопасные консервативные методы.
Имея специализации и огромный практический опыт в области оперативной онкологии, гинекологии, урологии, колопроктологии, профессор К.В. Пучков часто выполняет симультанные (сочетанные) операции. Они позволяют в процессе одного вмешательства и однократной анестезии провести хирургическое лечение других заболеваний брюшной полости и малого таза, помимо ахалазии кардии. Это избавляет пациентов от необходимости оперироваться последовательно с интервалом в 1-1,5 месяца, каждый раз проходя предоперационное обследование, перенося наркоз и период послеоперационного восстановления.
Профессор К.В. Пучков всегда сам отвечает на дистанционно поступающие к нему вопросы пациентов. Ежедневно он уделяет такому общению несколько часов, несмотря на регулярные операции в Москве, Женеве, Фрайбурге и других городах мира, многочисленные мастер-классы в России и за рубежом, руководство Швейцарской университетской клиникой и профильными кафедрами в Академии постдипломного образования врачей.
Все запросы, поступившие через формы заявки или консультанта в нашем чате, мы передаем профессору К.В. Пучкову. Вы можете получить у него детальные рекомендации или второе мнение по поводу предложенной другими докторами тактики лечения ахалазии кардии, согласовать время проведения удаленной видео-консультации или очного приема в Москве.
Ахалазия кардии — нервно-мышечное заболевание пищевода (НМЗП), характеризующееся отсутствием рефлекторного раскрытия кардии при глотании, сопровождающееся нарушением перистальтики и снижением тонуса грудного отдела пищевода [1—4]. Вместе с диффузным эзофагоспазмом и другими моторными расстройствами ее относят в группу нейромышечных заболеваний пищевода [5].
Впервые это заболевание описал английский врач T. Willis в 1672 г. у пациента с постоянной прогрессировавшей рвотой; восстановить проходимость пищевода у него удалось с помощью губки, насаженной на китовый ус [5—7].
Распространенность ахалазии кардии, по данным мировой статистики [7—9], составляет 0,6—2 случая на 100 000 населения (вне зависимости от пола), в США — 1 случай на 100 000 населения. Доля ахалазии пищевода в структуре всех заболеваний этого органа равна 3—20%.
За все время было принято более 25 классификаций ахалазии кардии [10—13], например классификация Т.А. Суворовой (1966), в которой выделено два типа ахалазии пищевода. Трехстадийная классификация кардиоспазма была предложена Г.Д. Вилявиным в 1978 г. В 1987 г. классификация Т.А. Суворовой была изменена и дополнена А.Л. Гребеневым [7]. В нашей стране наиболее распространена классификация Б.В. Петровского (1962), согласно которой различают четыре стадии: I (начальная) — пищевод не расширен, рефлекс раскрытия кардии сохранен, но моторика пищевода усилена и дискоординирована; II — рефлекс раскрытия кардии отсутствует, отмечается расширение пищевода до 4—5 см; III — значительное расширение пищевода до 6—8 см, задержка в нем жидкости и пищи, отсутствие пропульсивной моторики; IV — резкое расширение (более 8 см), удлинение и s-образное искривление пищевода с атонией стенок, длительной задержкой жидкости и пищи [2, 5, 7, 12]. Эта классификация основывается на результатах рентгенологических и эндоскопических методов исследования.
При рентгеноконтрастном исследовании пищевода типичными признаками ахалазии кардии являются расширение просвета пищевода, отсутствие газового пузыря желудка, замедленное освобождение пищевода от контрастного вещества, отсутствие нормальных перистальтических сокращений пищевода, сужение терминального отдела пищевода («пламя свечи») [9, 10].
При эндоскопическом исследовании в первую очередь обращают внимание на степень дилатации просвета пищевода, наличие в нем остатков пищи, жидкости и слизи. Одновременно оценивают состояние слизистой оболочки пищевода, ее толщину, цвет, блеск, определяют наличие перистальтики. Типичные признаки при эзофагогастродуоденоскопии: ослабление перистальтики пищевода, отсутствие адекватного расслабления нижнего пищеводного сфинктера (НПС), сужение пищевода в области НПС и его супрастенотическое расширение; незначительное сопротивление при проведении эндоскопа через НПС [14, 15]. В случае присоединения эзофагита наблюдаются утолщение складок, гиперемия слизистой оболочки, эрозии и изъязвления.
В настоящее время в мире общепринята Чикагская классификация нарушений моторики пищевода, впервые предложенная в 2008 г. и пересмотренная в 2011 и 2014 гг. (СС v3.0) [4, 16—18]. Эта классификация основывается на интерпретации объективных данных, регистрируемых при манометрии высокого разрешения (High-Resolution Manometry — HRM). HRM сегодня является общепринятым стандартом диагностики моторной функции пищевода.
Согласно данной классификации выделяют три типа ахалазии в зависимости от преобладания тех или иных моторных нарушений пищевода, таких как гипертензия НПС, диффузный спазм пищевода, неспецифическая или неэффективная моторика пищевода (см. рисунок).
Манометрическая картина ахалазии кардии. a — type I; b — type II; c — type III. При I типе ахалазии кардии (классическая ахалазия) в 100% влажных глотков отсутствует любая перистальтика грудного отдела пищевода — это выраженная гипокинезия. При II типе отсутствует нормальная перистальтическая волна сокращения, однако наблюдается равномерное спастическое сокращение умеренной интенсивности (>30 мм рт.ст.) по всей длине пищевода от верхнего до НПС более чем в 20% влажных глотков. При этом типе сохранена перистальтика грудного отдела пищевода. Тип III характеризуется отсутствием нормальной перистальтической волны, наличием отдельных эпизодов перистальтики в дистальном отделе пищевода или преждевременными спастическими сокращениями (дистальный эзофагоспазм), зарегистрированными более чем в 20% влажных глотков — это гиперкинетический тип ахалазии кардии. При нем нерасслабление НПС сопровождается чрезвычайно мощным сокращением грудного отдела пищевода [4, 19—21].
Клинические проявления ахалазии кардии чаще всего наблюдают в возрасте от 20 до 40 лет [1, 5, 7]. Основные симптомы заболевания — прогрессирующая дисфагия, регургитация и загрудинная боль, связанная с неполным опорожнением пищевода и хроническим эзофагитом [22—24]. Среди других симптомов заболевания отмечаются похудание, икота, тошнота, повышение слюноотделения, неприятный запах изо рта, изредка изжога [9].
Пациенты с ахалазией кардии могут испытывать вышеперечисленные клинические симптомы длительное время, симптомы могут носить волнообразный характер. Периоды усиления клинических проявлений могут резко сменяться периодами удовлетворительного самочувствия.
Несмотря на то что ахалазия кардии является относительно редкой болезнью, она несет риск тяжелых последствий, таких как, например, аденокарцинома пищевода [11, 25, 26]. Ахалазия кардии, по мнению разных авторов [25, 27], может быть отнесена к предраковым заболеваниям, поскольку известно, что рак развивается у 3—8% больных с кардиоспазмом и ахалазией кардии и вероятность его возникновения возрастает с увеличением продолжительности заболевания, причем не только в кардии, но и в измененном пищеводе. В связи с этим необходимо ее своевременное выявление и лечение.
Консервативное лечение при ахалазии кардии включает медикаментозную терапию с коррекцией диеты [7, 12]. Фармакологическая терапия как самостоятельный метод является наименее эффективным, редко приводит к долгосрочным и стойким положительным результатам, не уменьшает проявление симптомов и часто сопровождается побочными эффектами, поэтому сейчас ему уделяется меньше внимания, чем остальным методам лечения [3, 28].
На протяжении последних 40—50 лет на начальном этапе лечения больных ахалазией кардии считалось целесообразным использовать неоперативные методы, и основным и наиболее доступным из них всегда была ступенчатая баллонная пневматическая дилатация (ПД) под рентгеноскопическим контролем [7, 12].
После дилатации и для мониторирования состояния после лечения, которое необходимо проводить 1 раз в год, жалобы пациентов могут быть оценены по шкале Eckardt (см. таблицу)
Шкала Eckardt Примечание. * 0—3 балла — ремиссия, более 4 баллов — неэффективность ПД. [29, 30].
Кроме регрессии клинических проявлений заболевания, прогностическим показателем длительной ремиссии после ПД является достижение давления НПС менее 10 мм рт.ст., измеренного по окончании процедуры. После П.Д. необходимо провести контрольное рентгенологическое исследование пищевода с контрастированием.
В последние годы с развитием эндоскопических технологий многие авторы [7] предлагают воздержаться от применения ПД, для предотвращения образования рубцов в зоне кардиоэзофагеального перехода, что в дальнейшем затрудняет выполнение эндоскопических операций.
Первые сообщения в зарубежной литературе [31] об использовании ботулинового токсина, А для эндоскопического лечения кардиоспазма и ахалазии кардии появились еще в 1994 г. Процедура основана на интрамуральном эндоскопическом введении ботулинового токсина, А в НПС в дозе 80—100 ЕД, при этом 1 мл препарата (20—25 ЕД) вводят в каждый из четырех квадрантов НПС под визуальным контролем. Эффективность терапии составляет около 80% в течение 1-го месяца наблюдения, 70% после 3 мес, 50% через 6 мес и около 40% через 1 год, в связи с чем иногда требуется повторная инъекция [7].
За всю историю лечения больных с НМЗП было разработано более 60 оперативных методик, например операции J. Mikulicz-Radeck, G. Marwedel и W. Wendel, анастомоз пищевода с желудком в модификации Н. Гейровского, С.С. Юдина, Е.Л. Березова и др., которые из-за возникновения частых рецидивов и развития тяжелых послеоперационных осложнений (рефлюкс-эзофагит, стриктура пищевода) в наше время практически не выполняются и представляют лишь исторический интерес [13]. Неудовлетворительные результаты таких операций способствовали поиску новых подходов к хирургическому лечению ахалазии.
Впервые идею миотомии для лечения НМЗП высказал G. Gottstein в 1901 г. [32, 33]. В 1913 г. E. Heller [34] выполнил первую такую операцию и описал ее в своей статье «Внеслизистая кардиопластика при хроническом кардиоспазме с дилатацией пищевода», операция получила всемирное признание и стала основой для большинства выполняемых хирургических вмешательств [32]. Эзофагокардиомиотомия по E. Heller, заключающаяся в рассечении мышечной оболочки нижнего конца расширенного сегмента пищевода и кардиальной части желудка по передней и задней стенкам, в 15% наблюдений осложнялась развитием гастроэзофагеальной рефлюксной болезни [7].
Предложено множество модификаций, например разработанная в РНЦХ РАМН органосохраняющая кардиопластическая операция, основой которой является эзофагокардиомиотомия по E. Heller с неполной фундопликацией [5]. В связи с тем, что органосохраняющие операции удавалось выполнить не всегда, развитие осложнений в виде рецидивирующего рефлюкс-эзофагита и пептических стриктур пищевода вынуждало производить субтотальную резекцию пищевода с одномоментной эзофагопластикой изоперистальтической желудочной трубкой с анастомозом на шее [35].
Предложенный в 1972 г. Б.В. Петровским метод пластики пищеводно-желудочного перехода лоскутом диафрагмы на питающей ножке из левостороннего трансторакального доступа часто приводил к рецидиву дисфагии, обусловленному развитием «рубцового блока» вокруг пищевода и тяжелым пептическим рефлюкс-эзофагитом [36]. Во избежание нежелательных осложнений ученики Б.В. Петровского — А.Ф. Черноусов и Э.Н. Ванцян предложили пневматическую ступенчатую кардиодилатацию (как основной метод лечения ахалазии кардии I—II стадии), а у больных со II и III стадиями ахалазии кардии — органосохраняющую кардиопластическую операцию, в основе которой лежит модифицированная кардиомиотомия по E. Heller с неполной фундопликацией, позволяющей предотвратить рефлюкс-эзофагит и формирование пищеводного дивертикула [37]. Тем не менее после этой операции у некоторых больных может развиться резидуальная дисфагия, связанная с «гиперфункцией» фундопликационного клапана.
Прогресс в лечении ахалазии кардии связан с внедрением лапароскопии и торакоскопии в клиническую практику. Лапароскопические методы в современной хирургии заняли одно из ведущих мест в помощи больным НМЗП [2, 38]. По эффективности минимально инвазивные вмешательства не уступают открытым хирургическим операциям — 94 и 84% соответственно, а частота послеоперационных осложнений ниже при их выполнении [7].
Метаанализ результатов лечения больных ахалазией кардии, выполненный W. Hoogerwerf и P. Pasricha [39] в 2002 г., показал наибольшую эффективность лапароскопической миотомии среди всех методов лечения этого заболевания.
В терминальной стадии заболевания выполняют экстирпацию или субтотальную резекцию пищевода с одномоментной пластикой желудочной трубкой, в том числе с применением лапаро- и торакоскопической техники [40]. Показания к выбору метода оперативного вмешательства определяют индивидуально [41]. В то же время у пациентов при наличии противопоказаний для радикальной операции возможны органосохраняющие методики [42].
Активное развитие миниинвазивной внутрипросветной эндоскопической хирургии привело к созданию на основе двух методик — миотомии и эндоскопической диссекции в подслизистом слое — нового миниинвазивного метода лечения ахалазии кардии — пероральной эндоскопической миотомии (ПOЭM). С 2000-х годов подслизистый слой желудочно-кишечного тракта стал рабочим пространством для оперативной эндоскопии [43]. Следующим шагом, позволившим приблизиться к ПОЭМ, была разработка метода транслюминальной эндоскопической хирургии (Natural Orifice Translumenal Endoscopic Surgery (NOTES) — внутрипросветная эндоскопическая хирургия через естественные отверстия) — выхода из стенки желудочно-кишечного тракта с помощью туннельного смещения точки входа для безопасного выхода в полость тела, в этом случае вышележащий слизистый лоскут служил заслонкой в качестве защитного герметика [44]. Данная методика основана на формировании подслизистого тоннеля с доступом из просвета пищевода через небольшой разрез слизистой оболочки его грудного отдела в зону повышенного мышечного тонуса и последующим рассечением циркулярных мышечных волокон дистального отдела пищевода, НПС и кардиального отдела желудка [45, 46].
В 2007 г. P. Pasricha и соавт. [47] предложили и успешно апробировали в эксперименте на животных технику эндоскопической миотомии — при контрольной манометрии в результате операции выявлено значительное снижение давления в области НПС, а при наблюдении в течение 7 дней признаков перитонита и медиастинита не отмечено. Дальнейшие исследования [48] показали, что влияние на давление НПС было сопоставимо с любым из ранее применяемых методов лечения ахалазии кардии.
У человека методику эндоскопической миотомии впервые разработал и выполнил в 2008 г. H. Inoue с коллегами (Иокогама, Япония). Он же предложил название новой методике: ПОЭМ [45]. На начальном этапе ПОЭМ была выполнена 17 больным ахалазией кардии. Методика заключалась в создании длинного подслизистого тоннеля (средняя длина около 10—12 см), последующей эндоскопической миотомией циркулярных мышечных волокон длиной 8 см (6 см в дистальном отделе пищевода и 2 см в кардиальном отделе желудка). В результате у всех больных купированы симптомы дисфагии и давление покоя нижнего пищеводного сфинктера уменьшилось в среднем с 52,4 до 19,9 мм рт.ст. [49].
В настоящее время ПОЭМ применяется у всех пациентов с симптоматической ахалазией всех типов [50]. Первоначально использование ПОЭМ было ограничено у пациентов младше 18 лет, но теперь оно успешно применяется в том числе и у больных в возрасте от 3 лет [51].
Результаты первых операций методом ПОЭМ, говорят о том, что новая методика может быть эффективной и являться альтернативой для лечения ахалазии кардии классическими методами, однако ее роль у больных с предшествующими операциями, возрастными ограничениями и сопутствующими заболеваниями пока полностью не изучена [52].
Главные преимущества данной методики заключаются в отсутствии риска неконтролируемой перфорации пищевода, миниинвазивности и малой травматичности хирургической операции, сохранении связочного аппарата пищевода, коротких сроках восстановления и реабилитации [53].
В 2015 г. H. Inoue [54] опубликовал отчет о самом крупном в настоящий момент опыте применения ПОЭМ — 500 больным ахалазией кардии, при этом получены следующие результаты: эндоскопическая миотомия успешно выполнена всем больным, побочные эффекты операции отмечены в 3,2% наблюдений, через 2 мес после ПОЭМ при анкетировании пациентов зафиксировано значительное уменьшение баллов по шкале Eckardt — с 6 до 1 балла, давление НПС в среднем с 25 мм рт. ст. до операции снизилось до 13 мм рт. ст. Гастроэзофагеальная рефлюксная болезнь выявлена у 16,8% пациентов. Был завершен набор в рандомизированное контролируемое исследование, сравнивающее эндоскопическую и лапароскопическую миотомию при ахалазии. Он включает 240 пациентов из Чехии, Германии, Италии, Нидерландов и Швеции. Предполагаемая дата завершения исследования — декабрь 2021 г. В настоящий момент существует несколько систематических обзоров и результатов метаанализа, основанных на ретроспективных данных, опубликованных в последние годы. R. Talukdar и соавт. [46] пришли к выводу, что между ПОЭМ и лапароскопической миотомией нет различий по шкале Eckardt. Однако отмечено, что длительность операции значительно сокращалась при ПОЭМ.
Клиника Майо (Рочестер, США) в 2021 г. поделилась опытом успешного лечения 28 пациентов в период с апреля 2012 г. по май 2015 г. комбинированным методом, который включал в себя ПОЭМ и ПОЭМ, дополненный лапароскопической миотомией по E. Heller с неполной фундопликацией. Авторы отметили снижение баллов по шкале Eckardt с 6 до 0, и лишь 3 пациентов продолжали жаловаться на дисфагию в послеоперационном периоде [55].
L. Marano и соавт. [56] систематически анализировал данные 486 пациентов (196 в группе ПОЭМ и 290 в группе лапароскопической миотомии). Исследование показало, что разница в послеоперационных клинических проявлениях, продолжительности операции и побочных эффектах не достоверна. Продолжительность пребывания пациентов в стационаре была значительно короче при ПОЭМ.
В России ПОЭМ только начинает активно внедряется в клиническую практику, данные о его применения крайне малочисленны. В 2015 г. Е.Д. Федоров [2] привел результаты применения ПОЭМ у 4 больных ахалазией кардии и сделал вывод о непосредственной эффективности и относительной безопасности данного метода в ранние сроки. В 2021 г. К.В. Шишин опубликовал результаты успешного применения метода у 15 больных ахалазией кардии, свидетельствовавшие об его эффективности и безопасности.
Несмотря на положительные отзывы о новом методе лечения больных ахалазией кардии, имеется ряд проблем и вопросов, касающихся особенностей операции [57]. В процессе выполнения ПОЭМ должны быть решены такие технические аспекты, как выбор уровня доступа в пищеводе для формирования подслизистого тоннеля, идентификация НПС в сформированном тоннеле, протяженность миотомии, вопрос полнослойности миотомии — ограничиться только рассечением внутреннего циркулярного слоя или выполнять миотомию и наружных продольных мышечных волокон [58].
Таким образом, совершенствование технических аспектов, появление миниинвазивной оперативной методики ПОЭМ, разработка показаний и противопоказаний к этому, оценка непосредственных и отдаленных результатов вмешательства является перспективным направлением для дальнейших научных исследований.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare n conflicts of interest.
Сведения об авторах
Гасанов А.М
. — https://orcid.org/0000-0002-1994-2052
Алиев Н.А
. — https://orcid.org/0000-0002-9772-1351
Даниелян Ш.Н
. — https://orcid.org/0000-0001-6217-387Х; e-mail
Gasanov A.M.
— https://orcid.org/0000-0002-1994-2052
Aliev N.A.
— https://orcid.org/0000-0002-9772-1351
Danielyan Sh.N.
— https://orcid.org/0000-0001-6217-387Х
Преимущества лечения в Швейцарской Университетской клинике
- Клиника оснащена оборудованием последнего поколения, что позволяет проводить операцию, не повреждая рядом расположенные структуры, мышечная оболочка рассекается без повреждения слизистой, исключены также интраоперационные осложнения и т.п.
- Методика лечения подбирается для каждого пациента индивидуально, с учетом состояния его здоровья. Огромное значение уделяется сохранению естественного анатомического расположения пищевода, диафрагмы и желудка, что позволяет избежать появления рефлюкс-эзофагита и недостаточности сфинктера в дальнейшем.
- При лечении больных в клинике используется методика, благодаря которой после операции нет необходимости оставлять трансгастральный зонд, что облегчает послеоперационное течение. Благодаря используемой авторской методике риск развития рецидива в дальнейшем минимален, у более чем 97% пациентов удалось добиться хороших результатов, подтвержденных фиброэзофагогастродуоденоскопией, рентгенологическим обследованием и эзофагоманометрией.
- В нашей клинике пациентам, имеющим несколько заболеваний, требующих оперативного лечения, может быть проведена симультанная операция. Выполнение нескольких оперативных вмешательств в ходе одной анестезии сокращает нагрузку на организм, время госпитализации, при этом восстановление, по сравнению с обычной операцией, занимает гораздо меньше времени.