Оппортунистические инфекции, включая микозы, представляют собой актуальную проблему современной медицины. Парадоксально, но именно достижения науки, обеспечившие успехи клинической медицины, привели к увеличению числа больных с оппортунистическими микозами. В частности, достижения в лечении ряда онкологических и аутоиммунных заболеваний (применение химиотерапии, антицитокиновой терапии, глюкортикостероидов и иммунодепрессантов) ассоциированы с появлением популяции пациентов с острыми и хроническими ятрогенными иммунодефицитными состояниями. В свою очередь иммунодефициты и локальные нарушения антимикробной резистентности у человека являются основой для развития оппортунистических микозов, в первую очередь кандидоза. Диагностика и лечение кандидоза слизистых оболочек пищеварительного тракта в ряде случаев сопряжены со значительными трудностями.
Грибы (лат. fungus, греч. mykes) – самостоятельное обширное царство эукариотических микроорганизмов, включающее около 90 тыс. изученных видов. До конца 1960-х гг. грибы ошибочно относили к царству растений. Среди грибов различают макрои микромицеты. Первые видны невооруженным глазом, вторые – с помощью микроскопов. Известны одноклеточные (низшие грибы, например, Mucor ) и многоклеточные (высшие грибы, например, Penicillium) формы микромицетов [1].
Дрожжеподобные грибы рода Candida – одноклеточные микроорганизмы размером 6–10 мкм. Эти микромицеты диморфны: в различных условиях они образуют и бластомицеты (клеткипочки), и псевдомицелий (нити удлиненных клеток). Эта морфологическая особенность имеет, как будет показано ниже, важное клиническое значение.
Микромицетам рода Candida присуща убиквотность – повсеместная распространенность в окружающей среде. Жизнеспособные клетки Candida spp. могут быть обнаружены в почве, питьевой воде, пищевых продуктах, на коже и слизистых оболочках человека и животных. Таким образом, контакт с этими микромицетами “открытых систем” человека, т. е. его кожи и слизистых оболочек, – ординарный факт.
Антифунгальная резистентность
Исход контакта с дрожжеподобными грибами рода Candida обусловлен состоянием системы антифунгальной резистентности человека. В большинстве случаев такой контакт представляет собой транзиторное кандидоносительство, когда структуры и механизмы антифунгальной резистентности обеспечивают спонтанную деконтаминацию организма человека. В то же время у лиц с нарушениями в системе антифунгальной резистентности контакт может сформировать как персистирующее носительство, так и кандидоз. Таким образом, кандидоз пищеварительного тракта имеет типичные черты оппортунистической инфекции. Заболевание кандидозом слизистых оболочек предопределено наличием у грибов рода Candida т. н. факторов патогенности.
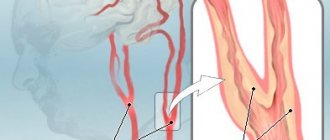
В частности, клетки гриба могут прикрепляться к эпителиоцитам (адгезия), а затем через трансформацию в нитевидную форму (псевдомицелий) внедряться в слизистую оболочку, даже “закрытые” системы (инвазия), и вызывать некроз тканей макроорганизма за счет секреции ферментов – аспартилпротеиназ и фозфолипаз. Перечисленным факторам патогенности естественным образом противостоят многочисленные факторы антифунгальной резистентности. В частности, большое значение имеют целостность эпителиального слоя пищеварительного тракта и мукополисахариды слизи. Защитная роль отводится антагонизму дрожжеподобных грибов и облигатных бактерий пищеварительного тракта, активности пищеварительных ферментов и фунгистатическому действию неспецифических гуморальных факторов, таких как лизоцим, комплемент, секреторный IgA, трансферрин, лактоферрин и др.
Однако решающее значение в системе антифунгальной резистентности имеет функция фагоцитирующих клеток, в первую очередь полиморфноядерных лейкоцитов, и в меньшей степени – мононуклеарных фагоцитов и естественных киллеров. Специфический антифунгальный гуморальный ответ реализуется за счет синтеза Вклетками специфических противокандидозных антител классов IgA, IgM, IgG и в определенной степени – IgE. Наконец, сложная кооперация дендритных и других антигенпрезентирующих клеток, Тхелперов типов 1 и 2, а также Трегуляторных клеток обеспечивает адекватный специфический иммунный ответ.
Как диагностируют заболевание
Визуальные методы диагностики кандидоза. При осмотре выявляются воспаление участков кожи, ограниченное бордюром отслаивающегося, мацерированного эпидермиса, белесоватый налет на слизистых оболочках.
Лабораторная диагностика. Вопреки распространенному мнению, главным методом диагностики кандидоза до сих пор является микроскопия мазка с пораженных участков слизистой. ПЦР (ДНК — диагностика), популярная в последнее время, как правило, плохо подходит для диагностики кандидоза.
Лабораторная диагностика заболевания включает в себя:
- микроскопию мазка выделений
- культуральную диагностику (посев)
- иммуно-ферментный анализ (ИФА)
- полимеразная цепная реакция (ПЦР).
Факторы риска по кандидозу слизистых оболочек
Дефекты в кратко описанной выше системе антифунгальной резистентности являются факторами, способствующими возникновению кандидоза, или т. н. факторами риска. Группы риска по развитию кандидоза пищеварительного тракта представлены ниже: • физиологические иммунодефициты (ранний детский период, старческий возраст, беременность); • генетически детерминированные иммунодефициты (например, селективный дефицит IgA); • ятрогенные иммунодефициты – (например, последствия лечения глюкокортикостероидами, иммунодепрессантами, антицитокиновая, лучевая и полихимиотерапия); • заболевания эндокринной системы (например, сахарный диабет, аутоиммунный полиэндокринный синдром, гипотиреоз); • дисбиоз слизистых оболочек после антибиотикотерапии; • СПИД; • хронические “истощающие” заболевания (например, цирроз печени); • нарушения нутритивного статуса (например, голодание и авитаминозы).
В указанных группах кандидоз выявляют чаще обычного. Отметим, что иногда явную причину нарушения антифунгальной резистентности определить не удается.
Что такое кандидоз пищевода?
Это заболевания, которое вызвано инфекцией грибков рода Candida. Инфекционное поражение грибком внутренних органов, слизистой оболочки и кожи является опасным и при отсутствии должного лечения может привести к серьезным последствиям, а в некоторых случаях и к летальному исходу. Поэтому откладывать визит к врачу при обнаружении симптомов кандидоза пищевода небезопасно.
При первых признаках недуга, обязательно обратитесь в медицинский центр, и запишитесь на прием гастроэнтеролога в ближайшее время. В НЕОМЕД есть квалифицированные специалисты, которые помогут в вашей проблеме.
Патогенез, клиника и диагностика
Развитие кандидоза пищеварительного тракта характеризуется последовательным прохождением грибами следующих этапов: адгезия, инвазия, кандидемия и висцеральные поражения. На первом этапе микромицеты адгезируются к эпителиоцитам какоголибо участка слизистой оболочки. В дальнейшем дефекты в системе резистентности позволяют микромицетам через трансформацию в псевдомицелий внедряться (инвазироваться) в слизистую оболочку и подлежащие ткани. Цитопения – решающий фактор, позволяющий инвазирующимся грибам достигать стенки сосудов, разрушать ее и циркулировать в сосудистом русле (этот этап называют кандидемией). В отсутствие адекватной терапии кандидемия приводит к образованию очагов инвазивного кандидоза в висцеральных органах, чаще –в печени и селезенке, легких, центральной нервной системе.
На первый взгляд парадоксально, но внедрение грибов рода Candida зачастую наблюдается в участках слизистой оболочки, представленной многослойным эпителием (полость рта, пищевод), и значительно реже это происходит в отношении однослойного эпителия (желудок, кишечник).
На практике клиницисту приходится сталкиваться преимущественно с кандидоносительством, частота которого у здоровых лиц достигает в полости рта 25, в кишечнике – до 65–80 % и значительно превышает частоту заболевания. Кандидоз пищевода, например, встречается у больных общего профиля в 1–2 % случаев, у пациентов с сахарным диабетом типа 1 – в 5–10, а у больных СПИДом – в 15–30 % [2].
Симптомы кандидоза в первую очередь характеризуются появлением т. н. молочницы и раздражением слизистых оболочек. Характерными жалобами являются жжение слизистой оболочки языка и полости ротоглотки, дис, одинофагия, ретростернальный дискомфорт, однако встречается и латентное течение. Симптомы кандидоза пищевода могут нарушить акт глотания, что в свою очередь приводит к нарушению питания и значительному снижению качества жизни.
Объем обследования при кандидозе органов пищеварения включает изучение анамнеза и клинической картины, оценку рутинных клинических тестов, эндоскопические исследования, микологические (культуральные, морфологические, серологические) и иммунологические тесты.
Эндоскопические признаки кандидоза – гиперемия и контактная ранимость слизистой оболочки, а также фибринозные налеты различной локализации, конфигурации и размеров. “Стандарт” диагностики кандидоза слизистых оболочек – обнаружение псевдомицелия Candida spp. при морфологическом исследовании биоптатов и соскобов.
С целью обнаружения псевдомицелия используют морфологические микологические методы: цитологический – с окраской мазков по Романовскому–Гимза, гистологический – с окраской биоптатов ШИКреакцией.
Таким образом, учет диморфности микромицетов Candida spp. является ключом к дифференциальному диагнозу между кандидозом и кандидоносительством. В современных условиях клиницист должен требовать от морфолога точного описания морфологических структур гриба, ведь обнаружение отдельных дрожжевых клеток, как правило, свидетельствует о кандидоносительстве, а обнаружение псевдомицелия позволяет подтвердить диагноз кандидоза.
К недостатку морфологических методов можно отнести их ограниченную чувствительность при эндоскопической биопсии. Известно, что биопсионные щипцы позволяют получить для изучения миниатюрный фрагмент ткани и вероятность обнаружения информативного признака при однократной биопсии недостаточна.
Культуральный микологический метод основан на посеве биоматериалов слизистых оболочек на среду Сабуро. Преимущество данного метода состоит в возможности видовой идентификации грибов рода Candida и тестирования культуры на чувствительность к антимикотикам. Актуальность таких исследований обусловлена
тем, что различные виды Candida, в частности C. albicans, C. tropicalis, C. parapsilosis, C. krusei, C. glabrata и др., имеют различную чувствительность к современным антифунгальным препаратам. В настоящее время в арсенале овременных лабораторий имеется несколько диагностических систем для определения видовой принадлежности грибов и их чувствительности к антифунгальным препаратам. В основе видовой идентификации и определения чувствительности к антифунгальным препаратам лежат использование селективных питательных сред, изучение характера утилизации грибами сахаров и энзимный профиль грибов, метод разведений, флуоресцентная гибридизация и др. (диагностические системы Кандиселект, Ауксаколор, Фунгискрин, 60780 Фунгитест и др.). Культуральное исследование биоматериалов слизистых оболочек с определением вида возбудителя становится строго необходимым при рецидивирующем течении кандидоза или резистентности к стандартной антимикотической терапии.
Недостаток культурального метода в невозможности дифференцировать кандидоносительство и кандидоз при исследовании материалов “открытых систем”, поскольку слизистые оболочки и в норме могут быть контаминированными грибами рода Candida.
Чувствительность и специфичность серологических тестов диагностики кандидоза пищевода (иммуноферментный анализ с антигеном Candida, уровень специфического IgE, тест латексагглютинации Platelia) пока не достигли требуемой точности, и их результаты должны оцениваться с известной осторожностью.
В план ведения пациентов с кандидозом пищевода необходимо включить диагностику и коррекцию фоновых заболеваний, других очагов кандидозной инфекции, рациональную антифунгальную терапию и иммунокоррекцию.
В клинике НИИ медицинской микологии СанктПетербургской медицинской академии последипломного образования у пациента с кандидозом обязательно проводится минимальный объем диагностики предполагаемого фонового заболевания, включающий: • уточнение фармакологического анамнеза; • клинический анализ крови; • анализ крови на ВИЧ-инфекцию; • анализ крови на толерантность к глюкозе; • исключение наиболее часто встречающихся злокачественных опухолей и в связи с этим рентгенография легких, фиброгастро, фиброколоноскопия, дополнительно для мужчин – ультразвуковое исследование (УЗИ) предстательной железы, дополнительно для женщин – УЗИ молочных желез и малого таза с консультацией гинеколога.
Лечебные мероприятия
Лечение кандидоза слизистых оболочек основано на применении антифунгальных препаратов. Общий принцип действия всех антифунгальных средств – угнетение биосинтеза эргостерина клеточной стенки микромицетов. В целом антифунгальные средства, используемые для лечения кандидоза, можно разделить на три группы. Первая – полиеновые антимикотики, практически нерезорбируемые при приеме внутрь. К ним относят амфотерицин В, нистатин и натамицин. Вторая – азольные антимикотики, относительно хорошо резорбируемые при пероральном приеме. К ним относятся: кетоконазол, флуконазол (наиболее часто назначаемый при кандидозе), итраконазол, вориконазол, позаконазол. Третья группа – эхинокандины: каспофунгин, анидулафунгин, микафунгин.
Цель лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта – устранение симптомов и клиниколабораторных признаков заболевания, а также предотвращение рецидивов. Современный пересмотр стандартов лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта, опубликованный в США в 2009 г., содержит принципиальные изменения и дополнения по сравнению с аналогичным документом 2004 г. [3].
Большинство случаев орофаринге ального кандидоза и кандидоза пищевода вызваны C. albicans либо как единственным выявленным возбудителем, либо в составе микстинфекции. Однако все чаще встречаются случаи манифестной инфекции, вызванной видами, обычно резистентными к флуконазолу, – C. glabrata и C. krusei.
В США и Европе были проведены многочисленные рандомизированные проспективные исследования течения орофарингеального кандидоза у больных СПИДом и онкологическими заболеваниями, было отмечено, что большинство пациентов отвечают на терапию топическими антимикотиками. Однако также было установлено, что у больных СПИДом рецидивы кандидоза после терапии местно действующими антимикотиками возникают быстрее, чем после терапии флуконазолом, а резистентность к антимикотикам может появиться при всех режимах терапии.
Очевидно, что лечение флуконазолом и итраконазолом в растворе эффективнее, чем лечение кетоконазолом и итраконазолом в капсулах. Для детей в возрасте 5 лет и старше рекомендована доза раствора итраконазола 2,5 мг/кг дважды в сутки, и местный эффект раствора может быть так же важен, как и системный эффект. У больных СПИДом суспензия позаконазола так же эффективна, как и терапия флуконазолом.
Рецидивирующая кандидозная инфекция типична для больных с иммунодефицитом, особенно для больных СПИД. Для предотвращения рецидивов орофарингеального кандидоза долгосрочная поддерживающая терапия флуконазолом достаточно эффективна. Она прошла сравнение по эффективности с эпизодическим применением флуконазола в ответ на рецидив заболевания, и было показано, что продолжительная поддерживающая терапия предотвращает рецидивы кандидоза более эффективно, чем периодическая терапия, но ассоциирована с большим риском развития резистентности возбудителя.
В то же время показано, что для предотвращения рецидивов орофарингеального кандидоза пероральная терапия амфотерицином В, нистатином и капсулами итраконазола менее эффективна, чем лечение флуконазолом.
Согласно рекомендациям, для лечения флуконазолрезистентного кандидоза вначале должен быть назначен раствор итраконазола. Показано, что не менее 64, но не более 80 % пациентов отвечают на такую терапию. Суспензия позаконазола эффективна приблизительно у 74 % больных с рецидивирующим орофарингеальным кандидозом или кандидозом пищевода, а вориконазол может быть эффективным при флуконазолрезистентном кандидозе. Внутривенно вводимые каспофунгин, микафунгин и анидулафунгин могут быть обоснованной альтернативой триазольным антимикотикам. Пероральный или внутривенный амфотерицин В также может быть эффективным у определенной части больных.
Иммуномодуляция с добавлением гранулоцитарномакрофагального колониестимулирующего фактора и препараты интерферона гамма могут быть полезными при рецидивирующем кандидозе полости рта.
Одновременное обнаружение орофарингеального кандидоза и дисфагии или одинофагии может быть свидетельством наличия у пациента кандидоза пищевода. Пробное лечение флуконазолом для таких пациентов с предполагаемым кандидозом пищевода может быть экономически выгодной альтернативой эндоскопическому исследованию: большинство больных кандидозом пищевода отмечают исчезновение жалоб в течение 7 дней после начала терапии. При лечении кандидоза пищевода флуконазол эффективнее, чем кетоконазол, итраконазол в капсулах и флуцитозин, а раствор итраконазола сравним с флуконазолом по эффективности. До 80 % пациентов с флуконазолрезистентным кандидозом отвечают на лечение раствором итраконазола. Вориконазол так же эффективен, как флуконазол, причем его преимущество проявляется при лечении флуконазолрезистентного кандидоза, хотя он ассоциирован с большим числом побочных эффектов.
Для применения эхинокандинов характерна более высокая частота рецидивов кандидоза, чем после лечения флуконазолом. Флуконазолрезистентный кандидоз отвечает на каспофунгин, эффективность которого схожа с таковой при лечении микафунгином и анидулафунгином. У больных СПИДом кандидоз обычно приобретает рецидивирующий характер, и долгосрочная поддерживающая терапия флуконазолом эффективна в плане предупреждения рецидивов. У ВИЧинфицированных пациентов использование ВААРТ (высокоактивной антиретровирусной терапии) ассоциировано с уменьшением степени контаминации слизистых оболочек грибами C. albicans и уменьшением частоты орофарингеального кандидоза. Таким образом, ВААРТ должна быть использована как дополнительная терапия (насколько это возможно) у всех ВИЧинфицированных больных орофарингеальным кандидозом и кандидозом пищевода.
Хронический кандидоз кожи и слизистых оболочек – редко встречающееся заболевание, характеризующееся хроническим персистирующим онихомикозом и поражением слизистых оболочек, вызванными грибами рода Candida. Часть таких больных страдают тимомой или аутоиммунным полиэндокринным синдромом типа 1. Этим пациентам в качестве начальной терапии должен быть назначен флуконазол. Когда имеются распространенные кожные и ногтевые поражения, ответ на антифунгальную терапию может быть замедленным, и почти всегда отмечаются рецидивы. Таким образом, большинство пациентов нуждаются в хронической поддерживающей антифунгальной терапии. Часто встречается развитие флуконазолрезистентного кандидоза. Пациенты с этой формой заболевания должны получать лечение такими терапевтическими схемами, которые используются при флуконазолрезистентности у больных СПИДом.
Лечение орофарингеального кандидоза Для лечения легких случаев: орошения раствором клотримазола в дозе 10 мг 5 раз в сутки или суспензия нистатина местно в концентрации 100 тыс. ЕД/мл в дозе 4–6 мл 4 раза в день, или 1–2 пастилки с нистатином (200 тыс. ЕД каждая), назначаемые 4 раза в день на 7–14 дней. Отметим, что в РФ лекарственные формы нистатина в виде суспензии или пастилок не зарегистрированы.
Для лечения среднетяжелых или тяжелых случаев заболевания: флуконазол перорально в дозе 100–200 мг (3 мг/кг) в сутки на 7–14 дней.
Для лечения флуконазолрезистентных форм заболевания: либо раствор итраконазола в дозе 200 мг/сут или суспензия позаконазола в дозе 400 мг 400 мг дважды в сутки на первые 3 дня, а затем по 400 мг в сутки до 28 дней. В случае неуспеха этих мер рекомендован вориконазол в дозе 200 мг дважды в сутки или по 1 мл оральной суспензии амфотерицина В, назначаемого в дозе 100 мг/мл 4 раза в сутки. Отметим, что в РФ лекарственные формы амфотерицина В в виде оральной суспензии не зарегистрированы.
В случае рефрактерного заболевания также рекомендованы эхинокандины или амфотерицин В внутривенно в дозе 0,3 мг/кг в день. Для больных СПИДом обычно необходима хроническая поддерживающая терапия. В этих случаях рекомендован флуконазол в дозе 100 мг 3 раза в неделю. Для предотвращения рецидивов инфекции рекомендована также ВААРТ.
Для лечения орофарингеального кандидоза, ассоциированного с зубными протезами, в дополнение к антифунгальной терапии рекомендовано проводить дезинфекцию протезов.
Лечение кандидоза пищевода
Во всех случаях требуется терапия системно действующими антимикотиками. Местнодействующие антифунгальные препараты (нистатин, натамицин, клотримазол) не эффективны. Рекомендован флуконазол перорально в дозе 200–400 мг (3–6 мг/кг) в сутки на 14–21 день. Для пациентов, у которых невозможен пероральный прием лекарств, рекомендованы флуконазол внутривенно в дозе 400 мг (6 мг/кг) в сутки или амфотерицин В в дозе 0,3–0,7 мг/кг в сутки, или эхинокандины. Приемлемо диагностическое пробное назначение антифунгальной терапии до выполнения эндоскопического исследования (заметим, что эта рекомендация характерна для США, где стоимость эндоскопического исследования существенно выше стоимости пробного курса антифунгальной терапии).
Для лечения флуконазолрезистентных форм заболевания рекомендованы: раствор итраконазола в дозе 200 мг/сут, суспензия позаконазола в дозе 400 мг дважды в сутки или вориконазол 200 мг дважды в сутки, назначаемый внутривенно или перорально на срок 14–21 день. Приемлемой альтернативой является назначение микафунгина в дозе 150 мг/сут, или каспофунгина 50 мг/сут, или анидулафунгина в дозе 200 мг/сут, или амфотерицина В в дозе 0,3–0,7 мг/кг/сут.
Для лечения рецидивирующего кандидоза пищевода рекомендован флуконазол в дозе 100–200 мг трижды в неделю. Для предотвращения рецидивов инфекции у больных СПИДом рекомендована ВААРТ.
В целом успех лечения кандидоза слизистых оболочек зависит не только от адекватной антифунгальной терапии, но и от успеха коррекции фонового заболевания.
Лечение кандидозного эзофагита
Кандиды под микроскопом
В настоящий момент существует множество методов лечения разнообразных болезней. Данное заболевание характеризуется некими сложностями в лечении. Иногда процесс выздоровления может происходить длительный срок, так как не все методы являются эффективны для одного человека.
Также иногда бывает, что определенные медикаменты или процедуры могут привести к ряду серьезных побочных эффектов. Поэтому врачи с большой осторожностью подходят к лечению Кандидозного эзофагита. Обычно пациент лежит в больнице под наблюдением врача. Ему выписывают ряд медицинских препаратов, назначают специальную диету, а в тяжелых случаях голодовку в течении нескольких дней.
Питание также может происходить через зонд, но это также в уже в осложненных случаях. Диета подразумевает под собой исключение всех продуктов питания, которые могут повредить слизистую оболочку кишечного тракта. К таким относят алкоголь, жирная пища, сладкое, кофе, все острое и горячее. Кроме того, любителям сигарет следует отказаться от вредной привычки на время лечения. Для более эффективного лечения посидите на водичке пару дней или же употребляйте только фрукты и овощи.
Кандидоз кишечника. Симптомы
Нарушения микробиоценоза кишечника с избыточным ростом грибов рода кандид или кандидозный дисбактериоз клинически проявляется бродильной диспепсией, болями в животе, больше в области сигмы, метеоризмом, отмечается частый обильный пенистый жидкий стул со слизью до 6-10 раз в сутки, сопровождается нарушениями витаминного обмена, субфебрильной температурой, выраженной слабостью, головной болью. Нередко наблюдаются симптомы поражения слизистых оболочек в виде стоматита, глоссита, вульвовагинальной молочницы. Грибковая инфекция резко снижает иммунитет, что приводить к более глубокому процессу развития висцерального кандидомикоза с поражением верхних дыхательных путей, легких, мочеполовой и пищеварительной систем. В крови – умеренный лейкоцитоз, ускоренное СОЭ, при сигмоскопии – катаральный геморрагический проктосигмоидит.
Показания к терапии при условии клинического, микробиологического, серологического или гистологического подтверждения кандидозной инфекции, обнаружение кандид с клиническими проявлениями с двух и более поверхностей колонизации грибов.
Кандидоз кишечника. Причины
Считается общепризнанным, что желудочно-кишечный тракт является основным эндогенным резервуаром Candida, откуда происходит последующее распространение инфекции по организму. Candida albicans относится к условно-патогенной флоре и является компонентом нормальной микрофлоры кишечника. Определение в бактериологическом анализе кала наличия Candida albicans в 10х4 степени по официальным требованиям не является показанием для выставления диагноза «кишечный кандидоз» и тем более для противогрибковой терапии. На практике клиницисту приходится сталкиваться с кандидоносительством, которое наблюдается в кишечнике до 80 % и лучше, чтобы Candida находилась ниже уровня определения в анализе (0).
Факторы риска развития кандидозной инфекции разнообразны, они обусловлены и различными заболеваниями органов и систем организма, при которых развиваются признаки нарушенной микрофлоры кишечника, в частности при сахарном диабете, онкопатологии, воспалительных заболеваниях кишечника (болезнь Крона и неспецифический язвенный колит), синдроме раздраженной кишки, анемии, СПИДе, снижении иммунной защиты, стрессах. Проводимая терапия по поводу основных заболеваний также может способствовать развитию нарушений микробиоценоза кишечника и избыточному росту кандид – это применение в лечении цитостатиков, иммуносупрессоров, лучевой терапии, антибиотиков, хирургических вмешательств.
Имеют значение в возникновении избыточного роста грибов рода кандид и физиологические периоды жизни человека, период новорожденности, беременности, менопаузы, старческий возраст, и ухудшение экологических условий, которые снижают антиинфекционную резистентность человека, что приводит к нарушению баланса между нормальной флорой и иммунным ответом организма. (Бурова С.А.,Курбатова И.В.,2006). Все причины, которые были описаны выше, при которых развивается нарушение микробиоценоза желудочно-кишечного тракта, могут привести к кандидозу. Следует выделить наиболее значимые состояния – это операции на желудке, нарушения секреторной и моторных функций желудка и кишечника, дивертикулез тостой кишки, цирроз печени.
Важным представляется для развития дисбиоза желудочно-кишечного тракта нерациональное питание и, в частности, содержащиеся в пище и добавках стероиды, пищевая непереносимость.