Общие сведения
Синдром Эдвардса (заболевание также называют синдром трисомии 18) – это хромосомная болезнь, для которой характерны множественные пороки развития и трисомия 18 хромосомы. Впервые эту болезнь описал Джон Эдвардс в 1960 году. Диагностируется такое заболевание редко – как свидетельствует статистика, в мире оно встречается с частотой 1:5000. Отмечено, что дети с такой патологией чаще рождаются у матерей зрелого возраста. Так, вероятность появления на свет малыша с такой патологией для женщины старше 45 лет составляет 0,7 %. Риск увеличивается, если будущая мать болеет сахарным диабетом. При этом девочки с такой патологией появляются на свет в три раза чаще, чем мальчики.
Болезнь Эдвардса – очень тяжелая патология, при которой выживаемость после года составляет 5–10%. Как диагностируется это заболевание и с чем связано его развитие, речь пойдет в этой статье.
Норма показателя у беременных в I триместре
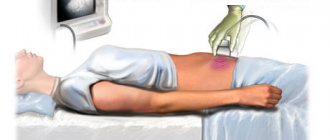
Для выявления генетических нарушений беременным необходимо систематически проходить УЗИ-диагностику. Исследование позволяет определить наличие аномалий еще на ранних сроках.
Во время обследования оцениваются фонометрические показатели. При этом главным критерием является определение толщины воротникового пространства (ТВП). Его нормы составляют 0,7-0,8 мм.
Также изучается строение лицевых структур, черепа, определяются параметры и наличие носовой кости (можно обнаружить уже к 10-й недели беременности). Ближе к 12-й недели ее размеры составляют от 2-х до 3-х мм.
Дополнительно проводятся замеры частоты сердечных сокращений у плода, оценивается кровоток в венозном протоке, поскольку нарушения в нем могут указывать на развитие такой патологии, как синдром Дауна.
Определяющими значениями являются параметры копчико-теменной и бипариетальной области:
| Показатель | Срок беременности | Норма |
| Копчико-теменной размер | 11 неделя | 34-42 мм |
| 12 неделя | 42-51 мм | |
| 13 неделя | 51-63 мм | |
| Носовая кость | 11 неделя | Рассматривается, но не измеряется |
| 12 неделя | 2-3,1 мм | |
| 13 неделя | 2-3,1 мм | |
| Частота сердечных сокращений (ЧСС)/мин. | 11 неделя | 153-165 |
| 12 неделя | 150-162 | |
| 13 неделя | 147-159 | |
| БПР (бипариетальный размер) | 11 неделя | 13-17 мм |
| 12 неделя | 18-21 мм | |
| 13 неделя | 20-24 мм | |
| ЛЗР (лобно-затылочный размер) | 11 неделя | 19-21 мм |
| 12 неделя | 22-24 мм | |
| 13 неделя | 26-29 мм | |
| ХЧГ (нг/мл) | 11 неделя | 17,4-130,4 |
| 12 неделя | 13,4-128,5 | |
| 13 неделя | 14,2-114,7 | |
| PAPP-A (мЕд/л) | 11 неделя | 0,46-3,73 |
| 12 неделя | 0,79-4,76 | |
| 13 неделя | 1,03-6,01 |
Патогенез
Трисомия 18 – это генетическая патология. В каждой человеческой клетке содержится 46 хромосом – это нормальные показатели. Во время оплодотворения по 23 хромосомы женских и мужских половых клеток соединяются и дают в сумме именно такое количество хромосом. Иногда по неизвестным причинам происходят генетические мутации, и в результате появляется лишняя 47 хромосома, дополнительная в 18 паре. Лишняя хромосома у гамет появляется вследствие нерасхождения хромосом при мейотическом делении. В большинстве случаев – в 95% — именно лишняя хромосома становится причиной развития болезни Эдвардса. Но иногда – примерно в 2% случаев – сумма хромосом остается нормальной, но при этом 18 хромосома аномально удлиняется, что приводит к развитию врожденной патологии. Еще в 3% случаев отмечается мозаичная трисомия, при которой дополнительная хромосома присутствует не во всех клетках организма, а только в какой-то его части. Все три формы синдрома протекают по одному типу. Но все же более тяжелое течение отмечается при первой форме болезни.
Цитологическая диагностика
Флюоресцентная гибридизация используется с целью выявления субмикроскопических делеций и дупликаций хромосом, которые являются слишком маленькими для идентификации методами конвенциональной цитогенетики. Ее также используют для идентификации «мягких» транслокаций и маркерных хромосом. РИ8Н-анализ выполняется на препарате метафазных хромосом, выделенных из культивируемых лимфоцитов, амниоцитов, ворсинок хориона, интерфазных ядер из крови, тканей, ворсинок хориона, амниотической жидкости при пренатальном выявлении аномалий развития плода и необходимости скрининга на анеуплоидии (трисомия 21 и т.д.). РИ8Н-анализ применяется с целью преимплантационной генетической диагностики по выявлению сбалансированных транслокаций или делеций. РИ8Н-метод предоставляет информацию по анализу специфической хромосомы или нескольких хромосом, но не выполняется для определения кариотипа.
Классификация
Полная трисомия – если целая дополнительная хромосома появилась на этапе одной клетки, то набор хромосом нарушается в каждой клетке плода. При такой форме у ребенка наблюдаются многочисленные пороки развития, несовместимые с жизнью. Это наиболее тяжелый вариант болезни.
Частичная трисомия – диагностируется, если лишняя хромосома появляется не на самых ранних этапах развития плода. В таком случае нарушение генетического набора отмечается не во всех клетках, и часть из них останутся здоровыми.
Можно ли вылечить хромосомную мутацию?
Хромосомные аномалии не поддаются клиническому излечению. В подавляющем большинстве дети умирают в первые месяцы жизни. При должном уходе и медицинской помощи шансы на продление жизни ребенка возрастают. Однако необходим постоянный контроль, сложные операции и уход за такими пациентами.
Наиболее опасным для жизни ребенка является синдром Дауна. При данном заболевании шансы прожить дольше 30-40 лет в несколько раз выше, чем при других хромосомных аномалиях.
На данный момент вопрос дефектов в хромосомном ряду изучается специалистами, но эффективных методов лечения патологий пока не разработано.
Трисомия в 18, 21 или 13 хромосомном ряду является опасным для жизни ребенка нарушением, поэтому перед зачатием и во время беременности будущей матери следует учитывать все риски развития патологии и проходить систематические исследования для выявления признаков аномалий на ранних этапах.
Причины
Трисомия 18 развивается как следствие наличия дополнительной 18-й хромосомы в кариотипе зиготы. Возникновение этой патологии случайно, и предотвратить его нельзя. Но определяются некоторые факторы риска развития этой патологии:
- Возраст матери – чем старше женщина, тем выше ожидаемый риск трисомии. Вероятность развития болезни Эдвардса увеличивается после 35 лет – с каждым годом частота проявления таких мутаций у ребенка выше.
- Генетическая расположенность – вероятность повышается, если в семье уже были случаи такого заболевания.
- Прием некоторых препаратов, влияющих на деление клеток эмбриона.
- Перенесенные инфекционные заболевания.
- Курение и потребление алкоголя.
Основные причины возникновения хромосомной мутации
На данный момент точные причины развития нарушений изучаются. Однако специалисты выделяют несколько предрасполагающих факторов, которые увеличивают шансы на рождение детей с хромосомными аномалиями.
Трисомия 21.18.13
Возможные причины:
- возраст старше 30 лет (для женщин);
- возраст старше 40 лет (для мужчин);
- наследственный фактор (в роду имеются родственники с генетическими нарушениями в хромосомном ряду);
- проблемы во время предыдущей беременности – замершая беременность, выкидыши, аборты;
- инфекционные заболевания, возникшие в период зачатия ребенка или непосредственно на первых этапах беременности.
Измененное число хромосом (анеуплодия) наблюдается у детей, рожденных женщинами старше 35 лет. При этом риски развития подобных нарушений составляют 1%.
Симптомы
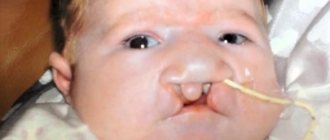
Фото новорожденных c синдромом Эдвардса
Синдром Эдвардса проявляется у плода еще в период внутриутробного развития. В этот период признаки такой патологии могут быть обнаружены в процессе ультразвукового исследования. В ходе такого исследования может быть обнаружена их часть. 9 месяцев беременности – период, на протяжении которого женщина должна проходить УЗИ несколько раз. О синдроме Эдвардса могут свидетельствовать следующие симптомы:
- Существенная задержка внутриутробного развития – она может составлять несколько недель.
- Многоводие.
- Пороки развития головного мозга.
- Одна пупочная артерия у плода.
- Очень слабые шевеления плода.
- Большая длительность беременности – до 42 недель. При этом ребенок рождается с очень маленьким весом.
Признаки синдрома Эдвардса у новорожденных заметны сразу после рождения малыша. Отмечаются такие характерные симптомы:
- Низкая масса тела.
- Низкий лоб, широкий затылок.
- Долихоцефалический череп.
- Ушные раковины недоразвиты, расположены очень низко.
- Короткая верхняя губа, маленький рот, высокое небо.
- «Заячья» губа, «волчья» пасть.
- Патологические изменения опорно-двигательного аппарата – узкий таз, вывихнутые бедра, слишком широкая грудная клетка, косолапость.
- Сросшиеся пальцы на ногах, также они могут быть с перепонками.
- Неровное расположение пальцев.
- Искаженная форма лица.
- Очень маленькая голова.
Отдельно выделяется ряд симптомов, связанных с поражением внутренних органов, а также с нарушением нервно-психического развития:
- Сколиоз, атрофия мышц.
- Косоглазие.
- Нарушения ЦНС: сглаживание извилин мозга, недоразвитый мозжечок и мозолистое тело, умственная отсталость.
- Патологи мочеполовой системы: сегментированная или подковообразная почка, удвоение мочеточников, недоразвитые яичники, крипторхизм у мальчиков, гипертрофия клитора у девочек.
- Патологии органов ЖКТ: атрезия заднего прохода или пищевода, неправильно расположенный кишечник, газоэозофагиальная рефлюксная болезнь, нарушенный сосательный и глотательный рефлекс.
- Паховые и пупочные грыжи.
- Врожденные пороки сердца, крупных сосудов.
Как правило, умственное развитие детей с таким заболеванием соответствует тяжелой степени олигофрении. Однако при мозаичной форме синдрома определенные достижения в умственном развитии у пациентов могут быть.
Какие разновидности бывают?
Патология классифицируется в зависимости от пораженной пары хромосом. Каждая разновидность нарушения имеет свое название, проявления, характеристики и другие отличительные особенности.
Трисомия 13, синдром Патау
Данное нарушение является редким и встречается с одинаковой частотой у обоих полов. При этом риски развития синдрома возрастают с повышением возраста родителей. Определить наличие болезни можно с 9-й недели беременности с помощью ультразвуковой диагностики или анализа крови.
Причины
Трисомия 21, 18, 13 может возникать в результате различных провоцирующих факторов, установить точно который практически невозможно.
На данный момент точные происхождения аномалии неизвестны. Большинство специалистов склоняются к версии случайного генетического нарушения в хромосомных парах. Патология развивается в результате образования дополнительной хромосомы в 13-й паре. Влияние соматических нарушений, инфекционных заболеваний, вредных привычек и других факторов не установлено.
Признаки
Симптомы патологии многообразны и затрагивают множество различных систем и внутренних органов.
Признаки:
- небольшая масса тела – до 2,5 кг;
- асфиксия (удушье);
- аномальное развитие головного мозга;
- дефекты в строении лица и черепа;
- нарушения со стороны центральной нервной системы – гидроцефалия, недоразвитость мозжечка, катаракта, глухота, поражение зрительного нерва;
- врожденные пороки сердца;
- очаговое отсутствие волосяного покрова или кожи;
- измененное строение стопы – отсутствие или наличие пальцев;
- аномалии в мочевыделительной системе;
- пороки развития пищеварительного тракта;
- недоразвитость костно-мышечной системы;
- аномальное строение половой и репродуктивной системы.
Дети с синдромом Пату отстают в развитии (умственная и физическая задержка).
Как выглядят новорожденные
Определить патологию можно по внешнему виду младенца. Для детей с заболеванием характерна небольшая окружность головы, низкий и скошенный лоб, узкие глазные отверстия. Переносица имеет плоскую форму и слегка западает во внутрь черепа.
При этом также отмечается развитие других дефектов лица (волчья пасть, заячья губа). Ушные раковины также подвержены деформации и расположены ниже, чем у здоровых детей.
Прогноз для детей
Прогноз при заболевании неблагоприятный. Более 95% всех новорожденных погибают в первые месяцы после рождения. У оставшегося процента детей наблюдаются тяжелые нарушения психомоторного развития, включая сложные формы идиотии.
Трисомия 18, синдром Эдвардса
Трисомия 18 отличается от нарушений в хромосомных парах 21 и 13. Патология занимает 2-е место среди хромосомных нарушений и характеризуется аномалиями в строении различных внутренних органов и систем.
Согласно статистическим данным заболеванию подвержены в большинстве девочки.
Патология подразделяется на 3 основные формы – полную, частичную и мозаичную.
Причины
Патология возникает в случае образования дополнительной пары хромосом. На данный фактор могут повлиять различные причины. При этом установлена взаимосвязь между частотой развитии нарушения и возраста матери – чем старше женщина, тем больше рисков.
Возможные факторы:
- возраст матери старше 40 лет;
- вредные привычки (курение и алкоголь);
- прием медицинских препаратов (особенно в 1-м триместре беременности);
- инфекционные заболевания половой системы (исследование не проводились);
- радиационное излучение.
В некоторых случаях болезнь развивается в результате генетической предрасположенности.
Указанные факторы являются лишь предположением, поскольку на данный момент точные причины возникновения патологии неизвестны. Считается, что при рождении ребенка с синдромом Эдвардса, риски рождения следующего ребенка со схожими аномалиями составляют 2-3%.
Признаки
При данной патологии беременность протекает с нарушениями. Во время вынашивания ребенка отмечается маловодие, низкая активность плода, небольшие размеры плаценты.
Сам ребенок после рождения имеет различные аномалии в строении систем и внутренних органов.
Признаки:
- низкая масса тела (до 2170 г);
- асфиксия;
- врожденные пороки сердца;
- патологии желудочно-кишечного тракта (грыжи, свищи, атрезии);
- аномалии в мочеполовой системе;
- пороки развития ЦНС – гидроцефалия, гипоплазии, кисты;
- проблемы с глотанием, сосанием, дыханием;
- олигофрения, имбецильность, идиотия.
В большинстве случаев развиваются дополнительные нарушения, вызванные осложнениями патологии.
Как выглядят новорожденные
Внешние признаки болезни характеризуются аномалиями в строении головы, конечностей. Также преобладают кожные признаки.
Внешние признаки:
- долихоцефалия – длинный и узкий череп;
- микроцефалия – несоответствие размеров головы с телом (слишком маленький размер черепа);
- низкое расположение ушей – рельефы хряща мало выражены или полностью отсутствуют, сужение слухового прохода, отсутствие мочки и узелка;
- незаращение мягкого или твердого неба, губы;
- изменение стопы и пальцев ног – аномальная длина пальцев, косолапость, сращение пальцев;
- недоразвитость полового члена и гипертрофические изменения клитора;
- флексорное положение кистей рук.
Также у ребенка с данным синдромом наблюдаются неадекватные эмоциональные реакции, иногда вплоть до полного их отсутствия.
Прогноз для детей
Прогноз при патологии практически всегда неблагоприятный. Около 55% детей с аномалиями не доживают до 3-месячного возраста. До 1 года доживает около 10% новорожденных.
Дети, дожившие до старшего возраста, имеют проблемы со здоровьем и нуждаются в постоянном уходе. Чтобы продлить жизни ребенку, необходимо проводить сложные операции на сердце, почках или других органах. Шансы на полноценную и длительную жизнь у детей с синдромом Эдвардса практически отсутствуют.
Трисомия 21, синдрома Дауна
Трисомия 21, 18 и 13 диагностируется в большинстве случаев у детей, рожденных от родителей, чей возраста старше 40 лет. Среди наиболее распространенных генетических нарушений 1-е место занимает патология 21-го хромосомного ряда.
Синдром Дауна представляет собой генетическое нарушение, которое наблюдается у 1 ребенка среди 700 младенцев.
Патология возникает в результате нерасхождения хромосом в половой клетке мужчины. Однако согласно статистическим данным дополнительная хромосома передается от женщины в 88% случаев, от отца – всего в 8%. В иных случаях аномалия возникает в результате неправильного деления клеток после оплодотворения.
Причины
На данный момент выделяют всего 2 основные причины, по которым происходит развитие болезни. Первой из них считается возраст родителей. Чем он больше, тем выше риски возникновения синдрома.
У родителей в возрасте 35-40 лет риски родить ребенка с генетическим аномалиями составляют 1 к 1000. После 40 лет данные риски значительно возрастают и составляют 1 к 60.
Второй причиной развития нарушения является наследственность. Если в роду есть или были родственники со схожими патологиями, риски развития данного заболевания значительно возрастают. Также болезнь может возникать у детей, рожденных от брака с кровными родственниками.
Считается, что такие факторы, как плохая экологическая обстановка, вредные привычки, радиации не оказывают влияние на рождение детей с синдромом Дауна. Точные механизмы и причины на данный момент устанавливаются.
Признаки
Дети с генетическим отклонением имеют характерные внешние признаки. Определить наличие патологии можно еще на этапах вынашивания ребенка во время УЗИ.
Симптоматика:
- непропорциональные размеры головы по сравнению с остальным телом (слишком маленький размер черепа);
- низкая масса тела при полном сроке вынашивания;
- задержка физического, психического и умственного развития;
- кардиологические нарушения – пороки сердца (сердечная недостаточность), одышка, гипергидроз, наличие шумов;
- расстройства со стороны пищеварительного тракта – непроходимость кишечника, диспепсические расстройства, обструктивные нарушения в области двенадцатиперстной кишки;
- сопутствующие заболевания – болезни глаз, проблемы со слухом, кожные проявления;
- склонность к ожирению, возникновению болезни Альцгеймера, развитию бесплодия.
В первые дни и годы жизни у детей с патологией обнаруживаются различные респираторные и воспалительные заболевания, из-за чего при отсутствии своевременной помощи они погибают.
Как выглядят новорожденные
Трисомия 21, 18, 13 имеет схожие внешние и внутренние признаки, поэтому для постановки точного диагноза требуются дополнительные исследования. Внешне дети с синдромом Дауна имеют значительные отличия от здоровых детей. Таким образом, у них наблюдаются различные дефекты в строении тела, конечностей, головы.
Внешние признаки:
- в профиле лицо ребенка плоское;
- микроцефалия (наблюдается не во всех случаях);
- плоский нос;
- образование кожных складов вокруг задней части шеи;
- узкий разрез глазных щелей (монголоидный тип);
- пятна Брушфильда (белые вкрапления на радужной оболочки глаз);
- приоткрытый рот;
- высунутый язык;
- обезьянья складка на ладонях;
- укороченные пальцы;
- наличие 2-х фаланг на пятом пальце.
Также отмечается укороченная шея, маленькие уши и широкие кисти рук.
У детей наблюдается гипермобильность (подвижность суставов). Связано это с недоразвитостью соединительной ткани.
В редких случаях у некоторых новорожденных присутствуют признаки деформаций грудной клетки и позвоночника.
Прогноз для детей
При заболевании прогноз наиболее благоприятный среди всех хромосомных нарушений. Связывается это с тем, что нарушение имеет не настолько критичные дефекты и аномалии в строении внутренних органов и систем.
Квалифицированная медицинская помощь и уход в первые годы жизни ребенка позволяют сократить риски летальности, так как в этот период времени новорожденный подвержен развитию респираторных заболеваний, к которым предрасположен ребенок с синдромом Дауна.
При правильно организованном уходе за ребенком длительность жизни составляет 40-45 лет.
Анализы и диагностика
Определить синдром трисомии у будущего ребенка можно уже на этапе внутриутробного развития. Если у плода подтверждается такая патология, это считается показанием к прерыванию беременности. Ведь ребенок с таким заболеванием не сможет полноценно жить, а здоровье у него будет ухудшаться с каждым днем. Именно поэтому очень важно диагностировать болезнь как можно раньше.
В настоящее время применяются неинвазивные и инвазивные методы исследования биоматериала.
Неинвазивные методики включают пренатальный скрининг крови женщины. Беременная сдает кровь в период с 11 по 13 неделю вынашивания плода, после чего проводится биохимический анализ крови. Риск развития трисомии определяется по уровню хорионического гонадотропина и плазменного протеина А.
Инвазивные методики позволяют определить синдром Эдвардса на самых ранних этапах развития. К таким методам относятся следующие:
- Амниоцентез – проводится исследование образца околоплодных вод. Эта методика позволяет определить патологию с 14 недели беременности.
- Биопсия ворсин хориона – проводится исследование предварительно взятого кусочка плаценты, так как его структура совпадает со структурой тканей плода. Проводится с 8 недели.
- Кордоцентез – исследуется пуповинная кровь плода. Проводится с 20 недели.
- УЗИ — синдром Эдвардса в процессе этого исследования определяется только на поздних сроках беременности. Характерными признаками этой патологии по УЗИ являются: наличие пороков сердечно-сосудистой и мочеполовой системы; патологии мягких тканей головы, черепа; нарушения развития опорно-двигательных структур.
Кроме того, косвенными признаками заболевания, определяемые в ходе ультразвукового исследования, являются:
- одна артерия в пуповине;
- задержка развития;
- грыжа в брюшине;
- брадикардия;
- отсутствие костей носа.
Показатели отклонений
Трисомия 21, 18, 13 определяется с помощью различных методов диагностики, поэтому их прохождение во время беременности считается обязательным.
Определить наличие отклонений можно с помощью УЗИ. Однако диагностика на первых неделях беременности малоэффективна. В связи с чем, рекомендуется проходить иные методы исследований.
Наиболее информативным и часто назначаемым обследованием является анализ крови и биопсия плода.
Забор крови происходит у матери. При оценке показателей учитываются принятые нормы. Оценить состояние можно по таким показателям, как ассоциированный с беременностью протеин А-плазмы (PAPP-A) и хорионический гонадотропин человека (ХГЧ).
Низкий уровень PAPP-A и ХГЧ явно указывает на одну их хромосомных аномалий. Повышенный уровень показателей свидетельствует о проблемах с вынашиванием ребенка.
Профилактика
Говоря о профилактике заболевания, следует отметить, что риск его развития у будущего ребенка существует всегда. Но все же он повышается у родителей в возрасте после 40 лет.
Поэтому беременной очень важно выполнять все предписания наблюдающего ее гинеколога и проходить процедуру антенатального скрининга для своевременного выявления патологий.
Если у одного из супругов отмечается неблагоприятный семейный анамнез, то на этапе планирования беременности стоит обязательно посетить специалиста-генетика и следовать всем его советам.
Материал и методы
В рамках современного акушерского мониторинга в России проводится массовый ранний пренатальный скрининг (РПС) беременных на частые ХА, трисомии по хромосомам 21, 18, 13 и рано манифестирующие пороки развития у плода. Алгоритм РПС основан на международном стандарте, разработанном независимой врачебной организацией «Фонд медицины плода» и признанном в большинстве стран мира [1]. В сроки 11—14 нед беременности на экспертном уровне ПД одновременно проводятся ультразвуковое исследование (УЗИ) и биохимический скрининг (БХС) для выявления патологических пренатальных маркеров, а также расчет индивидуального риска выявления ХА на основе единого программного обеспечения, позволяющего вести базу данных и проводить внутренний индивидуальный аудит всех пренатальных измерений с оценкой качества РПС в регионе в целом.
Источником данных для проведения настоящего исследования явились сведения об обследованиях, проведенных в рамках РПС в Московской области за 5 лет, с 2011 по 2015 гг. Всего были обследованы 270 087 беременных, взято в анализ 266 779 случаев одноплодных беременностей в связи с имеющимся различием подходов к расчету рисков и к интерпретации результатов при многоплодных беременностях.
В программе РПС были созданы базы данных, куда вводились результаты УЗИ (в том числе наличие и описание маркеров ХА и ВПР), показатели биохимического исследования материнских сывороточных маркеров ХА (РАРР-А и свободная β-субъединица ХГч) [11], расчетные риски ХА с учетом порогового значения cut-off 1:100, результаты медико-генетического консультирования (МГК), инвазивной пренатальной диагностики (ИПД): виды манипуляций и лабораторные данные по анализу плодного материала, а также исходы беременности у женщин, прошедших РПС.
ИПД (аспирация ворсин хориона, амниоцентез) для постановки окончательного диагноза была проведена в 3053 случаях: в 61% наблюдений — аспирация ворсин хориона, в 39% — амниоцентез. По результатам лабораторного исследования плодного материала, выполненного посредством молекулярно-цитогенетических, цитогенетических исследований, было выявлено 916 различных хромосомных аномалий при общей эффективности пренатального кариотипирования 30%. Структура пренатально установленных за период исследования ХА представлена на рис. 1. Число включенных в исследование частых анеуплоидий (трисомий по хромосомам 21, 18 и 13) составило 663.
Рис. 1. Структура пренатально выявленных ХА в Московской области (2011—2015 гг.).
Диета
Диета при планировании беременности
- Эффективность: нет данных
- Сроки: 3-5 месяцев до планируемой беременности
- Стоимость продуктов: 1800-2000 руб. в неделю
Детям с такой патологией требуется специальное питание. В тяжелых случаях, при отсутствии глотательного и сосательного рефлексов, проводится питание через зонд.
Будущим мамам до и после зачатия нужно питаться правильно, не потребляя вредных продуктов и спиртного.
Синдром Дауна: причины и факторы риска
Синдром Дауна возникает из-за ошибки в производстве половых клеток – яйцеклеток или сперматозоидов.
Яйцеклетки и сперматозоиды возникают в результате деления клеток-предшественников с нормальным двойным набором хромосом. Этот диплоидный или двойной набор хромосом включает 22 пары аутосомы и 1 пару половых хромосом (XX у женщин и XY у мужчин). Итак, всего 46 хромосом.
В процессе деления генетическая информация обычно равномерно распределяется между развивающимися половыми клетками, каждая из них затем имеет гаплоидный или одинарный набор хромосом – 22 аутосомы и одна половая хромосома = 23 хромосомы. При оплодотворении – слияние яйцеклетки и сперматозоида образуется клетка-зигота с нормальным двойным набором хромосом. Из нее развивается ребенок в результате многочисленных делений клеток.
Ошибки могут возникать при делении 46 хромосом на создаваемые половые клетки – иногда две копии хромосомы случайно попадают в одну и ту же новую половую клетку. Тогда у гаметы всего 24 хромосомы вместо 23.
Если позже она сливается с другой «нормальной» половой клеткой во время оплодотворения, то в результате получается трисомная клетка – она содержит три рассматриваемой хромосомы – всего 47 хромосом. При синдроме Дауна лишняя хромосома, то есть 3 вместо 2, присутствует в 21 паре.
Прогноз
Синдром Эдвардса, как и другие генетические заболевания (трисомия 16 хромосомы, трисомия по X хромосоме), является неизлечимым недугом.
Как и любое другое генетическое заболевание, синдром Эдвардса не лечится. Однако возможно симптоматическое лечение, связанное с облегчением жизни данному ребенку, в том числе и хирургическое лечение пороков, сопутствующих синдрому.
Дети с полной формой синдрома редко доживают до года. По статистике, около 60% детей с этой болезнью умирают в возрасте до 3 месяцев. До годовалого возраста доживают только 5-10% таких больных, до 10 лет доживают только около 1% детей. В среднем мальчики живут 2-3 месяца, девочки – 10 месяцев. Больные навсегда остаются олигофренами.
Но если таким детям обеспечивают хороший уход и лечение, в некоторых случаях они могут жить дольше и иметь более качественную жизнь. Они могут научиться узнавать близких, самостоятельно есть, улыбаться.
У детей с мозаичной формой болезни шансы на более полноценную жизнь выше.
Что такое пренатальный скрининг
Пренатальный скрининг, диагностика и лечение является относительно новой проблемой в акушерстве. Началом пренатального скрининга была, возможно, эра ультразвуковой диагностики в акушерстве, которая началась около двух десятилетий назад. С открытием новых генов и их фенотипов становится все более возможным пренатальный генетический диагноз. Следует различать понятия скрининга и диагностики.
Пренатальный скрининг позволяет выявить индивидов высокого риска осложнений среди популяции индивидов с низким риском осложнений. Специфичность и чувствительность скрининговых тестов очень важны, учитывая возможность ложноположительных и ложноотрицательных результатов скрининга.
Пренатальная диагностика, конечно, более специфическая, чем скрининг (например, амниоцентез или биопсия хориона), но имеет и больший риск осложнений. Первым шагом по определению риска для плода является скрининг матери о наличии определенных состояний или заболеваний.
Нередко возникает вопрос о вероятности роста частоты врожденных пороков у потомков семейных пар, которые получали лечение по поводу бесплодия. Тяжелая олигоспермия и азооспермия ассоциируются со сбалансированными транслокациями хромосом (3-5%), синдромом Кляйнфельтера (47, ХХУ), аномалиями и микроделеции У-хромосомы.
Аномалии Х-хромосомы (ХХУ, ХХХ, Х-мозаицизм при синдроме Тернера) ассоциируются с пониженной фертильностью (субфертильностью), а также увеличением риска хромосомных аномалий у потомков. В 2/3 пациентов с врожденным отсутствием семявыносящих протоков имеет место хотя бы одна мутация гена, который отвечает за развитие кистозного фиброза. Итак, эти пациенты подлежат скринингу на наличие кистозного фиброза. Таким пациентам обычно показана интрацитоплазматическая инъекция сперматозоида в яйцеклетку, хотя наличие мутантного гена по кистозному фиброзу может влиять на репродуктивные намерения.
Синдром Дауна: факторы риска
В принципе, при каждой беременности существует вероятность того, что ребенок родится с синдромом Дауна или другим генетическим заболеванием. Однако по мере старения матери вероятность этого увеличивается. У 20-летней матери он ниже, но затем увеличивается с возрастом беременной, особенно заметно у матерей старше 35 лет.
Вероятность того, что ребенок родится с синдромом Дауна
| Возраст матери | Вероятность рождения ребёнка с синдромом Дауна |
| 20 лет | 1: 1500 (0,06%) |
| 25 лет | 1: 1350 (0,075%) |
| с 30 лет | 1: 900 (0,11%) |
| с 32 года | 1: 700 (0,14%) |
| с 34 лет | 1: 500 (0,2%) |
| с 35 лет | 1: 360 (0,27%) |
| с 36 лет: | 1: 300 (0,33%) |
| с 38 лет | 1: 200 (0,5%) |
| с 40 лет | 1: 100 (1%) |
| с 42 года | 1:65 (1,5%) |
| в 44 года | 1:37 (2,7%) |
| в 46 лет | 1:21 (4,8%) |
Решающим фактором является возраст матери при рождении ребенка.
Ученые предполагают, что деление яйцеклеток более подвержено нарушениям с возрастом. Это может облегчить совершение ошибок при делении хромосом. Вопрос о том, играет ли роль возраст отца, остается спорным.
Исследователи также обсуждают другие факторы, способствующие развитию синдрома Дауна. К ним относятся:
- эндогенные или внутренние факторы – определенные варианты генов;
- экзогенные или внешние факторы: вредное излучение, злоупотребление алкоголем, чрезмерное курение, использование оральных контрацептивов или вирусная инфекция во время оплодотворения.
Однако важность таких факторов неоднозначна.
Симптомы синдрома Дауна
Избыточный генетический материал влияет на физическое и умственное развитие.
Типичные симптомы:
- короткая голова – брахицефалия;
- плоский затылок;
- короткая шея;
- круглое и плоское лицо;
- раскосые глаза с тонкой складкой во внутреннем углу глаза – эпикантусом;
- увеличенное межзрачковое расстояние;
- яркие белые пятна на радужке – «пятна кисти» — они исчезают с возрастом и с накоплением цветных пигментов в радужке;
- плоская широкая переносица;
- в основном открытый рот и повышенное слюноотделение;
- выровненный язык, он часто бывает слишком большим и высовывается изо рта – макроглоссия;
- узкое, высокое небо;
- недоразвитые челюсти и зубы;
- маленькие, глубоко посаженные, круглые уши;
- избыток кожи на затылке, короткая шея;
- короткие широкие руки с короткими пальцами;
- четырехпальцевая борозда – поперечная борозда на ладони, начинающаяся под указательным пальцем и продолжающаяся ниже мизинца;
- большое пространство между первым и вторым пальцами стоп;
- плохо развитые мышцы – низкое мышечное напряжение и задержка рефлексов;
- рост медленный и ниже среднего – низкий рост, выраженная слабость соединительной ткани делает суставы излишне подвижными.
Возможные последствия:
- Пороки сердца. Они встречаются примерно у половины всех людей с синдромом Дауна. Распространенный порок сердца – АВ-канал или атриовентрикулярный канал. Это дефект перегородки между предсердиями и желудочками. Это вызывает одышку, нарушения роста и рецидивирующую пневмонию. Во многих случаях перегородка сердца между камерами сердца также не полностью закрыта – дефект межжелудочковой перегородки.
- Пороки развития пищеварительного тракта, например, сужением в области тонкой кишки или пороками развития прямой кишки.
- Ортопедические проблемы. К ним относятся, например, неправильное положение в области шеи и плеч, а также бедра – дисплазия бедра, нестабильная коленная чашечка и пороки развития стоп, например, плоскостопие.
- Нарушения слуха и зрения.
- Повышенная восприимчивость к инфекциям, поскольку иммунная система недостаточно развита. Например, многие дети с синдромом Дауна предрасположены к отиту, бронхиту и пневмонии.
- Нарушения дыхания во сне – обструктивное апноэ во сне. Оно сопровождающимся храпом: верхние дыхательные пути расслабляются и сужаются во время сна, что приводит к коротким паузам в дыхании. Насыщения кислорода в крови падает каждый раз. Мозг реагирует на это тревожным импульсом – человек просыпается. Однако пострадавшие быстро снова засыпают и обычно не могут вспомнить короткие фазы бодрствования на следующий день. Однако они часто устают в течение дня из-за недостатка спокойного и продолжительного сна.
- Повышенный риск лейкемии. Он в 20 раз больше, чем у детей без этой хромосомной аномалии. На хромосоме 21 есть несколько генов, играющих важную роль в развитии лейкемии. Так называемый острый миелоидный лейкоз чаще встречается при синдроме Дауна, чем острый лимфобластный лейкоз.
- Повышенный риск эпилепсии.
- Повышенный риск аутоиммунных заболеваний:
- сахарный диабет 1 типа;
- глютеновая болезнь;
- хроническая ревматическая болезнь в детстве – ювенильный ревматоидный артрит или ювенильный идиопатический артрит;
- заболевания щитовидной железы, например, тиреоидит Хашимото.
- Ограниченные интеллектуальные возможности. Синдром Дауна — ведущая причина врожденной умственной отсталости. Дети с трисомией 21 часто учатся говорить позже, чем другие дети, отчасти потому, что они хуже слышат. Вот почему их язык иногда бывает трудно понять. Во многих случаях людям требуется больше времени, чтобы понять проблему. Им часто бывает трудно вспомнить то, что они уже узнали, если им приходится узнавать что-то новое.
- Задерживается двигательное развитие — дети поздно начинают ползать или ходить.
- Повышенный риск поведенческих проблем или психических заболеваний, например, СДВГ, аутизма, тревожных расстройств и эмоциональных проблем вплоть до депрессии.
- Сниженная фертильность. Мальчики или мужчины с трисомией 21 обычно бесплодны. Пораженные девочки и женщины фертильны в ограниченной степени. Вероятность того, что они передадут хромосомную аномалию нерожденному ребенку во время беременности, составляет около 50%.