Синдром Золлингера-Эллисона — что это?
Данная патология является клиническими проявлениями гастриномы, которая представляет собой гормонально-активную опухоль.
Ряд вариантов опухоли развиваются агрессивно с образованием метастазов. Опухоль вырабатывает чрезмерное количество гастрин, тем самым вынуждая отвечать на это слизистую оболочку желудка выработкой большого количества секрета, что становится причиной язв, рвоты, диареи. В некоторых случаях патология развивается так стремительно, что необходимость в проведении операции возникает менее чем за сутки.
В 50-х годах XX столетия патологию считали язвенной болезнью желудка, которая протекает с диареей. Отмечалась и чрезмерная выработка желудком сока, а также высокий показатель в крови гастрина.
Причиной патологии считали:
- Серьезные нарушения питания;
- Чрезмерное употребление алкоголя;
- Стресс.
Лишь затем выяснили, что инициирует патологию опухоль нейроэндокринного характера, которая, как правило, локализуется в органах ЖКТ.
Описываемый синдром – довольно редкая патология, обнаруживающаяся у 1 человека на 1000000. Даже у тех, кто страдает язвой желудка, патология возникает около 1%.
Большая часть людей, подверженных патологии, – мужчины 40-55 лет.
Причины патологии
Опухолевые клетки вырабатывают гормональное вещество гастрин, он, в свою очередь, провоцирует желудок на выработку соляной кислоты в чрезмерном количестве.
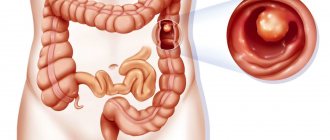
Почти 80% случаев возникновения опухоли приходится на двенадцатиперстную кишку, остальные локализуются в области поджелудочной железы.
Причиной возникновения опухоли является мутация генетичекого характера.
Неоплазии гастрин-продуцирующего типа могут локализоваться и в других органах, например, в легких, проявления их могут быть описываемой патологией.
Болезнь Менетрие
Менетрие описал два типа нарушений ассоциированных с полиповидными разрастаниями в желудке, которые он попытался связать с карциномой желудка [10].
- Первый (называемый «polyadenomes polypeux») состоит из множественных не сливающихся полипов желудка, которые в настоящее время классифицируются как гиперпластические полипы [11].
- Второй (который он назвал полиаденоматозом Менетрие, или множественными простыневидными (sheet-like) аденомами) является новым типом ассоциированным с фовеолярной гиперплазией и должен по закону носить его имя [8].
Кто подвержен особому риску?
Трудно спрогнозировать развитие патологии. Однако, изучая семейственность, можно предположить его генетические корни даже в тех случаях, когда симптомы были неявными либо их принимали за проявление иных заболеваний. Патология наследственной формы в большинстве случаев локализуется в двенадцатиперстной кишке.
Если говорить о тех, кого патология коснулась случайно, то необходимо отметить ее локализацию в поджелудочной железе.
Неоплазмы наследственного характера способны развиваться как множественные опухоли. Патология протекает мягче и онкологическая гастринома реже встречается. При этом хирургическое вмешательство полного излечения при данной форме не дает.
Диагностика и течение гастриномы
Для диагностики Синдрома Золлингера-Эллисона проводится анализ показателя гастрина. Концентрация 1000 нг на литр может свидетельствовать о наличии заболевания. Если при этом в сыворотке подтверждается хромогранин, все говорит о наличии нейроэндокринной опухоли. Устойчивые к терапии боли в животе атипичной локализации доказывают диагноз.
Для подтверждения расположения опухоли важно пройти ряд исследований. Для этого проводится визуализационная диагностика:
- Октреотид-сканирование;
- ПЭТ-КТ;
- МРТ;
- компьютерная томография.
Когда следует обратиться к врачу
Боли в животе, отеки, язвы или изменения формы тела, а также нарушения со стороны ЖКТ, диарея могут быть симптомами заболевания и поэтому необходимо проконсультироваться со специалистом, не дожидаясь обострения подобных проявлений.
Кроме того, обследование нужно пройти, если вы отметили:
- нарушения в пищеварении;
- изжогу;
- воспаление гортани;
- потерю веса;
- постоянные давящие боли;
- раздражительность;
- утомляемость;
- потерю аппетита.
Симптоматические проявления
Патология может обнаруживать себя различными проявлениями:
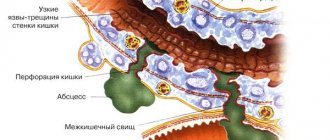
- Язвами желудка и 12-типерстной кишки;
- Постоянным интенсивным болевым синдромом в верхней части живота;
- Обильным, полуоформленным либо водянистым стул;
- Длительной изжогой и отрыжкой;
- Сужением пищевода;
- Желудочно-кишечными кровотечениями и т.д.
При онкологической природе патологии наблюдается снижение веса больного, причем снижения значительного.
Синдром верхней полой вены (СВПВ)
Симптомы заболевания
СЗЭ вызывает сильные боли в животе, имеющие, как привило, атипичную локализацию. Часто пациенты страдают от рефлюкса, при котором происходит заброс содержимого желудка в пищевод. Желудочная кислота вызывает воспаление слизистых и изжогу. Частым следствием рефлюкса является воспаление гортани. Половина пациентов страдают диареей.
Все это ведет к потере электролитов и витаминов. У ряда пациентов наблюдается рвота с кровью.
Кроме того, говоря о симптомах Синдрома Золлингера-Эллисона, нужно отметить, что переизбыток желудочного сока инактивирует липазы. Так как эти энзимы поддерживают пищеварение, нарушается адсорбция жиров в тонком кишечнике, и они попадают в толстую кишку, вследствие чего возникают жировые изменения консистенции кала. Иногда в крови повышается уровень pH. В редких случаях растет выработка гормонов паращитовидной железы.
Диагностические мероприятия
Определить наличие патологии можно, наблюдая многократное повышение уровня гастрина в крови.
При выполнении эндоскопического ультразвукового исследования можно увидеть опухоль, но лишь ее часть, т.к. расположена она в стенке двенадцатиперстной кишки.
Исследование с помощью компьютерной томографии и магнитно-резонансной томографии более четкое в смысле чувствительности. Степень этой чувствительности определяет размер опухоли. В любом случае ее необходимо обнаружить для дальнейшего мониторинга развития.
Эффективность ангиографии и ПЭТ связаны с хорошим снабжением кровью новообразования. Окончательно диагноз объявляют после исследования биоптата.
Как показывает практика, 2/3 опухолей не являются злокачественными, соответственно, метастазы отсутствуют. Агрессивностью отличаются спорадические опухоли, но это для множественной эндокринной неоплазии это не типично.
Раковые образования железы поджелудочной обычно метастазируют. Они могут стать причиной поражения печени и лимфатических узлов полости брюшины.
Опухоли двенадцатиперстной кишки чаще поражают кости, как правило, плоские.
Возможность появления метастазов зависит от размера опухолевого очага, они могут стать причиной усиления патологии.
Введение
В настоящее время широкое распространение приобрело понятие «заболевания, связанные с повышенной секрецией соляной кислоты». Оно описывает спектр патологических состояний, при которых повышенная продукция соляной кислоты слизистой желудка является одной из основных причин жалоб больных [8]. То, что соляная кислота является основным компонентом желудочного сока, известно давно и установлено Вильямом Протом (William Prout (1785-1850 гг.) в 1823 г. [28]. Еще Парацельс (Paracelsus (1493-1541 гг.), вопреки главенствовавшему тогда мнению Святой Церкви, отводил кислоте значимую роль в пищеварении [28]. В соответствии с современными представлениям о патогенезе заболеваний, связанных с повышенной секрецией соляной кислоты, важнейшим является нарушение равновесия между кислотно-пептической агрессией и защитными механизмами слизистой органов желудочно-кишечного тракта [60]. Гиперпродукция кислоты важная, но, как правило, не единственная причина развития симптомов заболевания [41]. Понятие «заболевания, связанные с повышенной секрецией соляной кислоты» определяет круг больных, которым целесообразно назначение терапии, направленной на снижение кислотопродукции [8].
Современные принципы лечения заболеваний, связанных с повышенной секрецией соляной кислоты, основываются на назначении в первой линии комплексной терапии ингибиторов протонной помпы (ИПП). Всемирный конгресс гастроэнтерологов, состоявшийся в Риме в 1988 г., признал ИПП основной группой кислотоконтролирующих лекарственных средств [57]. Значительные успехи в клиническом применении антисекреторных препаратов внесли коррективы и в хирургическую гастроэнтерологию. Число операций по поводу язвенной болезни значительно уменьшилось. В 1993 г. на конференции гастроэнтерологов в Йеле было принято соглашение о том, что ваготомия не может больше рассматриваться как метод выбора в лечении язвенной болезни [57].
В настоящее время ИПП применяются при лечении широкого круга заболеваний желудочно-кишечного тракта. В первую очередь речь идет о хроническом гастрите, дуодените и язвенной болезни желудка и двенадцатиперстной кишки, в том числе и для профилактики развития острых язв желудка и двенадцатиперстной кишки при длительном приеме неселективных НПВП, комбинированной терапии с антибиотиками для эрадикации Helicobacter pylori,
а также гастроэзофагеальной рефлюксной болезни и пищеводе Барретта. Принципы лечения этих заболеваний достаточно освещены в литературе [4, 5, 7, 11, 17, 18, 23, 24, 32, 38-40, 42, 44, 45, 49] и опубликованы в стандартах медицинской помощи, утвержденных Минздравсоцразвития России. Следует отметить, что терапия ИПП может маскировать симптомы злокачественных заболеваний и до начала лечения необходимо верифицировать диагноз, а также исключить наличие у больного злокачественной опухоли желудочно-кишечного тракта.
В современной литературе необоснованно мало внимания уделяется роли ИПП в лечении синдрома Золлингера-Эллисона, при котором повышенная продукция соляной кислоты играет ключевую роль в развитии симптомов заболевания, а антисекреторная терапия имеет ряд особенностей.
Общие сведения о синдроме Золлингера-Эллисона
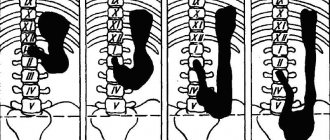
Синдром Золлингера-Эллисона характеризуется развитием пептических язв двенадцатиперстной кишки и желудка, трудно поддающихся лечению, склонных к желудочно-кишечным кровотечениям и сопровождающихся поносами, на фоне гастринпродуцирующей нейроэндокринной неоплазии (гастриномы). Сочетание нейроэндокринной неоплазии поджелудочной железы с чрезвычайно агрессивным течением язвенной болезни описали американские хирурги R. Zollinger и E. Ellison в 1955 г. [54], и в мировой литературе комплекс клинических проявлений ульцерогенной аденомы (гастриномы) носит их имена.
Частота синдрома Золлингера-Эллисона составляет 0,5-3 случая на 1 млн населения в год [12, 35, 43]. В большинстве наблюдений (50-88%) гастриномы локализуются в двенадцатиперстной кишке. Однако эти новообразования могут встречаться в желудке, печени, общем желчном протоке, яичнике, а также вне брюшной полости (в сердце, легком) [15, 51, 52]. Длительность заболевания до верификации диагноза в среднем составляет 5,2 года, симптомы заболевания соответствуют гиперсекреции соляной кислоты: развитие пептических язв или гастроэзофагеальной рефлюксной болезни на фоне диареи [12]. Боли в животе, обычно связанные с язвенной болезнью или гастроэзофагеальной рефлюксной болезнью, наблюдаются у 75-98% больных, диарея встречается в 30-73% наблюдений, изжога — в 44-56%, желудочно-кишечные кровотечения — в 44-75%, тошнота/рвота — в 12-30%, снижение массы тела — в 7-53% наблюдений [36]. Наличие H. pylori
при язвенной болезни у больных с синдромом Золлингера-Эллисона отмечается в 24-48% наблюдений, в то время как у больных идиопатической язвенной болезнью — более чем в 90%. Отсутствие хеликобактерной инфекции у больного с рецидивирующей язвенной болезнью тяжелого течения должно насторожить клинициста в отношении наличия синдрома Золлингера-Эллисона [51]. У больных с синдромом множественных эндокринных неоплазий 1-го типа (МЭН-1) клинические проявления синдрома Золлингера-Эллисона (20-30% больных с МЭН-1) возникают в более раннем возрасте, в среднем в 32-35 лет [37].
Более чем у 98% больных с синдромом Золлингера-Эллисона отмечается повышенный уровень гастрина сыворотки крови натощак, у 87-90% больных — повышенная секреция соляной кислоты в желудке и у 100% больных уровень рН желудочного сока не превышает 2,0 [35, 36]. Гипергастринемия, как правило, превышает 1000 пг/мл, в то время как при язвенной болезни уровень гастрина крови редко превышает 100 пг/мл. Кислотопродукция у больных с синдромом Золлингера-Эллисона превышает 100 ммоль/ч.
Размер гастрином, локализующихся в двенадцатиперстной кишке, у 77% больных не превышает 1 см, в то время как размер гастрином, выявляемых в поджелудочной железе, в среднем составляет 3,8 см, только у 6% больных обнаруживаются гастриномы поджелудочной железы диаметром менее 1 см. Аналогично другим нейроэндокринным неоплазиям желудочно-кишечного тракта гастриномы классифицируются по системам ВОЗ (2010 г.) и TNM [6] и в большинстве наблюдений характеризуются как нейроэндокринные опухоли G1-G2. На момент диагностики они имеют признаки инвазивного роста и метастазы в лимфатические узлы [3, 20, 21]. Метастазы в печень наиболее характерны для гастрином поджелудочной железы и выявляются в 22-35% таких наблюдений. Отдаленные метастазы гастрином двенадцатиперстной кишки обнаруживаются не более чем у 10% больных [16, 20, 21]. Гистологически большинство гастринпродуцирующих неоплазий имеют трабекулярное строение, высокодифференцированы, а индекс пролиферации Ki67 чаще составляет около 2% и редко превышает 10% [16, 20, 21].
Основным методом лечения больных гастринпродуцирующими нейроэндокринными неоплазиями с синдромом Золлингера-Эллисона является хирургический [19]. Пятилетняя выживаемость больных со спорадическими гастриномами достигает 45% [16, 29-31]. Спорным остается и вопрос о необходимости оперативного лечения больных с гастринпродуцирующими нейроэндокринными неоплазиями в рамках МЭН-1 [2, 48]. Есть мнение, что оперативное вмешательство таким больным целесообразно выполнять лишь при размерах неоплазий более 2 см. Такая позиция связана с низкой вероятностью излечения и хорошими показателями выживаемости больных с опухолями малых размеров (до 2 см) на фоне симптоматической терапии ИПП [29]. По мнению других авторов, оперативное лечение показано всем больным с синдромом Золлингера-Эллисона в рамках синдрома Вермера [1, 2, 47].
Механизм действия ингибиторов протонной помпы
Одним из широко используемых в клинической практике ИПП является контролок, который эффективен в комплексном лечении заболеваний желудочно-кишечного тракта, связанных с повышенной секрецией соляной кислоты [7]. Молекулы препарата, накапливаясь во внутриклеточных канальцах париетальных клеток, трансформируются в тетрациклический сульфенамид, который ковалентно включается в цистеиновые группы Н+/К+-АТФазы, делая тем самым фермент неспособным участвовать в процессе транспортировки ионов. Таким образом, препарат подавляет конечную фазу образования соляной кислоты. Для восстановления способности секретировать соляную кислоту париетальная клетка вынуждена в таких случаях синтезировать новую молекулу фермента [58].
Контролок быстро всасывается, максимальная концентрация его в плазме крови достигается даже после приема одной дозы препарата. В среднем максимальная концентрация 1,0-1,5 мкг/мл достигается через 2,0-2,5 ч после приема, эти уровни остаются постоянными после многократного приема. Контролок отличается от омепразола и лансопразола структурой радикалов на пиридиновом и бензимидазольном кольцах, что делает его и стабильнее при значениях рН, близких к нейтральным [13, 33]. Объем распределения составляет 0,15 л/кг, клиренс контролока приблизительно 0,1 л/ч/кг, период полувыведения 1 ч. В связи со специфической активацией контролока в париетальных клетках период полувыведения не коррелирует с длительностью действия (угнетения секреции кислоты). Фармакокинетика не меняется после одноразового или многократного приема. В диапазоне доз от 10 до 80 мг фармакокинетика препарата остается линейной как после перорального приема, так и после внутривенного введения. Связывание с белками плазмы крови составляет 98%.
Препарат метаболизируется в печени. Основной путь выведения метаболитов — почечный (80%), с калом выводится 20%. Контролок полностью всасывается после перорального приема. Абсолютная биодоступность препарата в форме таблеток, резистентных к желудочному соку, составляет 77%. Употребление пищи не влияет на максимальную концентрацию препарата и его биодоступность. Больным с нарушениями функции почек (включая находящихся на гемодиализе) нет необходимости снижать дозу контролока. Как и у здоровых субъектов, период полувыведения препарата у таких больных короткий. У больных циррозом печени (класс А и В) период полувыведения препарата увеличивается до 3-6 ч и максимальная его концентрация в плазме крови повышается в 1,3 раза по сравнению с таковой у здоровых людей. Больным с тяжелыми нарушениями функции печени суточную дозу необходимо снижать до 20 мг. Небольшое повышение максимальной концентрации в пожилом возрасте по сравнению с соответствующими данными у больных младшего возраста не является клинически значимым [46, 50].
Известно, что расовые генетические особенности могут влиять на выраженность ингибирования кислотообразования [56]. Метаболизм контролока происходит в печени с участием изоформ цитохрома Р450: CYP2C9, CYP2C19, CYP2D6 и CYP3A4. Полиморфизм гена, кодирующего изоформу CYP2С19, определяет различную скорость метаболизма ИПП. Отмечен значительный разброс индивидуальной продолжительности антисекреторного эффекта от 1 до 12 сут [14, 55]. Поэтому с целью исключения «неудачи» при терапии ИПП подбор препаратов следует проводить под контролем суточной рН-метрии [59].
Особенности применения контролока при синдроме Золлингера-Эллисона
Симптоматическое лечение больных с синдромом Золлингера-Эллисона кардинально изменилось с внедрением в клиническую практику ИПП [10]. От гастрэктомии, выполняемой с целью профилактики развития острых язв [53], в настоящее время рекомендовано воздерживаться, особенно в случае, если хирургическое лечение гастрином имеет радикальный характер [19]. Снижение кислотопродукции при использовании стандартных терапевтических доз ИПП для лечения язвенной болезни способствует уменьшению интенсивности симптомов заболевания практически у всех больных с синдромом Золлингера-Эллисона. Применение Н2-блокаторов в терапевтических дозах, как правило, не дает столь значимого клинического эффекта [9, 51].
Опубликован ряд исследований, доказывающих эффективность применения контролока при симптоматическом лечении синдрома Золлингера-Эллисона [10, 22, 25-27, 34]. При пероральном приеме рациональной суточной дозой контролока у таких больных считается 120 мг. Подбор дозы препарата должен быть индивидуальным. Суточная доза может колебаться от 40 до 160 мг [10]. Внутривенное введение контролока также эффективно, у 93% больных с синдромом Золлингера-Эллисона внутривенное введение 80 мг в сутки адекватно и не сопровождается серьезными нежелательными явлениями [22, 26]. Контролок эффективен и при длительной поддерживающей терапии синдрома Золлингера-Эллисона. У большинства больных контроль над симптомами заболевания достигали приемом 40-80 мг препарата в сутки (см. рисунок)
[25].
Рисунок 1. Динамика средней кислотопродукции у больных с синдромом Золлингера-Эллисона на фоне длительного приема различных суточных доз контролока [25].
Длительное назначение ИПП связано еще с двумя аспектами. Во-первых, бесконтрольное длительное их назначение привело к росту числа больных с запущенными гастриномами. Симптомы заболевания маскируются эффективным подавлением кислотопродукции, именно поэтому множественные язвы или язвы с нехарактерной локализацией встречаются все реже [51]. Во-вторых, следует помнить, что длительное использование ИПП приводит к гипергастринемии у больных язвенной болезнью без синдрома Золлингера-Эллисона [32]. В связи с этим необходимо временное прекращение приема препаратов перед исследованием уровня гастрина. Само по себе повышение уровня гастрина недостаточно для верификации синдрома Золлингера-Эллисона. Причинами гипергастринемии могут быть гипо- и ахлоргидрия (при хроническом атрофическом гастрите, пернициозной анемии), а также инфекция H. pylori,
стеноз выходного отдела желудка, почечная недостаточность, синдром короткой тонкой кишки.
Таким образом, контролок является эффективным и безопасным средством в лечении целого ряда заболеваний, связанных с повышенной секрецией соляной кислоты. Принципы терапии этих заболеваний определены стандартами медицинской помощи, утвержденными Минздравсоцразвития России. Имеются особенности применения ИПП при симптоматическом лечении больных с синдромом Золлингера-Эллисона, которые недостаточно освещены в литературе, российских стандартов лечения таких больных нет. При назначении контролока больным с синдромом Золлингера-Эллисона рекомендуется увеличивать его суточную дозу до 120 мг при пероральном применении и до 80 мг при внутривенном введении. Контролировать концентрацию гастрина крови у больных, длительное время получающих контролок, целесообразно только после заблаговременной отмены препарата. В противном случае выявленная гипергастринемия не будет иметь диагностической ценности. Пролонгированное применение контролока у этой группы больных также эффективно.
Лечение
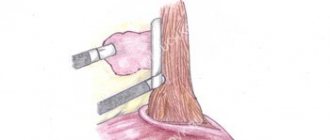
Радикальный метод лечения патологии – удаление опухоли. При этом проводят волоконно-оптическую диафаноскопию 12-типерстной кишки и латеральную дуоденотомию. Как правило, на момент оперативного вмешательства выявляют метастазы, что значит, только для 30% пациентов можно будет добиться полного излечения.
Невысока эффективность удаления значительной части желудка: риск быстрого рецидирования достаточно высок.
Несколько десятилетий назад широко использовался метод тотальной гастрэктомии. Сейчас к нему прибегают, если лечение консервативное положительных результатов не дает и осложняется течение язвы.
Для терапии применимы препараты, которые снижают уровень соляной кислоты. Их применение может быть показано пожизненно, так как риск рецидива высокий. Дозы препаратов превышают обычные, назначаемые при стандартной язве.
При онкологии и невозможности провести хирургическую операцию на опухоль, применяют химиотерапию.
Патогенез
Патогенез болезни Менетрие не вполне понятен, но может реализовываться через трансформирующий фактора роста альфа (TGF-alpha). TGF-alpha усиливает продукцию желудком слизи и ингибирует секрецию кислоты [12-14]. Уровень TGF-alpha в клетках слизистой желудка у пациентов с болезнью Менетрие значительно увеличен [12]. Роль TGF-alpha дополнительно подтверждается при исследовании на мышах в котором гиперпродукция TGF-alpha связанна со значительной гиперплазией слизь продуцирующих клеток желудка, сравнимой с таковой обнаруживаемой у людей с болезнью Менетрие [12]. Эти мыши так же имели сниженную базальную и гистамин стимулированную секрецию кислоты, сходную с наблюдаемой у людей с болезнью Менетрие [12,13,15]. TGF-alpha может оказывать свой эффект путем связывания с эпидермальными рецепторами фактора роста. Это было предположено на основании сообщения о пациенте с наступившим клиническим улучшением после лечения моноклональными антителами, направленными против эпидермальных рецепторов фактора роста [16]. Сходную связь с цитомеголовирусной инфекцией наблюдается при так называемой детской болезни Менетрие. Ее механизм может так же реализовываться через TGF-alpha [17]. Однако при различных видах воспаления и регенеративного ответа в желудке могут так же наблюдаться увеличения фовеолярного TGF-alpha, демонстрируя, что эти находки могут быть неспецифичными [18]. В дополнение к этому, данная патология может быть примером неправильного использования термина болезнь Менетрие к другим формам гипертрофической гастропатии.
Диагноз
Диагноз болезни Менетрие выставляется на основе выявления экстремальной степени фовеолярной гиперплазии с атрофией желез при биопсии у пациента со значительным увеличением складок желудка наблюдаемым при эндоскопическом исследовании или рентгенографии с барием. Биопсия «на всю толщу» или петлевая биопсия обычно необходима [3,22]. Увеличенные складки ограничены телом и дном желудка. Складки обычно увеличены симметрично, хотя редко может встречаться асимметричное «полиповидное» увеличение.