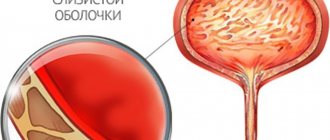
Избавление от рака — заветная мечта всех онкологических больных, большинство пациентов готово платить за долгую жизнь после рака большую цену. Мало кто предполагает, что жизнь после лечения будет другой по патофизиологическим ощущениям.
После радикального лечения рака желудка (успешного, потому что операция возможна далеко не всегда) пациент в первые дни сталкивается с новой проблемой. До операции доктор расскажет, что большая часть желудка с опухолью будет удалена. Как правило, удаляют три четверти, или весь желудок целиком. С этими четвертями уйдёт способность привычно питаться три раза в день, но про эту утрату больной пока не задумывается. После операции может возникнуть состояние, не позволяющее не только нормально поесть, но и нормально чувствовать себя после еды. Речь о пострезекционном синдроме, появившемся из-за удаления части желудка. Состояние также именуется демпинг-синдром от английского «dumping» — сброс.
Что делают с желудком хирурги
Операция на желудке – чётко выверенная на тысячах больных хирургическая методика, позволяющая удалить какую-то часть или весь орган с наименьшими потерями. Наименьшие потери при удалении части желудка – максимальное сохранение анатомо-физиологического пути передвижения и переваривания пищевых масс. В зависимости от места расположения опухоли в желудке выполняют субтотальные резекции дистальную и проксимальную, и по-прежнему часто выполняется полное удаление желудка – гастрэктомия.
Лечение
Если говорить о стадии легкой, то на помощь приходит диета, в основе которой высококалорийное питание и витамины. А вот потребление жидкости необходимо ограничить. Такое же предписание и к потреблению углеродов.
Если синдром проявляется в форме средней, показан прием специальных препаратов, которые снижают сбои в работе кишечника. Значимую роль играет терапия общеукрепляющего характера.
Синдром формы тяжелой при недостаточности терапии требует хирургической манипуляции, суть которой интерпозиция части кишечника.
Операции Бильрота и гастрэктомия
Первым хирургом, не просто 29 января 1881 года удалившим поражённую раком часть желудка, но и выходившим после тяжёлой операции больного, был австриец Христиан Альберт Теодор Бильрот. Позже его пригласили к погибающему от рака ротовой полости великому хирургу Пирогову, также он оперировал поэта Некрасова. Важнейшие операции на желудке, применяемые по сей день, были разработаны Бильротом и носят его имя.
Резекция желудка по Бильрот I заключается в соединении остатка желудка с двенадцатиперстной кишкой «конец-в-конец». Это не соответствует природе человека, сформировавшей плотно закрывающийся мышечным жомом переход между желудком и кишкой. Эвакуация пищевых масс из оперированного желудка происходит быстро, тем не менее, желудок частично исполняет роль резервуара для еды. Слизистая желудка не соприкасается со слизистой тонкой кишки, что уберегает последнюю от хронических изъязвлений.
При резекции желудка по Бильрот II оставшуюся часть желудка сшивают «бок-в-бок» с тощей кишкой, а двенадцатиперстная кишка выключается из оборота, что совсем нефизиологично. Субтотальная резекция желудка по Бильрот-II очень распространена в онкологии, хирургическую тактику определяет раковая опухоль. Именно при этом варианте чаще развивается демпинг-синдром.
Гастрэктомия – полное удаление желудка – обязательно приводит к демпинг-синдрому. Пищевод соединяется с кишкой, нет резервуара для временного хранения пищи с одновременным перевариванием, роль которого исправно исполнял желудок, пища сразу попадает в кишку, не приспособленную к неподготовленным пищевым массам.
Возможные осложнения
Если длительное время игнорировать клиническую картину синдрома, присоединяется дополнительная симптоматика:
- Заболевания органов ЖКТ: язвенная болезнь, энтериты, колиты, панкреатит.
- Гипогликемические состояния, провоцирующие гормональный дисбаланс, развитие сахарного диабета.
- Кахексия. Пациент теряет вес, что в итоге приводит к значительному дефициту массы тела и общему истощению. Запущенная патология может привести к летальному исходу.
Лечение демпинг-синдрома без повторной операции возможно при условии выполнения неотложных медикаментозных назначений опытного специалиста.
Проявления демпинг-синдрома
При раке желудка в организме больного происходят настолько выраженные биохимические нарушения, что даже в конце прошлого века четверть больных погибала после операции по неясным причинам. Сегодня современная наука выхаживания послеоперационных пациентов позволила забыть об этой печальной четверти, тем не менее, биохимические процессы в организме желудочного больного не стали меньше.
Быстрая эвакуация пищи в кишку приводит к серьёзным нарушениям биохимических процессов, что отражаемся на состоянии больного. Через несколько минут после еды больного буквально накрывает слабость. Интенсивность слабости очень разная, от кратковременной и принципиально не мешающей жизни и работе, до состояния полного бессилия.
Слабость сопровождается сильным сердцебиением и даже болями в области грудной клетки, но это не стенокардитические боли, обусловленные нарушением питания миокарда – ишемией, а кардиалгия, то есть как бы боли в сердце. Но на самом деле болит не сердце. При истинной сердечной боли болит за грудиной, боль отдаётся в руке, плече, челюсти. Но в особо тяжёлых случаях демпинг-синдрома на ЭКГ отмечаются преходящие изменения по типу ишемии миокарда.
Наблюдаются скачки артериального давления. Дрожат руки, кружится голова, шумит в ушах. Пациент бледен или наоборот, краснеет лицом, почти всегда обильно потеет. Часто отмечаются позывы на мочеиспускание. Беспокоят тошнота и рвота, боли в животе, громкое урчание, отрыжка, позывы на дефекацию вплоть до поноса. Клиническая картина очень разнообразная, видно, что человеку очень плохо, некоторые на пару часов после каждой еды нуждаются в постельном режиме.
Пациент испытывает страх, настолько неприятны и разнообразны симптомы. Он может терять сознание, о чём не всегда и вспоминает после. Как не странно, но воспоминания при демпинг-синдроме тоже далеко не всегда соответствуют действительности, возможна и амнезия после приступа. В связи с этим даже выделили эпизодический вариант, когда синдром развивается сразу после еды, сопровождается страхом, о котором пациент плохо помнит. Пароксизмальный вариант возникает через пару часов после еды, приводит к потере сознания и амнезии. И всему этому есть объективная биохимическая причина.
Симптомы синдрома оперированного желудка
По тяжести заболевания демпинг-синдром бывает легким, средним и тяжелым.
Легкая степень тяжести:
- Приступы возникают 1-2 раза в месяц при погрешности в диете. Длятся по 15-30 минут, проходят самостоятельно после отказа от продуктов богатых углеводами, молока. Иногда отмечаются диареи.
Средняя степень тяжести:
- Приступы по 4-5 раз в неделю продолжительностью от 1 до 2 часов, сопровождаются учащенным сердцебиением, повышением артериального давления, диареей, снижением работоспособности, снижением массы тела до 10 кг.
Тяжелая степень тяжести:
- Приступы продолжительностью 3-4 часа после любого приема пищи, возможно с утратой сознания, кахексией.
Как часто отмечается демпинг-синдром
Такая картина может появляться после каждого приёма пищи, но во время завтрака она более выражена, в обед проявления чуть меньше, а в ужин ещё меньше. Симптомы могут длиться несколько минут, а могут продолжаться до трёх часов. Это далеко не всё, потому что у больного и в остальное время тоже отмечается слабость, но не такая интенсивная, а со временем развивается астенизация, в том числе, снижение потенции.
Частота развития демпинг-синдрома неизвестна, в специальной литературе указывают разные цифры – от 10 до 80%, всё зависит от того, насколько прицельно авторский коллектив, написавший статью, занимается его лечением. Если авторы статьи занимаются лечением пострезекционных осложнений, то частота высокая – они же специально собирают таких пациентов. Если научный материал подготовлен хирургами, то полноценная констатация демпинг-синдрома у оперированных больных далека от идеальной и реальной, как правило, отслеживается только тяжёлое течение.
В большинстве случаев синдром протекает легко с частично смазанными клиническими признаками, тяжёлое течение характерно для оперированных женщин. Опять-таки, толком неизвестно сколько бывает пациентов с тяжёлым по течению синдромом, предлагаются варианты от одного до десяти на сотню оперированных. Некоторые прооперированные пациенты, испытывающие слабость после еды, даже не подозревают о наличии лёгкого демпинг-синдрома, который можно было бы скорректировать, если бы диагноз был поставлен.
Методы диагностики в Медскан
Демпинг-синдром является осложнением хирургического лечения рака желудка или метастазов желудка при различных онкопатологиях. Предварительный диагноз ставится на основании клинической картины. Обязательная диагностика демпинг-синдрома при раке желудка включает в себя:
- Лабораторные методики обследования: анализы крови и мочи. Определяется состояние печени (печеночные пробы, уровень щелочной фосфатазы), сосудов (холестерин), поджелудочной железы (амилаза, глюкоза).
- Эндоскопия и рентгенографическое исследование пищевода и желудка. Исследование помогает узнать характер изменений органов после операции.
- КТ, МРТ прилегающих тканей.
- Проба с сахаром. Больному измеряют частоту пульса и давление, после чего внутривенно вводят раствор глюкозы. При ухудшении самочувствия измерения повторяются. Если характерных симптомов нет, анализ проводят повторно.
- Сцинтиграфия – процедура, позволяющая установить скорость опорожнения желудка.
Диагностический центр клиники Медскан оснащен современным оборудованием экспертного уровня. Своим пациентам мы предлагаем широкий спектр лабораторных и инструментальных обследований.
Почему развивается
В развитии демпинг-синдрома ведущая роль принадлежит быстрой эвакуации пищи через то, что осталось от желудка, и столь же скорое наполнение необработанной едой тощей кишки. Рефлекторные сигналы из раздувающейся пищевым комком тощей кишки вызывают приток крови к внутренним органам, на периферии объём циркулирующей крови наоборот снижается. Кровь внутренним органам в поступающем большом объёме совсем не нужна, поэтому она депонируется, при этом головной мозг испытывает настоящее голодание.
Поступившие в кишку без предварительной должной обработки питательные вещества проскакивают через мембраны клеток слизистой в кровь. В эксперименте растяжение тощей кишки приводит к выбросу в кровь биологически активных веществ, главным образом, «гормона радости» серотонина и ацетилхолина. Отсюда слабость, сердцебиение, покраснение лица и потливость, колебания артериального давления.
Обнаружено повышение уровня выделяемого надпочечниками адреналина, а процесс его секреции запускает гипофиз, получивший информацию от энтерохроматофинных клеток слизистой оболочки тонкой кишки. Эти клетки также возбуждают рвотный центр головного мозга. Растяжение кишки постёгивает перистальтику – сокращение кишечника, что оборачивается диареей, при которой теряются жидкость, белки и микроэлементы, что усугубляет слабость и снижение давления крови.
Быстрое всасывание глюкозы в тощей кишке нарушает обменные процессы в поджелудочной, которая выбрасывает в кровь инсулина больше необходимого. Концентрация сахара в крови снижается ниже нормального уровня, что тоже сопровождается резкой слабостью, голодом, дрожью. С этим механизмом связывают отсроченный демпинг-синдром, развивающийся через пару часов после еды. У каждого пациента в разной степени развиваются все эти патофизиологические изменения, которые в результате приводят к снижению и без того небольшого веса пациента, развитию у него анемии и авитаминозов, и главное – некомфортной жизни.
О прогнозе и мерах профилактики
Медицинская практика показывает, что развитие синдрома обычно приходится на первые послеоперационные шесть месяцев.
У половины пациентов он с течением времени ослабевает, еще у четверти остается на определенном уровне и не развивается, у последних двадцати пяти процентов наоборот.
Профилактические меры основываются к систематическому наблюдению у специалиста, диета, курортное лечение.
Клиника интегративной онкологии Onco.Rehab работает, используя международные протоколы лечения. Мы делаем все, чтобы сохранить здоровье наших пациентов!
И.В. Федоров
ГБОУ ДПО «Казанская государственная медицинская академия» МЗ РФ, г. Казань
Федоров Игорь Владимирович — доктор медицинских наук, профессор кафедры эндоскопии, общей и эндоскопической хирургии
420012, г. Казань, ул. Муштари, д. 11, тел., e-mail: Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Реферат. В лекции описаны этиология, диагностика, профилактика и лечение таких постгастрорезекционных осложнений, как демпинг-синдром, постваготомная диарея, щелочной рефлюкс-гастрит, синдромы приводящей и отводящей петли, желудочная атония, Ру-синдром, рецидив язвенной болезни, рак культи желудка и синдром малой культи желудка.
Ключевые слова: постгастрорезекционный синдром, демпинг-синдром, рак культи желудка.
Любые операции на желудке, особенно те, которые сопровождаются удалением или отключением привратника, особенно с сопутствующей ваготомией, могут сопровождаться серьезными нарушениями желудочной моторики. Такие расстройства весьма распространены, однако адаптация обычно наступает спустя 6 месяцев после операции. Небольшое, но значимое число пациентов страдают этими симптомами и дальше, что существенно подрывает их здоровье. Совокупность данных симптомов называют постгастрорезекционными (ПГРС) или постгастрэктомическими. Они включают демпинг, щелочной рефлюкс-гастрит, постваготомическую диарею, Ру-синдром, обструкцию приводящей/отводящей петли, хроническую атонию желудка и синдром малой желудочной культи. Эти симптомы связаны либо с ускорением, либо с замедлением опорожнения желудочной культи. Другие поздние осложнения — рецидив язвы, рак культи желудка, малабсорбция — напрямую не связаны с нарушением моторики.
Демпинг-синдром
Демпинг-синдром (ДС) — одна из наиболее частых причин болезненного состояния после операций на желудке. Симптомы развиваются после приёма пищи, но человек совершенно здоров натощак. Синдром характеризуется гастроинтестинальными и вазомоторными проявлениями. Гастроинтестиальные симптомы включают сжимающую боль в животе, вздутие, тошноту, рвоту, обильную диарею. Для вазомоторных симптомов характерно обильное потоотделение, головокружение, сердцебиение, слабость и огромное желание прилечь. Тяжесть ДС весьма вариабельна и зависит от вида хирургического вмешательства. В целом это состояние испытывают 25-50% больных после операций на желудке, однако лишь у 1-5% он протекает в тяжелой, калечащей форме. Тяжёлые симптомы возникают у 3-5% больных после селективной проксимальной ваготомии (СПВ), у 6-14% после стволовой ваготомии (СтВ) с дренированием и у 14-20% после резекции желудка.
ДС разделяют на ранний и поздний, в зависимости от времени появления клинических симптомов. Ранний демпинг стартует через 10-30 минут после еды. Больные испытывают вазомоторные и гастроинтестинальные симптомы. Поздний демпинг начинается через 2-3 часа после еды и проявляется только в виде вазомоторных симптомов. Примерно 75% больных испытывают ранний, а 25% — поздний демпинг, малое число страдает обоими. Симптомы проявляются обычно в первые недели после операции, когда больной возвращается к нормальному питанию. Жидкая и углеводородная пища переносится плохо. Некоторые больные из-за страха еды теряют в весе.
Широко распространена версия, что ДС связан с быстром опорожнением желудка. Это обусловлено четырьмя хирургическими факторами: снижением адаптации и рецептивной релаксации, которая сопровождает ваготомию; снижением объёма желудка, как следствие резекции органа; снижением контроля за опорожнением из-за удаления или отключения привратника; ликвидацией механизма обратной связи при отключении 12-перстной кишки. Специальные исследования показали, что ДС у здорового человека провоцируется быстрым введением глюкозы непосредственно в 12-перстную или тощую кишку. Введение гиперосмолярного химуса в тощую кишку приводит к перемещению большого количества жидкости из кровяного русла в просвет кишечника. В результате расширения тонкой кишки происходит увеличение амплитуды и частоты сокращений, что вызывает гастроинтестинальные симптомы. Секвестрация жидкости приводит к гиповолемии, что провоцирует вазомоторные проявления.
Однако есть доказательства, что не только желудочное опорожнение отвечает за ДС. Не все исследователи подтверждают прямую связь между этим осложнением и скоростью опорожнения желудка.
Гиповолемия сопровождается увеличением частоты сердечных сокращений, тахикардия имеет место у больных с ранним ДС. Это приводит к периферической вазоконстрикции. Хотя некоторые исследования демонстрируют вазодилатацию, например, увеличение кровонаполнения мезентериальных артерий после провокации ДС. Органная вазодилатация и депонирование крови может быть дополнительным фактором, усугубляющим вазомоторные симптомы.
Гуморальные факторы также играют роль в патогенезе раннего ДС. Эти кишечные гормоны включают вазоактивный интестинальный пептид, панкреатические полипептиды, нейротензин, энтероглюкагон, серотонин, пептид YY, мотилин, инсулинотропный пептид. Однако значительное повышение уровня энтеропептидов в развитии ДС полностью не доказано.
Быстрое опорожнение желудка также играет роль в развитии позднего ДС. Стремительное попадание пищи в тощую кишку и абсорбция глюкозы приводит к гипергликемии и гиперинсулинемическому ответу. Далее это ведет к гипогликемии через 2-3 часа после еды.
Диагностика ДС основана на данных анамнеза и провокацией симптомов оральным введением глюкозы. Для подтверждения ускоренной эвакуации жидкой и кашицеобразной пищи может быть использовано исследование с радиоактивным изотопом. Эндоскопия и рентгенография помогают в идентификации анатомии и диагностике других постгастрорезекционных симптомов.
У многих больных со временем тяжесть симптомов снижается. Подбор диеты – основа лечения. Больной должен быть обучен питаться дробно — часто и понемногу, с малым количеством углеводов и высоким уровнем белка. Часто помогает сухоедение с приемом жидкости через полчаса после основной твердой пищи. Больные должны потреблять клетчатку и ограничивать жир, а также отдавать предпочтение сложным углеводам (овощи) вместо простых (сахар). Если симптомы переносятся тяжело, пациент должен лечь на полчаса или час после еды. Многие больные интуитивно приходят к этому сами.
Большинство пациентов справляются диетой, но некоторым нужно дополнительное лечение. Добавление диетической клетчатки эффективно, так как она задерживает абсорбцию и удлиняет время транзита по кишечнику, хотя вкусовая привлекательность этих волокон весьма низка. Остеотид, аналог соматостатина, в виде подкожных инъекций с успехом применяют для лечения раннего и позднего ДС. Он воздействует на различные звенья патогенеза демпинга. Задерживает время опорожнения желудка и транзит по кишечнику, особенно натощак, за счёт блокады кишечных пептидов, ответственных за моторику кишечника. Остеотид также блокирует освобождение инсулина, абсорбцию глюкозы и тонкокишечную секрецию. Ингибирует вазодилатацию периферических сосудов, вызванную приемом пищи. Отдаленные осложнения остеотида неизвестны.
Для хирургического лечения ДС предложены сложные операции, как реконструкция привратника, сужение гастроеюноанастомоза, перевод соустья по Б-II в Б-I(редуоденизация), тонкокишечная интерпозиция, реконструкция анастомоза по Ру. Хотя первичный успех возможен, отдаленные результаты неутешительны. Хирургия — крайняя мера у больных с тяжелым ДС, резистентным к диете и медикаментозному лечению.
У больных, перенесших ранее пилоропластику, реконструкция привратника вполне возможна. Непрерывность пилорического кольца восстанавливают путем сближения пересеченных ранее мышечных волокон. Эта процедура проста и неопасна, но вероятность успеха весьма вариабельна. Сужение анастомоза весьма понятно, как концепция, но редко бывает успешна. Трудно заранее судить о размерах стомы, которая предотвратит ДС, но не приведет к стойкому нарушению эвакуации из желудка. К тому же, со временем может произойти стриктура или растяжение соустья. Перевод анастомоза из Б-II в Б-I восстанавливает дуоденальный пассаж, редко сопровождается осложнениями и приводит к смягчению симптомов примерно у 75% больных. Однако у 25% по неизвестным причинам, улучшение не наступает. Описаны многие виды еюнальной интерпозиции — изоперистальтические и антиперистальтические. Наиболее эффективен 10 см антиперистальтический еюнальный сегмент, который может быть расположен между желудком и 12-перстной кишкой, в отводящей петле гастроэнтероанастомоза или Ру-анастомоза. Некоторые авторы приводят хорошие результаты, а другие описывают тяжёлые нарушения эвакуации из желудка. Для больных, страдающих ДС после резекции желудка по Б-I или Б-II, реконструкция cY-образным анастомозом по Ру дает более стойкий результат. Пересечение тощей кишки при этой операции формирует эктопический водитель ритма, индуцирующий ретроградные сокращения, затрудняющий транзит химуса и замедляющий опорожнение желудка. Однако это процедура может приводить к развитию Ру-синдрома (см. ниже).
Постваготомная диарея
Хотя диарея и не специфична для желудочной хирургии, ее вероятность выше у больных, перенесших ваготомию. Частота диареи после стволовой ваготомии составляет 20%, после селективной — 5%, а после СПВ — 4%. Симптомы характеризуются частым водянистым стулом, нередко возникающим ночью и, как правило, не связаны с всасыванием углеводов. Атаки наблюдают периодически, продолжительностью нескольких дней, затем они не рецидивируют на протяжении нескольких месяцев. Симптомы ослабевают в течение года и редко подрывают здоровье.
Диагноз постваготомной диареи ставят клинически, важно отличать ее от других постгастрорезекционных симптомов, которые могут сопровождаться частым жидким стулом. Следует дифференцировать осложнение ваготомии от других причин диареи, например анаэробной инфекции, путем проведения специальных диагностических тестов. Больные с персистирующими симптомами могут потребовать обследования желудочно-кишечного тракта: ирригоскопии, колоноскопии, эндоскопии с биопсией слизистой тонкой кишки для исключения других причин расстройства стула.
Патофизиология постваготомной диареи полифакториальна. Быстрое опорожнение желудка часто сопровождается поносом, но хирургическая коррекция не решает проблем. Ускоренное продвижение химуса нередко приводит к малабсорбции питательных веществ. Когда ваготомию выполняют более селективно, частота диареи снижается, что подтверждает концепцию, что причина ее развития состоит в вагальной денервации тонкой кишки и билиарного тракта, потере внешнего контроля за гастроинтестинальной моторикой.
Медикаментозное лечение диареи сходно с ДС, диета имеет основное значение. Полезны антидиарейные препараты, как лоперамид, дифеноксилат и опиаты. Весьма эффективен холестирамин. При безуспешности этих мер назначают остеоцид.
Хирургический путь должен быть зарезервирован для небольшого числа пациентов с хроническими истощающими симптомами, не отвечающими на другие мероприятия. Как обсуждалось ранее, хотя быстрое желудочное опорожнение коррелирует с диареей, хирургическая операция не даёт улучшения. Стратегия, таким образом, состоит в том, чтобы замедлить пассаж по тонкой кишке. Наиболее часто используют 10-15 см антиперистальтический сегмент тощей кишки, расположенный на 100 см дистальнее гастроеюноанастомоза или связки Трейца. Однако результаты этой операции бывают различными.
Щелочной рефлюкс-гастрит
У 5-15% больных, оперированных на желудке, развивается щелочной рефлюкс-гастрит. Симптомы включают жгучую боль в эпигастрии, которую прекращает прием антацидов, они усиливаются после еды или в горизонтальном положении тела, сопровождаются тошнотой, желчной рвотой. Для уменьшения симптомов пациенты нередко ограничивают себя в еде, что приводит к потере веса и анемии. Щелочной рефлюкс-гастрит чаще требует хирургического лечения, чем другие ПГРС.
Патогенез симптомов состоит в том, что желчное кишечное содержимое вступает в контакт со слизистой желудка, после того как привратник был разрушен, отключен или резецирован. Частота осложнения выше после резекции желудка по Б-II, чем по Б-I, или стволовой ваготомии с дренированием. После СПВ рефлюкс не наблюдают. Объем рефлюкса коррелирует с тяжестью симптомов.
Диагноз щелочного рефлюкс-гастрита ставят методом исключения. Рецидив язвы, гастропарез, синдром приводящей или отводящей петли, заболевания поджелудочной железы и желчного пузыря должны быть отвергнуты. Гастроскопия с биопсией наиболее распространена. Она исключает рецидив язвы и синдром приводящей петли, которые также бывают причиной желчной рвоты. Для слизистой желудка типична гиперемия, окрашивание желчью. Поверхностный гастрит и эрозии поражают всю поверхность слизистой культи желудка, но более выражены в зоне малой кривизны. Гистологически определяют уменьшение числа обкладочных и главных клеток, снижение числа клеток, продуцирующих муцин, изъязвление и атрофию слизистой, признаки хронического воспаления желудочных желез, искажение их анатомии, интестинальную метаплазию. Однако тяжесть симптомов не коррелирует с изменениями гистологических данных. Рентгенография желудка малоинформативна, она лишь помогает уточнить послеоперационную анатомию и исключить другие ПГРС, как рецидив язвы и непроходимость.
Подтверждение и определение количества рефлюкса в желудок может быть оценено с помощью сканирования при помощи холецистокинина. Больному дают радиоактивный препарат, накапливающийся в печени и определяют радиоактивность над печенью, желчным пузырём, желчевыводящими путями, тонкой кишкой и культей желудка. Дополнительно введение в желудок щелочного раствора используют, как провокационный тест для диагностики и определения рефлюкса, и отбора больных — кандидатов для операции. Тест состоит во введении в желудок стандартных растворов —0.1 NHCl, и 0.1 NNaOH. Позитивным ответом считают появление симптомов после введения щелочи, но не других растворов. Медикаментозное лечение, как правило, не эффективно. Однако холестирамин может быть использован для связывания желчных кислот, вызывающих гастрит. Антациды также связывают желчные кислоты и лизолецитин. Стимуляторы моторики и антибиотики неэффективны.
Суть хирургического лечения состоит в отведении дуоденального содержимого от культи желудка. Наиболее часто используют гастроеюностомию по Ру с длиной петли не менее 45 см. Если ваготомия не была выполнена ранее, её следует провести во время наложения Y-образного анастомоза для профилактики образования язвы соустья. Другая альтернатива — интерпозиция изоперистальтического еюнального сегмента между культёй желудка и тонкой кишкой. Операции дают хороший ближайший, но не всегда удовлетворительный отдаленный результат. Эпигастральная боль рецидивирует у 30% больных, а тошнота и рвота — у 50%.
Потенциальной проблемой этих операций может быть задержка желудочного опорожнения твёрдой пищи — раннее насыщение, эпигастральная боль, рвота без желчи. Все это определяют, как Ру-синдом, развитие которого наиболее вероятно у больных с исходной задержкой опорожнения. Поэтому предоперационное изучение темпа эвакуации из желудка обязательно. Дополнительная его субтотальная ререзекция может ускорить опорожнение желудка.
Синдромы приводящей и отводящей петли
Это осложнение требует присутствия приводящей и отводящей петли, поэтому встречается только после резекции по Б-II или Ру. Любой из двух симптомов — приводящей и отводящей петли — обусловлен обструкцией и сопровождаются развитием острой и полной, либо хронической частичной непроходимости. Синдром приводящей петли (СПП) встречается чаще и обусловлен анатомическими факторами. Известны случаи внутреннего грыжеобразования, заворота петли и узлообразования анастомоза. Эти осложнения чаще наблюдают при впередиободочном расположнии анастомоза или при длинной приводящей петле (более 10-15 см). Сегодня симптом встречается после резекции желудка с частотой 1%.
Острая обструкция приводящей петли нередко приводит к несостоятельности дуоденальной культи и требует экстренного вмешательства. Осложнение проявляется на первой или второй неделе после операции. Желчь и панкреатический сок накапливаются внутри петли. По мере подъема давления происходит обструкция желчных и панкреатических протоков с возможным развитием некроза тонкой кишки. Пациенты жалуются на сильную боль в эпигастрии, тошноту и рвоту. Уровень амилазы повышается, на операции может быть выявлен некроз приводящей кишки. Если вовлечена лишь дистальная часть петли, выполняют ее резекцию с анастомозом по Ру. Вовлечение в процесс подковы 12-перстной кишки требует выполнения панкреатодуоденальной резекции. Заворот кишки может рецидивировать, поэтому избыток кишки должен быть резецирован. Ретроанастомотическое пространство и все мезентериальные дефекты должны быть ушиты для предотвращения рецидива грыжи.
Хронический СПП является результатом частичной обструкции кишки. Дополнительными анатомическими факторами признана стриктура анастомоза, наружная компрессия спайками или опухолью, рецидив язвы, опухоль культи желудка, рубцевание отверстия в мезоколон после позадиободочного анастомоза, еюногастральная инвагинация, хотя последнее состояние встречается редко. Симптомы включают в себя тошноту, боль в правом подреберье после еды, желчную рвоту, иногда — фонтаном, чаще без примеси пищи с быстрым стиханием боли после опорожнения. Больные сознательно или бессознательно избегают пищи и худеют.
Сбор анамнеза помогает в диагностике СПП, однако щелочной рефлюкс-гастрит всегда присутствует. КТ и УЗИ уместны, однако эндоскопия остается методом выбора. Она позволяет напрямую осмотреть анастомоз и взять биопсию. Если диагноз подтвержден, показана операция. Анастомоз по Б-II должен быть реконструирован в Б-I или Ру.
Обструкция отводящей петли встречается реже, как правило, в результате формирования ретроанастомотической грыжи. Другие причины — спайки, фиброз и еюногастральная инвагинация. Синдром также может иметь острую или хроническую форму. Беспокоят схваткообразные боли, тошнота и рвота — пищей с желчью. Диагноз ставят рентгенологически с задержкой контраста на уровне обструкции отводящей петли. Показана операция, которая состоит в рассечении спаек, ликвидации грыжи, укрытии анатомического дефекта, ревизии анастомоза или переводе его в Б-I или Ру.
Хроническая атония желудка и Ру-синдром
Хроническая желудочная атония характеризуется тошнотой, рвотой, болями в эпигастрии, вздутием после еды и образованием безоаров. Больные не переносят твердую пищу, но принимают жидкую, интуитивно формируя свою диету. Это осложнение связано с нарушением вагальной иннервации желудка, частота зависит от вида выполненной ранее ваготомии. Вероятность задержки опорожнения желудка выше при менее селективной ваготомии. Так как перистальтические сокращения антрального отдела желудка и тоническое сокращение его проксимальной части в позднюю фазу желудочного опорожнения находятся под контролем вагуса.
Оценка больных с хронической желудочной атонией начинается с эндоскопического исключения механического характера обструкции. Сцинтиграфия подтверждает задержку эвакуации твердой пищи. Медикаментозное лечение подразумевает использование прокинетиков. Может потребоваться постоянная или временная декомпрессия желудка. Прокинетики включают бетанехол, метаклопрамид, домперид, цисаприд, эритромицин. Лечение оказывается эффективным у 30-40% больных. Хирургическое лечение состоит в уменьшении желудочного резервуара, часто в сочетании с резекцией по Ру с длиной петли 45 см.
Дифференциальная диагностика Ру-синдома и желудочной атонии весьма затруднительна. Симптомы схожи. Вероятность самостоятельного существования Ру-синдрома независимо от атонии желудка весьма проблематична. Однако, существование Ру-синдрома после тотальной гастрэктомии с эзофагоеюностомией говорит о том, что сама по себе Ру-петля увеличивает риск желудочной атонии. Транзит по самой Ру-петле был изучен сцинтиграфически, установлено замедление транзита по ней. Как ваготомия, так и Ру-петля замедляют желудочное опорожнение, частота эвакуаторных нарушений составляет 27-33%. Несколько факторов дополнительно увеличивают вероятность стаза: исходное дооперационное нарушение эвакуации, большая культя желудка, значительная длина Ру-петли. В патогенезе Ру-синдрома ведущую роль играет отключение Ру-петли от дуоденального водителя ритма с возникновением ретроградных перистальтических волн.
Лечение больных с Ру-синдромом сходно с тактикой при атонии желудка. Важно исключить механическое препятствие. Рентгенография желудка и эндоскопия помогают этому, сцинтиграфия помогает задокументировать задержку химуса в культе желудка, Ру-петле или в обоих образованиях. Медикаментозное лечение редко приносит успех. Хирургическое лечение состоит в субтотальной резекции желудка и укорочении Ру-петли до 40 см, такая операция обеспечивает успех в 70-80% случаев. Следует помнить, что замедление желудочного опорожнения при помощи Ру-петли может играть определенную роль в лечении ДС, хотя клинические результаты противоречивы.
Синдром малой культи желудка
Этот синдром характеризуется быстрым насыщением, вздутием в эпигастральной области после еды и рвотой. Синдром связан с уменьшением резервуарной функции желудка после его резекции, ваготомии или обеих операций. Состояние развивается чаще после удаления более 80% объема желудка. Симптомы обычно проявляются мягко, но приводят, как правило, к потере веса, нарушению питания и анемии.
Диагноз основывается на клинической картине, но механическая обструкция должна быть исключена в каждом случае. Диета состоит в частом дробном питании с добавлением витаминов, препаратов железа, панкреатических энзимов. Некоторым больным помогают спазмолитики. Операция показана пациентам с тяжёлыми симптомами, резистентным к диете и медикаментозному лечению. Хирургическое вмешательство состоит в создании резервуара из дупликатуры тонкой кишки, выполняемого в различных вариантах. Наиболее распространены операции «TannerRoux-19 pouch» или «Hunt-Lawrence». И хотя благоприятный результат может быть получен в 50% случаев, значительное число осложнений в виде стаза, дилатации, язвообразования в петле или резервуаре диктуют строгие показания и понимания операции, как «меры отчаяния».
Рецидив язвы
Рецидив возникает после первичного хирургического лечения пептических язв желудка и 12-персной кишки. Данная патология, совместно с рефлюкс-гастритом, лидирует среди причин неудовлетворительных результатов желудочной хирургии. Наиболее частые симптомы рецидива — боль, сходная с первичной язвенной болью, которую наблюдают в 80-95% случаев. Однако, она трудно отличима от боли, возникающей при других ПГРС. Кровотечения возникают у 40-60% больных, что в 2 раза чаще, чем у не оперированных пациентов с язвенной болезнью. Кровотечения чаще носят скрытый характер, но и массивные геморрагии — не редкость. Перфорации язвы редки, рецидивная язва гастроэнтероанастомоза может пенетрировать в ободочную кишку и вызвать образование свища. При этом наблюдают понос, потерю веса, мутную рвоту, хотя боль обычно не выражена. Частота таких язв в настоящее время не велика, но они могут быть причиной стеноза выходного отдела желудка.
Первый и наиболее информативный диагностический тест — эндоскопия. Пассаж бария необходим для изучения эвакуации из желудка, хотя для визуализации язв он малоинформативен. Большинство язв имеют диаметр 2 см и расположены в области гастроэнтероанастомоза. Точность эндоскопии в их диагностике составляет 90%. Большинство язв отвечает на традиционное медикаментозное лечение.
Основная причина рецидива язвы (60%) — неадекватная или неверно выполненная первичная операция. Неполная ваготомия — наиболее частая причина, наблюдаемая в 1/3 случаев. Анатомия вагуса весьма вариабельна и 12% населения имеют более двух стволов. Большинство парасимпатических нервных волокон, обнаруженных на реоперации, находят справа от пищевода или в заднем параэзофагеальном пространстве, а также в области угла Гиса — криминальные ветви Грасси. В прошлом наиболее частой причиной рецидива была неадекватная резекция желудка, хотя сегодня удаление части органа без ваготомии выполняют редко. Неадекватное удаление антральной слизистой, которая в ряде случаев постирается на 1 см и далее в 12-перстную кишку, может быть причиной «синдрома оставленного антрума» и рецидива язвы, хотя данная ситуация встречается редко. Оставленная антральная слизистая постоянно продуцирует гастрин, который стимулирует желудочную секрецию. Другой редкой причиной рецидива изъязвления может послужить G-клеточная гиперплазия, синдром Золлигера — Эллисона, язва на почве инородного тела и рак. Сопутствующими факторами признаны ульцерогеные лекарства, курение, задержка опорожнения желудка, энтерогастральный рефлюкс, безоар и первичный гиперпаратиреоидизм.
Эндоскопия, наряду с определением уровня кальция и гастрина в сыворотке крови, — ведущий метод в диагностике рецидива язвы. Ели дефект слизистой желудка обнаружен, показана биопсия для исключения рака. Исследование дуоденальной слизистой помогает обнаружить оставшуюся антральную слизистую. Так как больные с гиперпаратиреоидизмом составляют группу риска язвенной болезни, определение уровня кальция в сыворотке показано всем пациентам с рецидивом язвы, как и определение уровня гастрина в сыворотке крови. Концентрация гормона выше 1000 pg/mL позволяет заподозрить синдром Золлингера — Эллисона, тогда как нормальный уровень гастрина исключает это заболевание. Уровень гастрина в сыворотке крови натощак при синдроме оставленного антрума, как правило, в 2-4 раза выше нормы. Задержка желудочного опорожнения говорит о возможной обструкции или атонии желудка, что может приводить к гипергастринемии. При этом концентрация гормона снижается после опорожнения желудка.
Дифференциальная диагностика при умеренном повышении уровня гастрина в сыворотке крови включает в себя синдром Золлингера — Элиссона, оставленную слизистую антрума, постваготомную гипергастринемию, антральную гиперплазию G-клеток. Постваготомная гипергастринемия представляет из себя умеренное повышение уровня гормона в крови, менее, чем в 2 раза, и наблюдается у 30-40% больных после операции. Антральная гиперплазия G-клеток, также именуемая «псевдо-Золлингер — Элиссон синдом», редкая ситуация, сопровождающаяся гипергастринемией и гиперсекрецией при отсутствии гастриномы. Провокационный тест с введением секретина показан этим больным. У пациентов с синдромом Золлингера — Элиссона инъекция секретина приводит к увеличению уровня концентрации гастрина более, чем на 100 pg/mL, чего не происходит после ваготомии. У больных с двухсмысленными результатами пробы с секретином, показана пищевая стимуляция. Стандартная белковая пища увеличивает концентрацию гастрина среди больных с оставленным антрумом или гиперплазией G-клеток.
Если один из диагнозов был установлен, начинают соответствующее лечение. Оставшуюся слизистую антрума удаляют хирургическим методом. При антральной гиперплазии G-клеток показана антрумэктомия. Диагноз гиперпаратиреоидизма требует паратиреоидэктомии. Лечение рака желудка зависит от его стадии. При синдроме Золлигера — Элисона нужно определить, показана ли операция. Вмешательство необходимо у больных с единичной неметастатической гастриномой при неэффективности медикаментозного лечения. Консервативное лечение уместно у больных с синдромом множественных эндокринных неоплазм и при метастатической гастриноме. Первичное исследование исключит наиболее редкие причины рецидива язвы, требующие специфического лечения. Большинство оставшихся случаев связаны с неполной ваготомией и зачастую могут быть излечены медикаментозно. Тест на полноту ваготомии показан при неэффективности медикаментов и высокой вероятности операции. Тест помогает в выборе варианта хирургического вмешательства.
Несколько тестов помогают измерить желудочную секрецию. Первый определяет базальную секрецию, последующий — стимулированную гастрином и пентагастрином. Для определения полноты ваготомии применяют гипогликемический тест Холландера.
Медикаментозное лечение показано больным с неосложненной рецидивной язвой, у которых нет гиперсекреции или нарушения эвакуации из желудка. Стандартные дозы Н2 блокаторов рецепторов гистамина излечивают 80% рецидивных язв. Поддерживающая терапия Н2 блокаторами показана далее на протяжении всей жизни. Отказ от неё приводит к быстрому рецидиву. Ясно, что приём ульцерогенных препаратов, курение и алкоголь должны быть исключены.
Операция показана, если рецидив не излечивается спустя 3 месяца после начала медикаментозной терапии; если язва рецидивирует в течении года на фоне поддерживающей терапии; когда язвенная болезнь протекает с короткими ремиссиями или вообще без оных; если образ жизни не может быть признан здоровым, или больной не в состоянии проводить рекомендованное врачом консервативное лечение. Должны быть приняты во внимание характер первичной операции и общее состояние пациента. Все больные перед операцией должны пройти тест на полноту ваготомии. Опорожнение желудка также следует изучить у каждого пациента.
Если тест показывает неполную ваготомию с адекватной эвакуацией, показана реваготомия. Многие хирурги также рекомендуют резекцию желудка, если она не была частью предшествующей операции. Если нарушение моторики имеет место, резекция желудка должна быть полноценной с оставлением небольшой культи. При сопутствующем щелочном рефлюкс-гастрите оптимальна реконструкция анастомоза по Ру.
Рак культи желудка
Хорошо известно, что операция на желудке при доброкачественном заболевании увеличивает риск развития рака желудка в последующем. Латентный период обычно превышает 15 лет. Это касается любых операций на желудке — как резекции, так и ваготомии, тем не менее, чаще это позднее осложнение наблюдают после резекции по Б-II.
Наиболее частые симптомы — боль в эпигастральной области, переполнение, рвота, дисфагия, потеря веса, кровотечение, обструкция. Так как эти симптомы сходны с рецидивом язвы или другими ПГРС, диагностика его сложна. Учитывая длительный латентный период при раке желудка, опухоль следует заподозрить при изменении характера жалоб или появлении новых гастроинтестинальных симптомов. Часто больной обращается с неспецифическими жалобами и симптомами, которые первоначально отвечают на медикаментозное лечение. Диагноз ставят на основании эндоскопии с биопсией. Хирургическое лечение обязательно, однако результаты нельзя признать удовлетворительными, как, впрочем, и у больных с первичным раком ранее не оперированного желудка.